Clear Sky Science · it
La meccanoporazione microfluidica con goccioline parallelizzata consente una consegna intracellulare dei geni robusta e resistente all’intasamento
Perché è importante per le medicine del futuro
Molte delle terapie più promettenti — come l’editing genico e i trattamenti a base di mRNA — richiedono di introdurre biomolecole fragili all’interno di cellule vive in modo sicuro. I metodi attuali possono essere potenti ma spesso danneggiano le cellule, funzionano in modo variabile a seconda del tipo cellulare o sono difficili da scalare fino ai miliardi di cellule necessari per terapie cliniche. Questo articolo presenta un nuovo approccio su chip che consegna materiale genetico alle cellule in modo efficiente, delicato e ad altissimo throughput, risolvendo al contempo un problema pratico ostinato: l’intasamento e il malfunzionamento dei dispositivi durante l’uso.
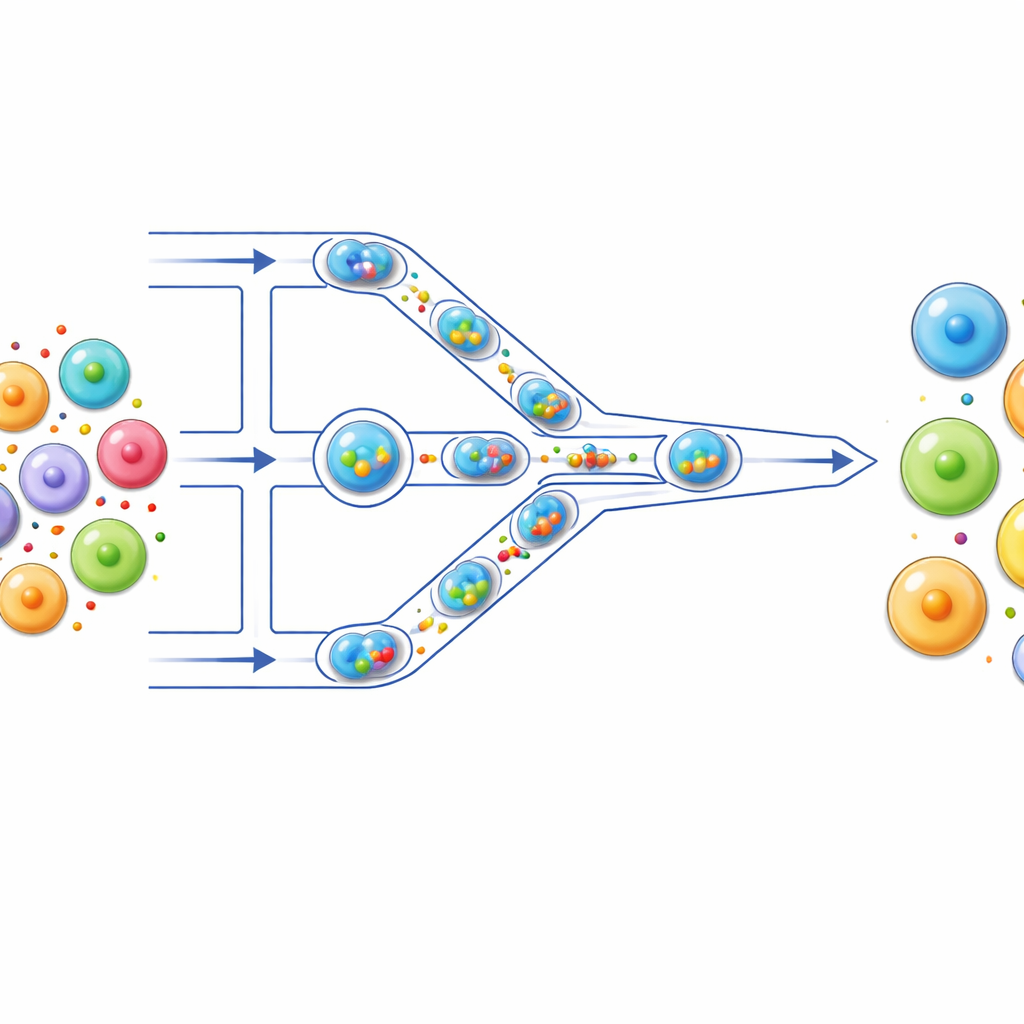
Una piccola linea di montaggio per le cellule
Gli autori hanno costruito una “linea di montaggio” microfluidica in cui le cellule viaggiano attraverso canali sottilissimi su un chip trasparente. Per prima cosa, ogni cellula viene confezionata insieme al suo carico — ad esempio colorante fluorescente, mRNA o componenti CRISPR — all’interno di una gocciolina microscopica d’acqua circondata da olio. Queste goccioline agiscono come piccoli vasi di reazione individuali, mantenendo isolate ciascuna cellula e il suo carico. Mentre le goccioline vengono spinte lungo il canale, incontrano una serie di strozzature strette più piccole delle stesse cellule. Quando una gocciolina le attraversa, la cellula all’interno viene brevemente deformata e poi si rilassa: il ciclo si ripete più volte mentre passa attraverso più strozzature.
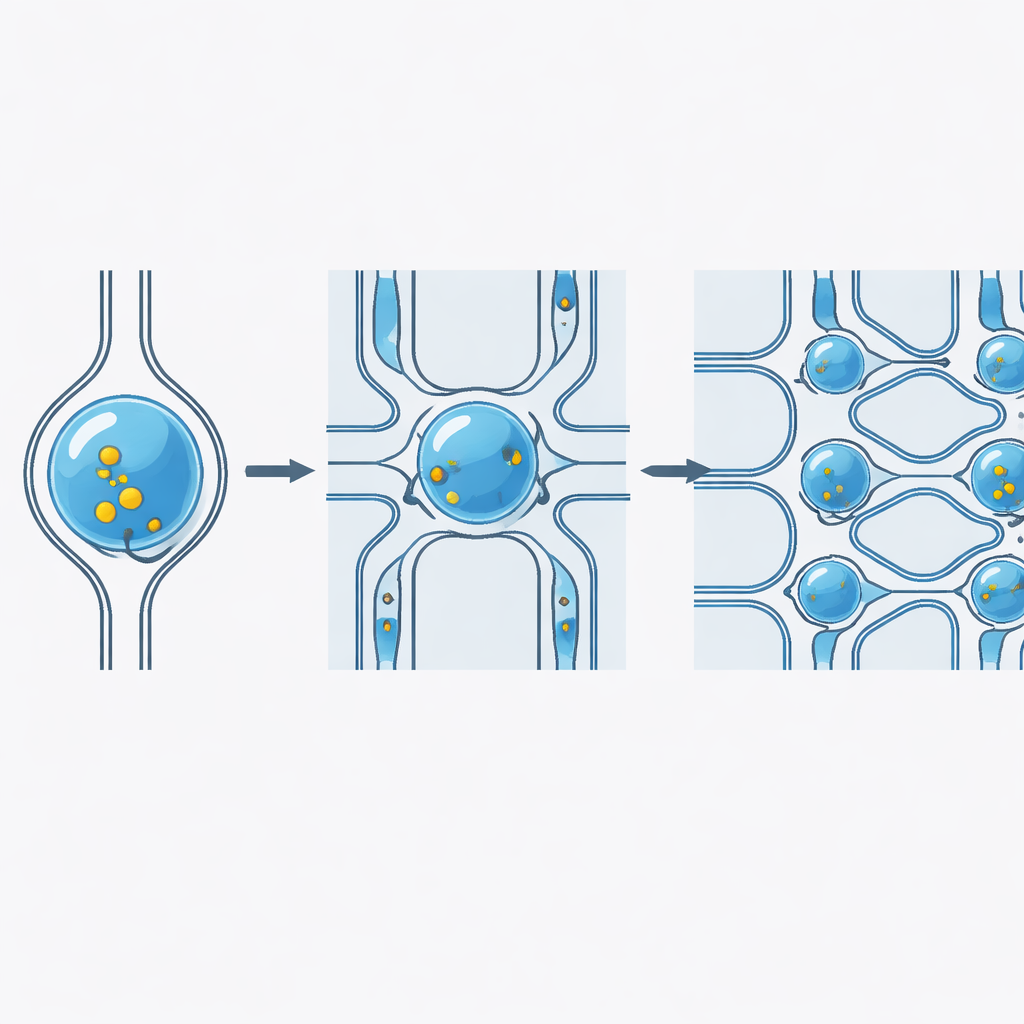
Come una compressione delicata apre la porta della cellula
Quando una cellula morbida viene forzata attraverso una strozzatura più stretta del suo diametro, la sua membrana si allunga formando aperture temporanee a scala nanometrica. Poiché la cellula si trova all’interno di una gocciolina che scorre rapidamente attraverso la strozzatura, il flusso di fluido scorre sulla superficie cellulare e spinge le molecole cargo attraverso queste piccole aperture verso l’interno della cellula. Una volta che la gocciolina esce dalla regione stretta, la cellula ritorna alla forma rotonda e la membrana si richiude, trattenendo il carico all’interno. Immagini ad alta velocità e misure quantitative hanno mostrato che velocità di flusso maggiori e dimensioni delle strozzature scelte con cura aumentano l’allungamento della membrana e la consegna, ma i ricercatori hanno tarato questi parametri in modo che la maggior parte delle cellule — oltre l’80% — rimanga viva e sana.
Un design intelligente che resiste agli intasamenti
Una barriera importante all’uso di questi chip al di fuori del laboratorio è l’intasamento: polvere, ammassi cellulari o frammenti di materiale possono bloccare un singolo canale stretto e fermare il sistema. Per superare questo problema, il team ha disposto molte strozzature in parallelo e le ha collegate con canali di bypass che permettono al flusso di deviare intorno agli ostacoli. Questa disposizione parallela e interconnessa stabilizza la pressione all’interno del chip e mantiene le goccioline in movimento anche quando alcuni percorsi sono parzialmente bloccati. I test che hanno confrontato chip con e senza bypass hanno mostrato che il nuovo design non solo mantiene elevata l’efficienza di consegna durante eventi di intasamento, ma migliora anche la quantità di materiale che ogni cellula riceve, con effetti modesti sulla sopravvivenza cellulare.
Funziona con diversi carichi, tipi cellulari e velocità
I ricercatori hanno indagato sistematicamente il comportamento della piattaforma in condizioni realistiche. Hanno consegnato molecole fluorescenti di dimensioni molto diverse, da piccoli coloranti a polimeri di grandi dimensioni, ottenendo sistematicamente efficienze di consegna superiori al 98%, con la quantità introdotta in ogni cellula controllata dalla concentrazione del carico. Il chip ha funzionato su una gamma di linee cellulari umane e animali, incluse cellule derivate dal sangue e cellule aderenti, regolando la larghezza delle strozzature per adattarla alla dimensione e alla rigidità delle cellule. Le prestazioni sono rimaste stabili anche processando fino a 100 milioni di cellule all’ora, indicando che il dispositivo può gestire i numeri di cellule richiesti per terapie cellulari senza perdere efficienza o viabilità cellulare.
Dalle proteine fluorescenti ai geni modificati
Per dimostrare l’impatto pratico, gli autori hanno consegnato mRNA codificante per una proteina fluorescente in cellule leucemiche e hanno confrontato il loro metodo con due tecniche non virali comuni: trasfezione lipidica ed elettroporazione. Il loro chip a compressione di goccioline ha eguagliato o superato l’elettroporazione sia nella frazione di cellule che esprimevano la proteina sia nell’intensità di espressione, mantenendo al contempo più cellule vive rispetto a entrambe le alternative. Hanno poi impiegato la piattaforma per consegnare complessi di editing genico CRISPR/Cas9 in cellule T per eliminare un recettore superficiale chiave. L’editing ha funzionato in oltre il 99% delle cellule, con segnali fluorescenti del recettore bersaglio ridotti di oltre venti volte e viabilità cellulare superiore all’80% per diversi giorni.
Cosa significa per il futuro dell’ingegneria cellulare
In termini semplici, questo studio dimostra che spremere delicatamente cellule incapsulate in goccioline attraverso un array di microcanali progettato per resistere agli intasamenti può caricare materiale genetico in quasi tutte le cellule mantenendo vive la maggior parte di esse, e può farlo a velocità rilevanti per l’industria. La piattaforma gestisce molecole e tipi cellulari diversi, eguaglia o supera i metodi non virali standard e può essere scalata aggiungendo più canali e generatori di goccioline. Con miglioramenti nelle fasi di recupero cellulare, questo approccio potrebbe diventare uno strumento pratico per la produzione di cellule ingegnerizzate per terapie, oltre che un utile strumento per la ricerca di base che richiede una consegna affidabile e quantitativa in grandi popolazioni cellulari.
Citazione: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Parole chiave: consegna genica microfluidica, meccanoporazione con goccioline, trasfezione intracellulare di mRNA, ingegneria cellulare CRISPR, microdispositivi resistenti all’intasamento