Clear Sky Science · de
Parallelisierte Tropfen‑Mikrofluidik‑Mechanoporierung ermöglicht robuste und verklumpungsresistente intrazelluläre Genlieferung
Warum das für zukünftige Medikamente wichtig ist
Viele der spannendsten neuen Therapien – etwa Geneditierung und mRNA‑basierte Behandlungen – hängen davon ab, empfindliche Biomoleküle sicher in lebende Zellen zu bringen. Heutige Methoden können leistungsfähig sein, beschädigen dabei aber oft Zellen, arbeiten inkonsistent zwischen verschiedenen Zelltypen oder sind schwer auf die Milliarden von Zellen zu skalieren, die für Therapien erforderlich sind. Diese Arbeit stellt einen neuen chipbasierten Ansatz vor, der genetisches Material effizient, schonend und mit sehr hoher Durchsatzrate in Zellen bringt und gleichzeitig ein hartnäckiges praktisches Problem löst: das Verstopfen und Ausfallen von Geräten während des Betriebs.
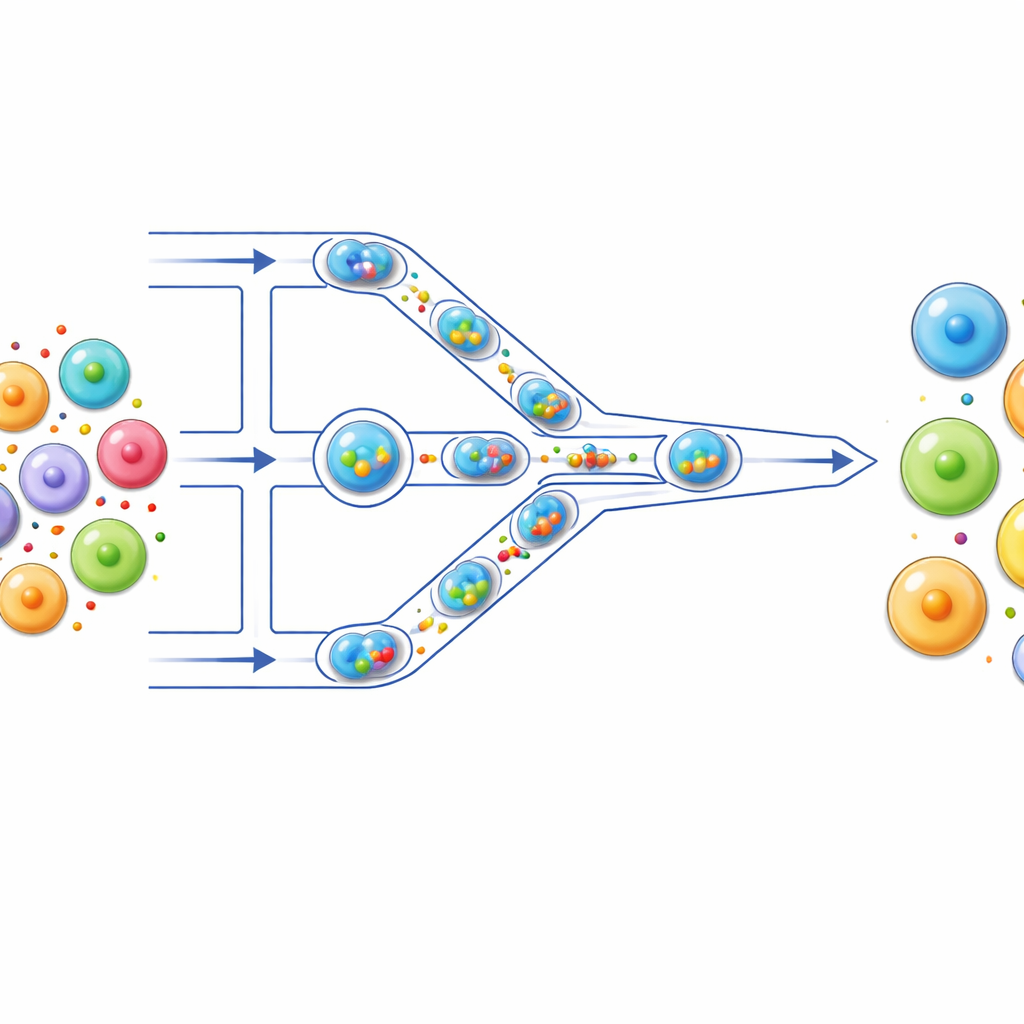
Eine winzige Produktionsstraße für Zellen
Die Autorinnen und Autoren bauten eine mikrofluidische „Produktionsstraße“, in der Zellen durch haarfeine Kanäle auf einem transparenten Chip transportiert werden. Zunächst wird jede Zelle zusammen mit ihrer Fracht – etwa einem fluoreszierenden Farbstoff, mRNA oder CRISPR‑Komponenten – in einem mikroskopisch kleinen Wassertropfen verpackt, der von Öl umgeben ist. Diese Tropfen fungieren wie einzelne Reaktionsgefäße und halten jede Zelle mit ihrer Fracht isoliert. Während die Tropfen durch den Kanal gedrückt werden, treffen sie auf eine Reihe enger Verengungen, die kleiner sind als die Zellen selbst. Wenn ein Tropfen hindurchgepresst wird, wird die darin befindliche Zelle kurzzeitig verformt und kann sich danach wieder entspannen; dieser Zyklus wiederholt sich mehrmals beim Passieren mehrerer Engstellen.
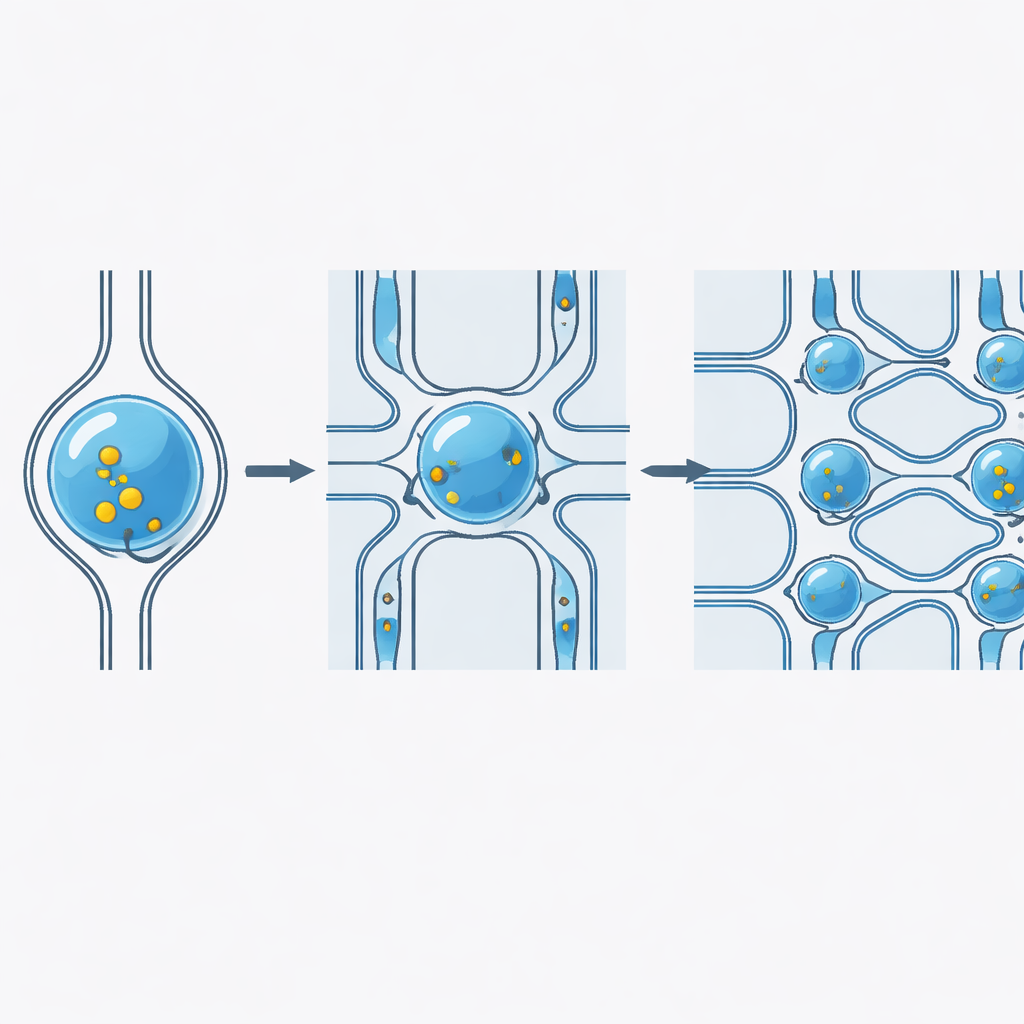
Wie sanftes Quetschen die Zellmembran öffnet
Wenn eine weiche Zelle durch eine Engstelle gezwungen wird, die schmaler als ihr Durchmesser ist, dehnt sich ihre Membran und es bilden sich vorübergehend nanoskalige Öffnungen. Weil sich die Zelle innerhalb eines Tropfens befindet, der schnell durch die Engstelle fließt, strömt Fluid über die Zelloberfläche und drückt Frachtmoleküle durch diese winzigen Öffnungen in das Zellinnere. Sobald der Tropfen den engen Bereich verlässt, schnellt die Zelle in ihre runde Form zurück und die Membran verschließt sich wieder, wobei die Fracht im Inneren eingeschlossen bleibt. Hochgeschwindigkeitsaufnahmen und quantitative Messungen zeigten, dass höhere Flussraten und sorgfältig gewählte Engstellgrößen die Membrandehnung und damit die Lieferung erhöhen, die Forschenden diese Parameter jedoch so einstellten, dass die Mehrheit der Zellen – über 80 % – lebendig und gesund bleibt.
Ein intelligentes Design, das Verstopfungen widersteht
Eine große Hürde für den Einsatz solcher Chips außerhalb des Laboratoriums ist das Verstopfen: Staub, Zellklumpen oder Materialpartikel können einen einzelnen engen Kanal blockieren und das System lahmlegen. Um dem entgegenzuwirken, ordnete das Team viele Engstellen parallel an und verband sie mit Umgehungskanälen, die den Fluss um Hindernisse herum umleiten. Dieses parallele, miteinander vernetzte Layout stabilisiert den Druck im Chip und hält die Tropfen in Bewegung, selbst wenn einige Wege teilweise blockiert sind. Tests, die Chips mit und ohne Umgehungen verglichen, zeigten, dass das neue Design nicht nur die Liefereffizienz während Verstopfungsereignissen hoch hielt, sondern auch verbesserte, wie viel Material jede Zelle erhielt, bei nur geringen Auswirkungen auf das Überleben der Zellen.
Funktioniert über Frachtarten, Zelltypen und Geschwindigkeiten hinweg
Die Forschenden untersuchten systematisch, wie die Plattform unter realen Bedingungen reagiert. Sie lieferten fluoreszierende Moleküle sehr unterschiedlicher Größe – von kleinen Farbstoffen bis zu großen Polymeren – und erreichten konstant Liefereffizienzen über 98 %, wobei die Menge, die in jede Zelle gelangte, durch die Frachtkonzentration gesteuert wurde. Der Chip funktionierte für eine Reihe menschlicher und tierischer Zelllinien, einschließlich blutabgeleiteter und adhärenter Zellen, indem die Engstellenbreite an Zellgröße und -steifigkeit angepasst wurde. Die Leistung blieb stabil, selbst bei der Verarbeitung von bis zu 100 Millionen Zellen pro Stunde, was darauf hinweist, dass das Gerät die für zellbasierte Therapien erforderlichen Zellzahlen bewältigen kann, ohne Effizienz oder Zellvitalität zu verlieren.
Von leuchtenden Proteinen zu editierter DNA
Um praktische Relevanz zu demonstrieren, lieferten die Autorinnen und Autoren mRNA für ein fluoreszierendes Protein in Leukämiezellen und verglichen ihre Methode mit zwei gängigen nicht‑viralen Techniken: lipidbasierter Transfektion und Elektroporation. Ihr Tropfen‑Quetsch‑Chip erreichte bei sowohl dem Anteil der Zellen, die das Protein exprimierten, als auch der Intensität der Expression vergleichbare oder bessere Werte als die Elektroporation, während er mehr Zellen am Leben ließ als beide Alternativen. Anschließend nutzten sie die Plattform, um CRISPR/Cas9‑Geneditierkomplexe in T‑Zellen zu liefern, um einen wichtigen Oberflächenrezeptor auszuschalten. Die Editierung gelang in über 99 % der Zellen, die Fluoreszenzsignale des Zielrezeptors sanken um mehr als das Zwanzigfache, und die Zellvitalität blieb über mehrere Tage bei über 80 %.
Was das für zukünftiges Zellengineering bedeutet
Einfach ausgedrückt zeigt diese Studie, dass das schonende Quetschen tropfen‑verkapselter Zellen durch ein klug gestaltetes, verklumpungsresistentes Mikrokanalnetz nahezu jede Zelle mit genetischer Fracht beladen kann, während die Mehrheit der Zellen überlebt, und das in industriell relevanten Geschwindigkeiten. Die Plattform verarbeitet verschiedene Moleküle und Zelltypen, tritt mit oder übertrifft Standard‑Nicht‑Viral‑Methoden und lässt sich durch Hinzufügen weiterer Kanäle und Tropfengeneratoren skalieren. Mit verbesserten Schritten zur Zellrückgewinnung könnte dieser Ansatz zu einem praktischen Arbeitstier für die Herstellung gentechnisch veränderter Zellen für Therapien werden sowie zu einem vielseitigen Werkzeug für die Grundlagenforschung, die zuverlässige, quantitative Lieferung in große Zellpopulationen benötigt.
Zitation: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Schlüsselwörter: mikrofluidische Genlieferung, Tropfen‑Mechanoporierung, intrazelluläre mRNA‑Transfektion, CRISPR‑Zellengineering, verklumpungsresistente Mikrogeräte