Clear Sky Science · nl
Paralleliseerde druppel-microfluidische mechanoporatie maakt robuuste en verstoppingsbestendige intracellulaire genafgifte mogelijk
Waarom dit belangrijk is voor toekomstige geneesmiddelen
Veel van de meest veelbelovende nieuwe therapieën—zoals genbewerking en mRNA-gebaseerde behandelingen—hangen af van het veilig inbrengen van kwetsbare biomoleculen in levende cellen. Huidige methoden kunnen krachtig zijn, maar beschadigen vaak cellen, werken inconsistent tussen celtypen of zijn moeilijk op te schalen naar de miljarden cellen die voor therapieën nodig zijn. Dit artikel introduceert een nieuwe microchipgebaseerde aanpak die genetisch materiaal efficiënt, zacht en met zeer hoge doorvoer in cellen brengt, terwijl een hardnekkig praktisch probleem wordt opgelost: apparaten die tijdens bedrijf verstopt raken en uitvallen.
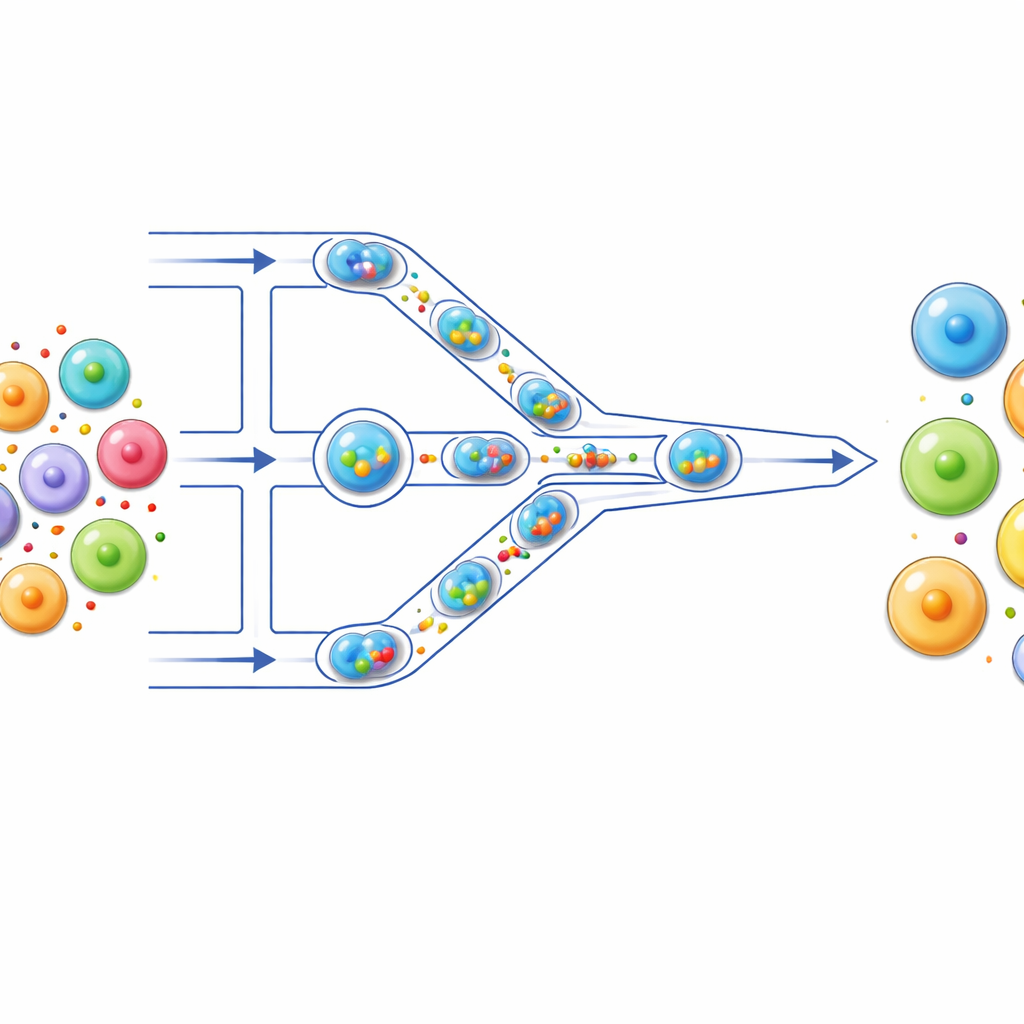
Een minuscule assemblagelijn voor cellen
De auteurs bouwden een microfluïdische "assemblagelijn" waar cellen door haarfijne kanalen over een transparante chip bewegen. Eerst wordt elke cel samen met zijn lading—zoals fluorescerende kleurstof, mRNA of CRISPR-componenten—verpakt in een microscopische waterdruppel omgeven door olie. Deze druppels fungeren als afzonderlijke reactievaten en houden elke cel en diens lading geïsoleerd. Terwijl druppels door het kanaal worden voortgeduwd, komen ze een reeks smalle vernauwingen tegen die kleiner zijn dan de cellen zelf. Wanneer een druppel erdoorheen wordt geperst, wordt de cel erin kort vervormd en daarna weer laten herstellen; die cyclus herhaalt zich meerdere keren terwijl de druppel meerdere vernauwingen passeert.
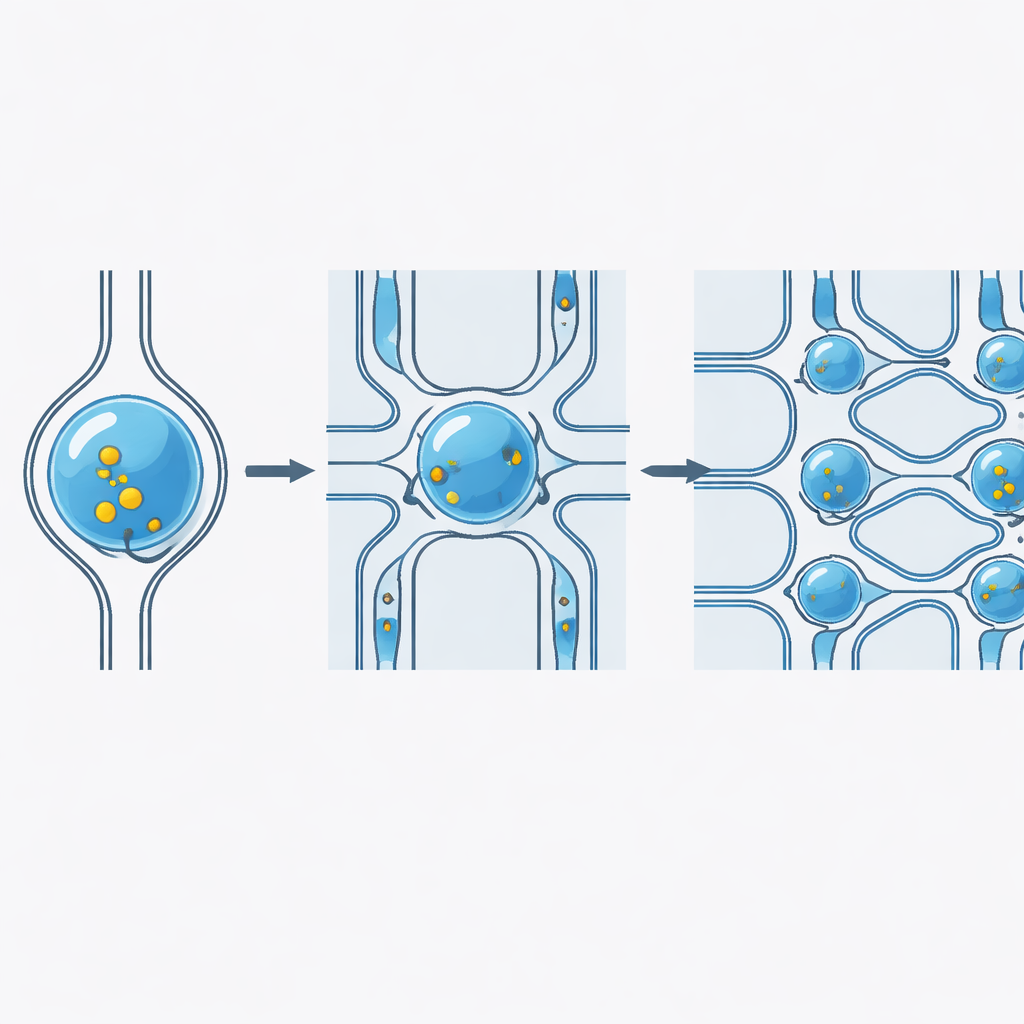
Hoe zacht knijpen de celmembraan opent
Wanneer een zachte cel door een vernauwing wordt geperst die smaller is dan zijn diameter, rekt het membraan uit en ontstaan tijdelijke nanoschaalopeningen. Omdat de cel zich in een druppel bevindt die snel door de vernauwing beweegt, stroomt er vloeistof over het celoppervlak en worden ladingmoleculen door deze kleine openingen in het celinterieur geduwd. Zodra de druppel de nauwe zone verlaat, herstelt de cel zijn ronde vorm en sluit het membraan zich weer, met de lading nu opgesloten. High-speed beeldvorming en kwantitatieve metingen toonden aan dat hogere stroomsnelheden en zorgvuldig gekozen vernauwingsmaten de membraanstrekking en aflevering vergroten, maar de onderzoekers stelden deze parameters zo af dat de meeste cellen—meer dan 80%—levend en gezond blijven.
Een slim ontwerp dat verstoppingen weerstaat
Een belangrijke drempel voor het gebruik van zulke chips buiten het laboratorium is verstopping: stof, celklontjes of stukjes materiaal kunnen een enkel smal kanaal blokkeren en het systeem stilleggen. Om dit te omzeilen plaatste het team veel vernauwingen parallel en verbond ze met bypasskanalen die de stroom rond obstructies laten omleiden. Deze parallelle, onderling verbonden lay-out stabiliseert de druk binnen de chip en houdt druppels in beweging, zelfs wanneer sommige paden gedeeltelijk geblokkeerd zijn. Tests die chips met en zonder bypasses vergeleken, lieten zien dat het nieuwe ontwerp niet alleen de afleveringsefficiëntie hoog hield tijdens verstoppingsgebeurtenissen, maar ook verhoogde hoeveelheden materiaal per cel leverde, met slechts bescheiden effecten op celoverleving.
Werkt voor verschillende ladingen, celtypen en snelheden
De onderzoekers onderzochten systematisch hoe het platform zich gedraagt onder realistische omstandigheden. Ze leverden fluorescerende moleculen van sterk uiteenlopende grootte, van kleine kleurstoffen tot grote polymeren, en bereikten consequent afleveringsefficiënties van meer dan 98%, waarbij de hoeveelheid die elke cel binnenkreeg werd bepaald door de concentratie van de lading. De chip werkte voor een reeks humane en dierlijke cellijnen, inclusief bloedafgeleide en aanhechtende cellen, door de vernauwingbreedte aan te passen aan celgrootte en stijfheid. De prestatie bleef stabiel zelfs bij verwerking van tot 100 miljoen cellen per uur, wat aangeeft dat het apparaat de cel aantallen aankan die nodig zijn voor celgebaseerde therapieën zonder efficiëntie of celviabiliteit te verliezen.
Van oplichtende eiwitten tot bewerkte genen
Om de praktische impact aan te tonen, brachten de auteurs mRNA dat codeert voor een fluorescerend eiwit in leukemiecellen en vergeleken hun methode met twee gebruikelijke niet-virale technieken: lipide-gebaseerde transfectie en elektroporatie. Hun druppel-knijpchip evenaarde of overtrof elektroporatie zowel in het aandeel cellen dat het eiwit tot expressie bracht als in de expressie-intensiteit, terwijl bovendien meer cellen in leven bleven dan bij de alternatieven. Vervolgens gebruikten ze het platform om CRISPR/Cas9-genbewerkingscomplexen in T-cellen af te leveren om een belangrijk oppervlakreceptor uit te schakelen. De bewerking slaagde in meer dan 99% van de cellen, met fluorescerende signalen van de doelreceptor die meer dan twintigvoudig afnamen, terwijl de celviabiliteit boven 80% bleef over meerdere dagen.
Wat dit betekent voor toekomstige celengineering
Kort gezegd laat deze studie zien dat het zacht knijpen van druppel-ingesloten cellen door een slim ontworpen, verstoppingsbestendige microkanaalarray bijna elke cel kan vullen met genetische lading terwijl de meeste cellen behouden blijven, en dat dit kan op industrieel relevante snelheden. Het platform verwerkt verschillende moleculen en celtypen, kan wedijveren met of beter presteren dan standaard niet-virale methoden, en is op te schalen door meer kanalen en druppelgeneratoren toe te voegen. Met verbeterde cel-herstelstappen kan deze aanpak uitgroeien tot een praktisch werkpaard voor de productie van gemodificeerde cellen voor therapieën, en tot een veelzijdig instrument voor fundamenteel onderzoek dat betrouwbare, kwantitatieve aflevering in grote celpopulaties vereist.
Bronvermelding: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Trefwoorden: microfluïdische genafgifte, druppelmechanoporatie, intracellulaire mRNA-transfectie, CRISPR-celengineering, verstoppingsbestendige microapparaten