Clear Sky Science · pt
Microperfuração mecanizada por microfluídica em gotas paralelizada permite entrega gênica intracelular robusta e resistente a entupimentos
Por que isso importa para os medicamentos do futuro
Muitas das terapias mais promissoras — como edição gênica e tratamentos baseados em mRNA — dependem de levar biomoléculas frágeis para dentro de células vivas com segurança. Métodos atuais podem ser potentes, mas frequentemente danificam células, funcionam de forma inconsistente entre tipos celulares ou são difíceis de escalar para os bilhões de células necessários em terapias. Este artigo apresenta uma nova abordagem em microchip que entrega material genético nas células de forma eficiente, delicada e com altíssima vazão, ao mesmo tempo em que resolve um problema prático persistente: o entupimento e falha dos dispositivos durante a operação.
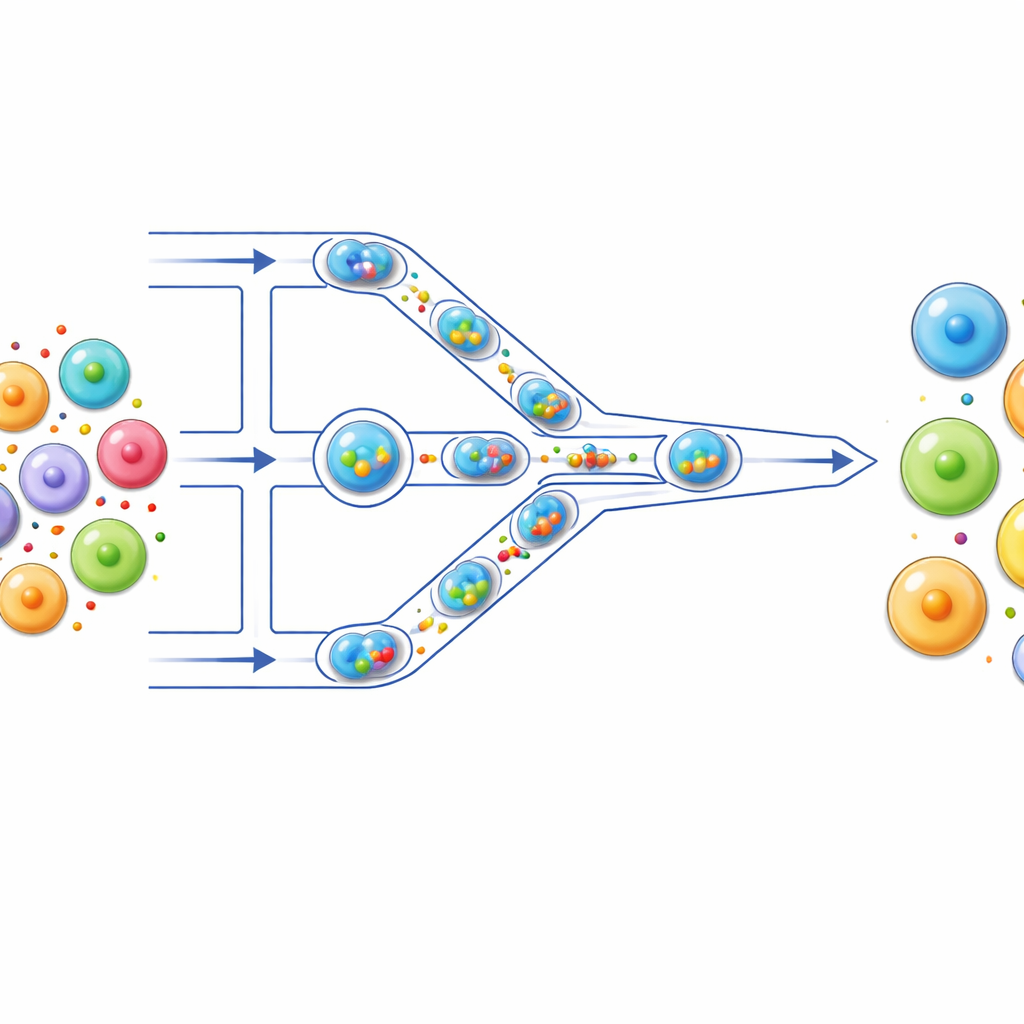
Uma linha de montagem minúscula para células
Os autores construíram uma “linha de montagem” microfluídica onde as células percorrem canais finíssimos em um chip transparente. Primeiro, cada célula é acondicionada junto com sua carga — como corante fluorescente, mRNA ou componentes CRISPR — dentro de uma gotícula microscópica de água rodeada por óleo. Essas gotas funcionam como vasos de reação individuais, mantendo cada célula e sua carga isoladas. À medida que as gotas são empurradas pelo canal, elas encontram uma série de estreitamentos menores do que as próprias células. Quando uma gota passa apertada, a célula no seu interior é brevemente deformada e depois relaxa, um ciclo que se repete várias vezes ao passar por múltiplos estreitamentos.
Como a compressão suave abre a porta da célula
Quando uma célula mole é forçada a atravessar um estreitamento mais estreito que seu diâmetro, sua membrana estica, formando aberturas temporárias em escala nanométrica. Como a célula está dentro de uma gota que se move rapidamente pelo estreitamento, o fluxo de fluido sobre a superfície celular empurra moléculas de carga através dessas pequenas aberturas para o interior da célula. Assim que a gota sai da região estreita, a célula retorna à forma arredondada e a membrana se sela novamente, agora com a carga aprisionada no interior. Imagens de alta velocidade e medições quantitativas mostraram que maiores taxas de fluxo e tamanhos de constrição cuidadosamente escolhidos aumentam o estiramento da membrana e a entrega, mas os pesquisadores ajustaram esses parâmetros de modo que a maioria das células — mais de 80% — permaneça viva e saudável.
Um projeto inteligente que resiste a entupimentos
Uma barreira importante para usar esses chips fora do laboratório é o entupimento: poeira, aglomerados de células ou fragmentos de material podem bloquear um único canal estreito e paralisar o sistema. Para superar isso, a equipe organizou muitos estreitamentos em paralelo e os conectou com canais de desvio que permitem que o fluxo contorne obstruções. Essa configuração paralela e interconectada estabiliza a pressão dentro do chip e mantém as gotas em movimento mesmo quando alguns caminhos estão parcialmente bloqueados. Testes comparando chips com e sem desvios mostraram que o novo projeto não apenas manteve alta eficiência de entrega durante eventos de entupimento, como também melhorou a quantidade de material recebida por cada célula, com efeitos modestos sobre a sobrevivência celular.
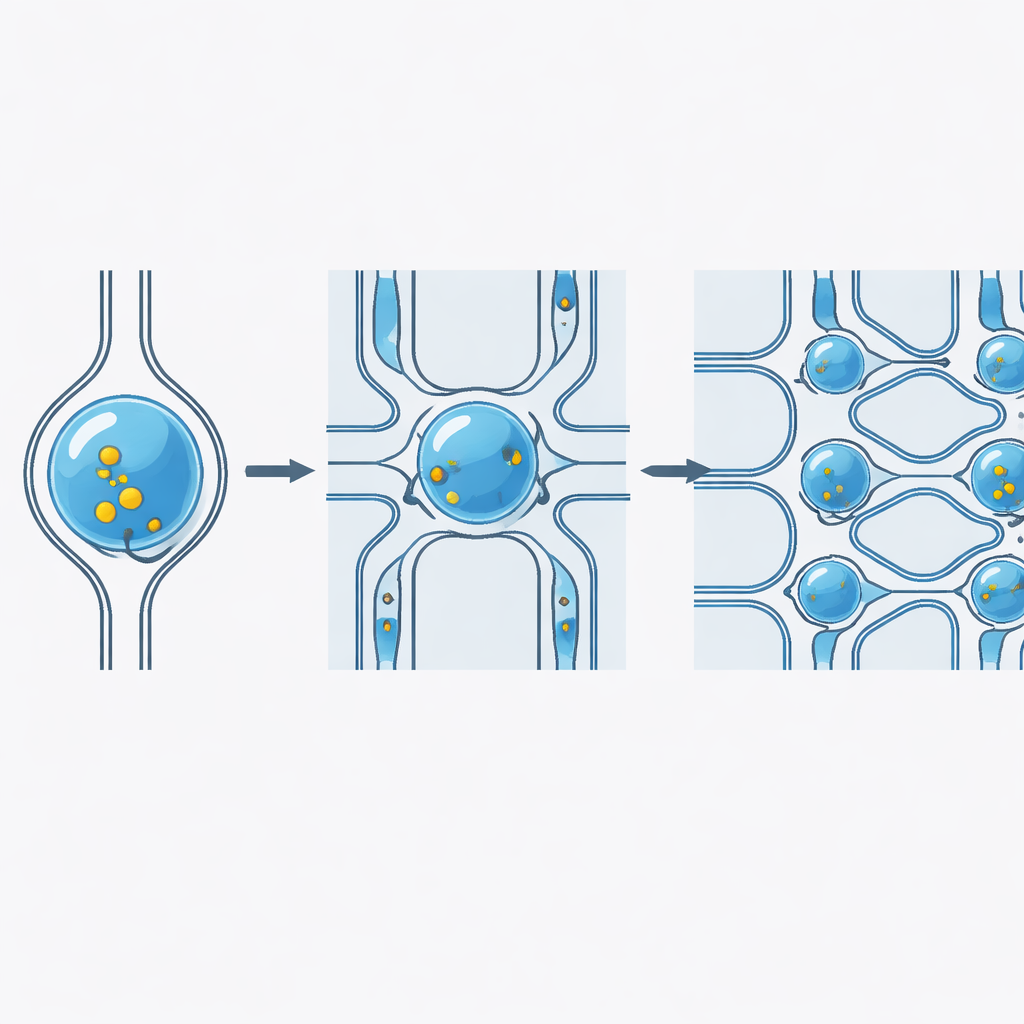
Funciona com diferentes cargas, tipos celulares e velocidades
Os pesquisadores examinaram sistematicamente como a plataforma se comporta em condições do mundo real. Eles entregaram moléculas fluorescentes de tamanhos muito distintos, desde corantes pequenos até polímeros grandes, e alcançaram de forma consistente eficiências de entrega acima de 98%, com a quantidade entregue a cada célula controlada pela concentração da carga. O chip funcionou em uma variedade de linhagens celulares humanas e animais, incluindo células derivadas do sangue e células aderentes, ajustando a largura dos estreitamentos para corresponder ao tamanho e à rigidez celular. O desempenho permaneceu estável mesmo processando até 100 milhões de células por hora, indicando que o dispositivo pode lidar com os números de células exigidos para terapias celulares sem perder eficiência ou viabilidade celular.
De proteínas fluorescentes a genes editados
Para demonstrar impacto prático, os autores entregaram mRNA codificando uma proteína fluorescente em células de leucemia e compararam seu método com duas técnicas não virais comuns: transfecção baseada em lipídios e eletroporação. Seu chip de compressão em gotas igualou ou superou a eletroporação tanto na fração de células que expressaram a proteína quanto na intensidade da expressão, mantendo mais células vivas do que cada alternativa. Em seguida, usaram a plataforma para entregar complexos de edição gênica CRISPR/Cas9 em células T para nocautear um receptor de superfície chave. A edição funcionou em mais de 99% das células, com sinais fluorescentes do receptor alvo caindo mais de vinte vezes, e a viabilidade celular permanecendo acima de 80% por vários dias.
O que isso significa para a engenharia celular futura
Em termos simples, este estudo mostra que comprimir suavemente células encapsuladas em gotas através de uma matriz de microcanais inteligente e resistente a entupimentos pode carregar carga genética em quase todas as células mantendo a maioria delas viva, e pode fazê-lo em velocidades relevantes para a indústria. A plataforma lida com diferentes moléculas e tipos celulares, rivaliza ou supera métodos não virais padrão e pode ser escalada adicionando mais canais e geradores de gotas. Com etapas aprimoradas de recuperação celular, essa abordagem poderia se tornar uma ferramenta prática para a fabricação de células engenheiradas para terapias, além de um recurso versátil para pesquisa básica que precisa de entrega confiável e quantitativa em grandes populações celulares.
Citação: Liu, Q., Chung, A.J. Parallelized droplet microfluidic mechanoporation enables robust and clogging-resistant intracellular gene delivery. Microsyst Nanoeng 12, 157 (2026). https://doi.org/10.1038/s41378-026-01273-6
Palavras-chave: entrega gênica microfluídica, mecanoperfuração em gotas, transfecção intracelular de mRNA, engenharia celular CRISPR, microdispositivos resistentes a entupimentos