Clear Sky Science · tr
Milyon-atom ölçeğindeki biyolojik sistemler için kuantum-mekanik çerçeve
Hayatın İçine Birer Elektronla Bakmak
Proteinlerin, DNA’nın ve virüslerin davranışı, elektronların sürekli hareketine dayanır; ancak gerçekten kuantum düzeyinde simülasyonlar bu büyüklükteki moleküller için uzun süreler boyunca çalıştırılamayacak kadar yavaştı. Bu çalışma, doğruluğu dikkatlice yeterince gevşeterek hesaplamaları hızlı, uygun maliyetli ve biyoloji, tıp ve ilaç tasarımıyla ilgili sorular için şaşırtıcı derecede kullanışlı hâle getiren bir yöntem sunuyor; böylece tam kuantum mekaniği devasa biyolojik yapılara—on milyonlarca atoma kadar—getirilebiliyor.
Neden Büyük Moleküller Kuantum Gözlerine İhtiyaç Duyar
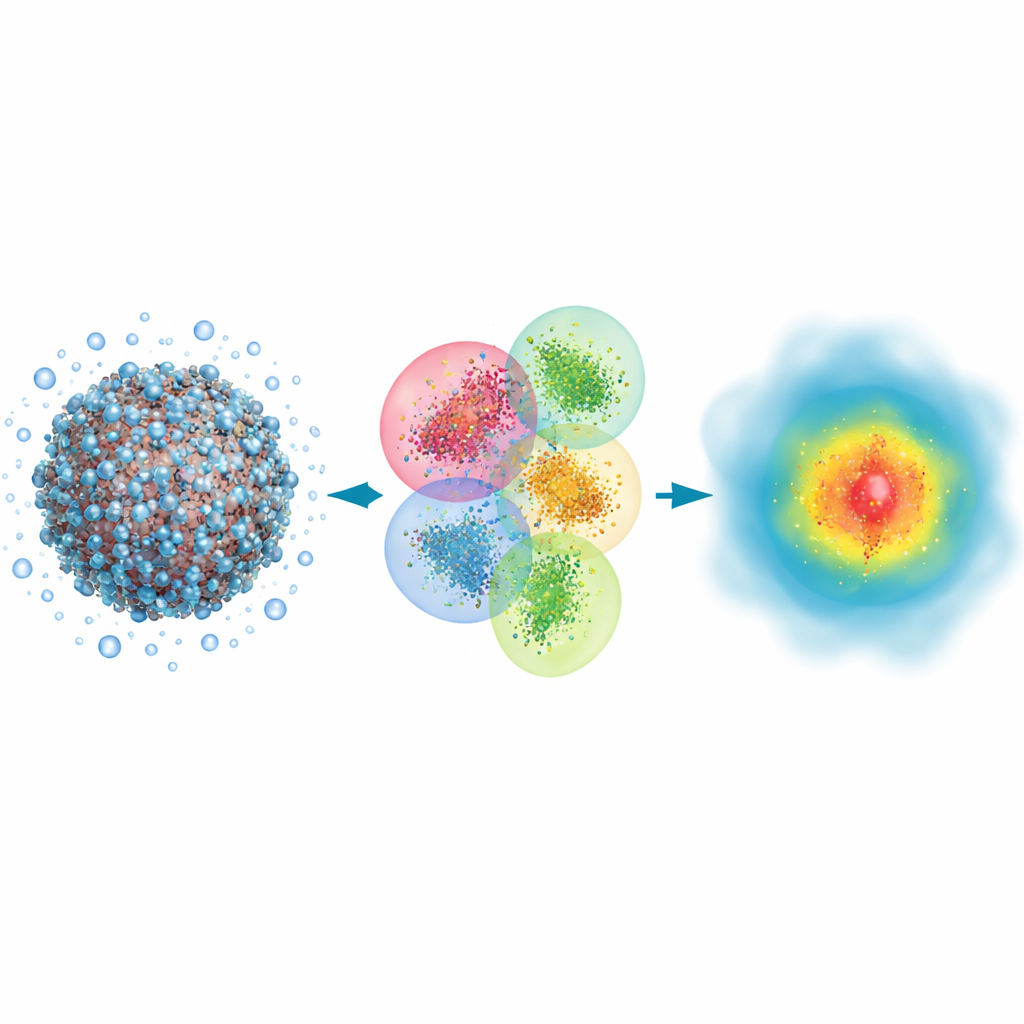
İlaç bağlanmasından görme üzerindeki güneş ışığının etkisine kadar birçok biyolojik olay kimyasal bağların kırılması ve oluşması ile elektron bulutlarının kaymasıyla ilgilidir. Klasik simülasyon yöntemleri büyük proteinler veya DNA içindeki atomların genel hareketini takip edebilir, ancak elektronları ancak dolaylı olarak ele alır ve ışığın nasıl emildiği veya bir ilacın hedefine ne kadar sıkı tutunduğu gibi daha ince etkileri kaçırır. Oysa kuantum-mekanik yaklaşımlar elektronları açıkça izler ve optik spektrumlar gibi özellikleri yüksek doğrulukla tahmin edebilir. Sorun şu ki, geleneksel kuantum yöntemleri sistemler büyüdükçe yürütme maliyeti patlayacak şekilde yavaşlar; bu yüzden tipik olarak yalnızca küçük parçalar için kullanılmış, tüm virüsler veya devasa protein toplulukları erişilemez kalmıştır.
Sorunu Lokma Büyüklüğünde Parçalara Bölmek
Yazarlar, elektronları matematiksel orbitallerle tanımlayan klasik bir kuantum yaklaşımı olan Hartree–Fock’u temel alıyor ve onu en yüksek doğruluktan çok hıza göre yeniden şekillendiriyor. Temel fikirleri, devasa bir biyomolekülü ve etrafındaki suyu birçok örtüşen kümeye bölmek. Her kümenin kuantum sonuçlarının korunduğu merkezi bir çekirdek bölgesi ve komşu atomların etkisini taklit eden bir tampon bölgesi var. Ardından her küme üzerinde ayrı ayrı kuantum hesaplamaları yürütülüyor ve parçalar birleştirilerek sistemin tam elektron yoğunluğu yeniden inşa ediliyor. Ayrıca orbitallerin çok kompakt bir temsili kullanılarak ve nihai cevaba az katkı sağlayan zayıf, uzun menzilli etkileşimler atılarak yöntem maliyetin patlaması yerine yaklaşık olarak atom sayısıyla orantılı ölçekleniyor.
Virüslerden DNA’ya ve Kan İlaçlarına
Bu sadeleştirilmiş çerçevenin neler yapabileceğini göstermek için araştırmacılar birkaç vitrini andıran sistemi ele alıyor. Bunlar arasında su içinde tam elektronik yapısı hesaplanan üç büyük montaj var; bunlardan biri bakterileri enfekte eden bir virüs olan bakteriyofaj ve etrafındaki çözücü kutusu toplamda 45 milyondan fazla atom ve 150 milyondan fazla elektron içeriyor. Modern bir küme üzerinde bu hesaplama yaklaşık yarım günde tamamlanıyor ve yazarların bildiğine göre şimdiye kadar yapılan en büyük Hartree–Fock simülasyonunu temsil ediyor. Ardından ışık emilimine geçiyorlar: yöntemlerinin zaman-bağımlı bir uzantısını kullanarak 21 baz çiftine kadar DNA parçaları ve kanser ilacı Actinomycin D için hem serbest hem de DNA’ya bağlanmış hâlleriyle ultraviyole–görünür spektrumları simüle ediyorlar. Öngörülen spektrumlar deneysel ölçümlerle yakından örtüşüyor; bu, doğruluğun azaltıldığı şemanın bile bu biyomoleküllerin ışıkla nasıl etkileştiğinin temel fiziğini yakaladığını gösteriyor.
AI Tahminli Protein Şekillerini Fizikle Kontrol Etmek
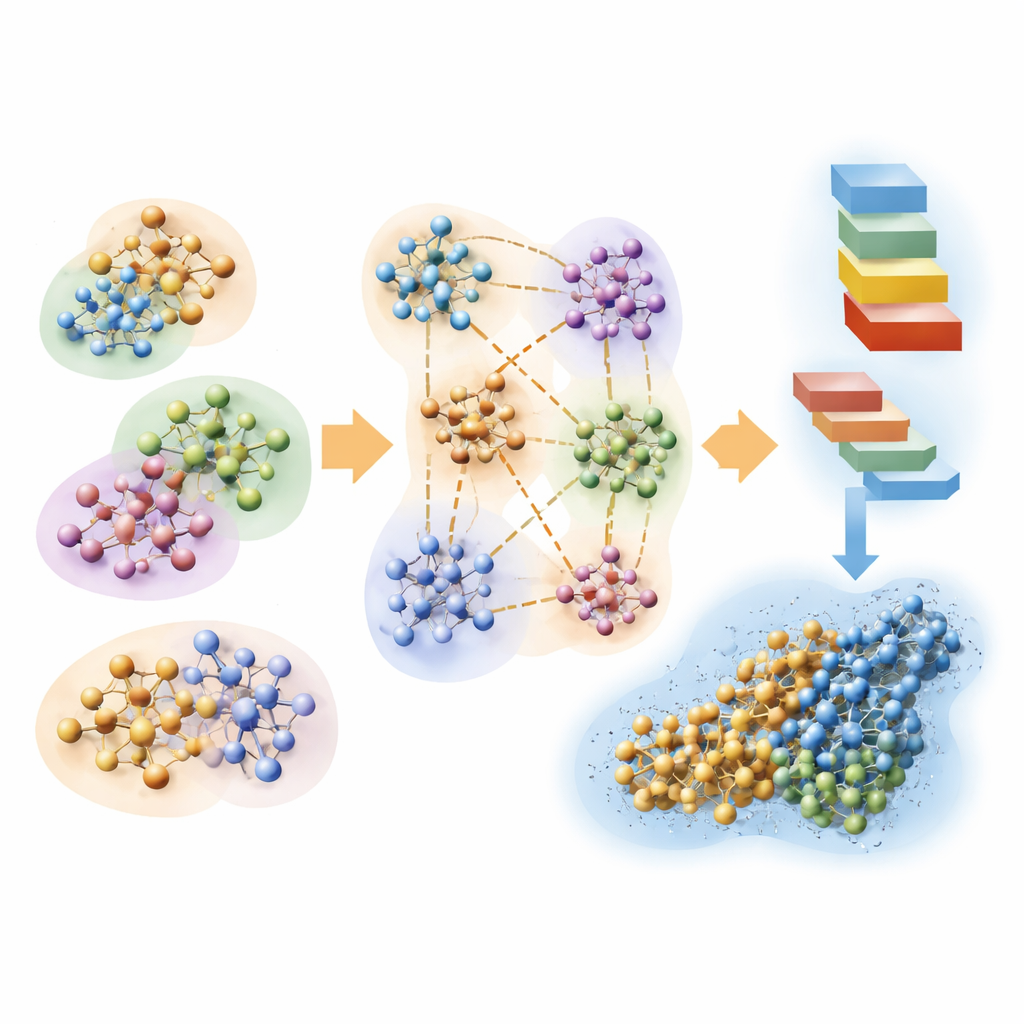
Ekip ayrıca kuantum hesaplarının AI araçları (ör. AlphaFold) tarafından tahmin edilen protein yapılarının değerlendirilmesine ne kadar hızlı yardımcı olabileceğini araştırıyor. Proteinler doğal olarak enerjilerini minimize eden şekillere katlanır. Doğrusal ölçeklenen Hartree–Fock yaklaşımlarını kullanarak yazarlar, birkaç AlphaFold-tahminli proteinin uzunluğu boyunca yerel atomik enerjileri gerçekçi su ortamlarında tahmin ediyorlar. Bu kuantum türevi enerji desenleri AlphaFold’un kendi güven skorlarıyla karşılaştırıldığında çarpıcı şekilde iyi örtüşüyor: düşük enerji bölgeleri AlphaFold’un güvenilir gördüğü alanlarla çakışırken, yüksek enerji belirsiz veya kararsız segmentleri işaretliyor. Bu durum, modern yapı-tahmin ağlarının altta yatan kuantum enerji manzarasının bazı yönlerini örtük olarak öğrendiğini ve birinci ilkelere dayalı hesaplamaların bağımsız, fizik temelli bir kalite kontrolü sağlayabileceğini gösteriyor.
Ödünler, Sınırlar ve Yeni Olanaklar
Hız kazanımları bilinçli ödünlerden kaynaklanıyor. Minimal bir orbital temeli kullanmak ve zayıf, uzak etkileşimleri kesmek bazı doğruluk kayıplarına yol açar; ayrıca böl-ve-yönet stratejisi, sıkı protein–ligand komplekslerindeki hassas bağlanma enerjileri gibi uzun menzilli etkilere hassas şekilde bağımlı nicelikler için ideal değildir. Yazarlar, böylesi yüksek doğruluk gerektiren görevler için kesme değerlerinin gevşetilmesi veya kaldırılması gerektiğini ve yöntemin daha geleneksel, daha yavaş bir kuantum kodu gibi davrandığını gösteriyor. Yine de tamamen doğru bir kuantum muamelesinin hiç mümkün olmadığı çok büyük sistemlerde, yaklaşımları güçlü bir orta yol sunuyor: niteliksel ve çoğu zaman niceliksel olarak güvenilir içgörüler sağlıyor ve mütevazı hesaplama kaynaklarıyla, yaklaşık bir milyon atoma kadar tek düğümlü hesaplama seviyesine kadar inebiliyor.
Moleküler Bilimin Geleceği İçin Anlamı
Standart bir kuantum yöntemini hız lehine yeniden mühendislik ederek deneylerle iyi uyumunu koruyan bu çerçeve, tüm virüslerin, protein makinelerinin ve büyük DNA–ilaç komplekslerinin rutin kuantum düzeyinde çalışmalarına kapı açıyor. Kesin elektron yoğunluğu haritaları sunuyor; bunlar en modern kristalografi sonuçlarıyla doğrudan karşılaştırılabilir, benzeri görülmemiş boyuttaki biyomoleküller için gerçekçi optik spektrumlar sağlar ve AI tarafından üretilen protein yapılarına bağımsız kontroller sunar. İleriye bakıldığında aynı fikirler hızlı kuantum-tabanlı moleküler dinamikleri, elektrik veya manyetik alanların biyomoleküller üzerindeki etkilerinin incelenmesini ve bir sonraki nesil makine öğrenimi modellerini eğitmek için büyük, kuantum-doğru veri setlerinin üretilmesini destekleyebilir. Pratik açıdan, yaşamın makinelerini tam elektronik ayrıntıyla ele alma hayalini—"kuantum biyolojisi"nı—günlük bilimsel uygulamalara daha da yakınlaştırıyor.
Atıf: Wieners, L., Garcia, M.E. A quantum-mechanical framework for million-atom scale biological systems. Commun Chem 9, 170 (2026). https://doi.org/10.1038/s42004-026-02038-y
Anahtar kelimeler: kuantum biyomoleküler simülasyon, Hartree–Fock, protein yapı tahmini, UV-Vis spektrumları, böl ve yönet algoritmaları