Clear Sky Science · ar
إطار ميكانيكي-كمّي للأنظمة البيولوجية بحجم ملايين الذرات
التعمق في جوهر الحياة، إلكترونًا تلو الآخر
تعتمد البروتينات والحمض النووي والفيروسات في سلوكها على الحركة الدؤوبة للإلكترونات، لكن المحاكيات الكمّية الحقيقية للمستويات الكبيرة من الجزيئات كانت لوقت طويل بطيئة للغاية ولا تُجرى إلا على أصغر الأنظمة. يقدم هذا العمل طريقة لجلب الميكانيكا الكمّية الكاملة إلى هياكل بيولوجية هائلة — حتى عشرات الملايين من الذرات — عن طريق تخفيف الدقة بعناية بما يكفي لجعل الحسابات سريعة وميسورة ومفيدة بشكل مفاجئ لأسئلة في علم الأحياء والطب وتصميم الأدوية.
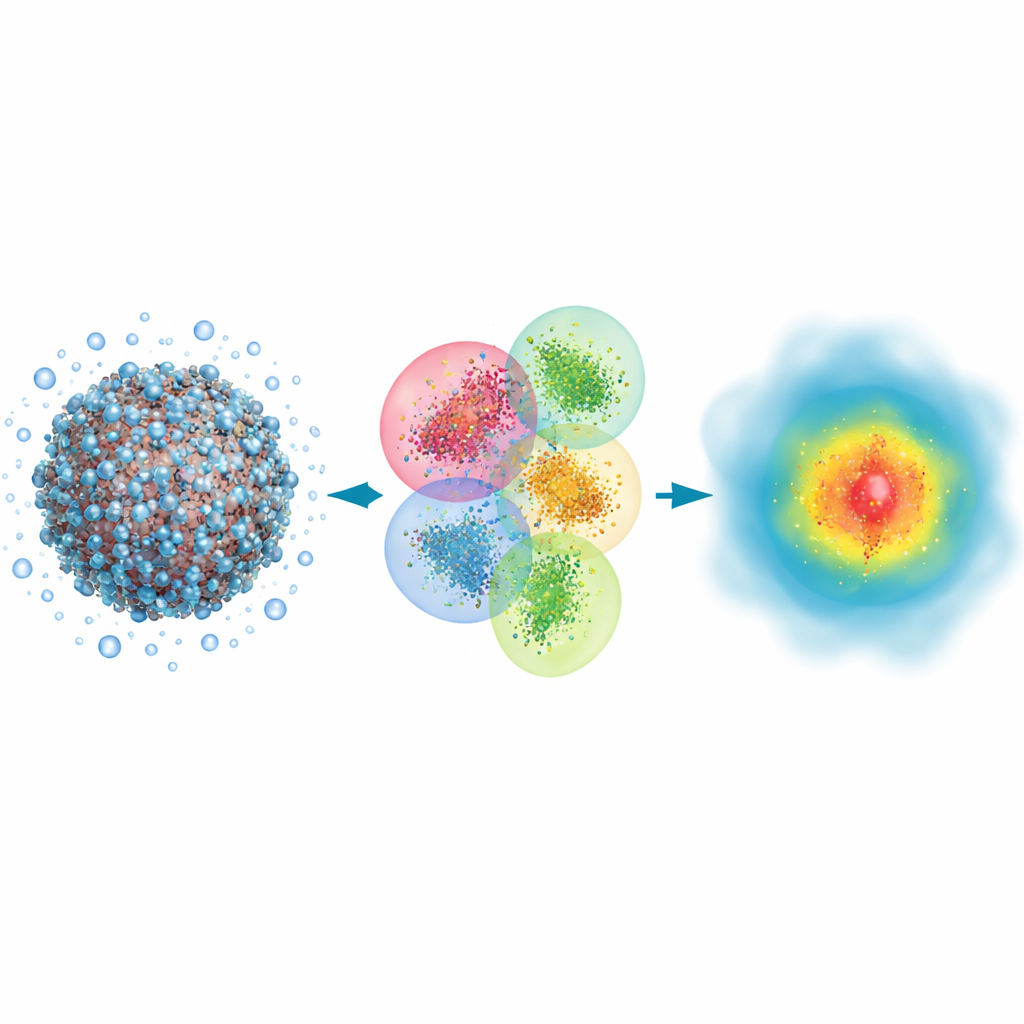
لماذا تحتاج الجزيئات الكبيرة إلى رؤية كمّية
العديد من الأحداث البيولوجية، من ارتباط الدواء إلى تأثير ضوء الشمس على الرؤية، تنطوي على تكسر وتكوين روابط كيميائية وتحولات سحب الإلكترونات. يمكن لطرق المحاكاة الكلاسيكية تتبع الحركة الإجمالية للذرات في البروتينات الكبيرة أو الحمض النووي، لكنها تتعامل مع الإلكترونات بشكل غير مباشر وتغفل بعض التأثيرات الدقيقة التي تحدد كيفية امتصاص الضوء أو مدى تمسك الدواء بمستهدفه. بالمقابل، تتابع الأساليب الكمّية الإلكترونات صراحةً ويمكنها التنبؤ بخصائص مثل الأطياف البصرية بدقة عالية. المشكلة أن الطرق الكمّية التقليدية تبطئ بشكل كبير مع زيادة حجم النظام، لذلك اُستخدمت عادةً فقط لأجزاء صغيرة، تاركة الفيروسات بأكملها أو التجمعات البروتينية الضخمة خارج نطاق الإمكان.
تقسيم المشكلة إلى قطع مناسبة
يعتمد المؤلفون على نهج كمّي كلاسيكي يُدعى هارتري–فوكم الذي يصف الإلكترونات باستخدام مدارات رياضية، ويعيدون تشكيله لصالح السرعة بدلًا من الدقة المطلقة. الفكرة الأساسية لديهم هي تقسيم جزيء حيوي ضخم مع الماء المحيط به إلى العديد من العناقيد المتداخلة. لكل عنقود منطقة مركزية تُحفظ فيها النتائج الكمّية، ومنطقة عازلة تُحاكي تأثير الذرات المجاورة. تُجرى الحسابات الكمّية بشكل منفصل على كل عنقود، وتُركب القطع معًا لإعادة بناء كثافة الإلكترونات الكاملة للنظام. وباستخدام تمثيل مدمج جدًا للمدارات واستبعاد التفاعلات البعيدة الضعيفة التي تساهم قليلًا في الناتج النهائي، يصبح مقياس الطريقة تقريبًا متناسبًا مع عدد الذرات بدلًا من أن يتفجر في التكلفة.
من الفيروسات إلى الحمض النووي وأدوية السرطان
لإظهار ما يمكن أن تفعله هذه الإطار المبسط، يتعامل الباحثون مع عدة أنظمة عرضية. يحسبون البنية الإلكترونية الكاملة لثلاثة تجمعات كبيرة في الماء، بما في ذلك بكتيريوفاج — فيروس يصيب البكتيريا — مع صندوق مذيب محيط يتجاوز 45 مليون ذرة وأكثر من 150 مليون إلكترون. على عنقود حوسبة حديث ينتهي هذا الحساب في حوالي نصف يوم، وهو، بحسب علمهم، أكبر محاكاة هارتري–فوكم تم إجراؤها على الإطلاق. ثم ينتقلون إلى امتصاص الضوء: باستخدام امتداد زمني لطريقتهم، يحاكون أطياف الأشعة فوق البنفسجية–المرئية لقطع من الحمض النووي تصل إلى 21 زوج قواعد وللدواء المضاد للسرطان أكتينوميسين دي، سواء كانت حرة أو مرتبطة بالحمض النووي. تتطابق الأطياف المتوقعة مع القياسات التجريبية عن قرب، مما يبيّن أن مخطط الدقة المخفّضة لا يزال يلتقط فيزياء التفاعل الأساسية بين هذه الجزيئات الحيوية والضوء.
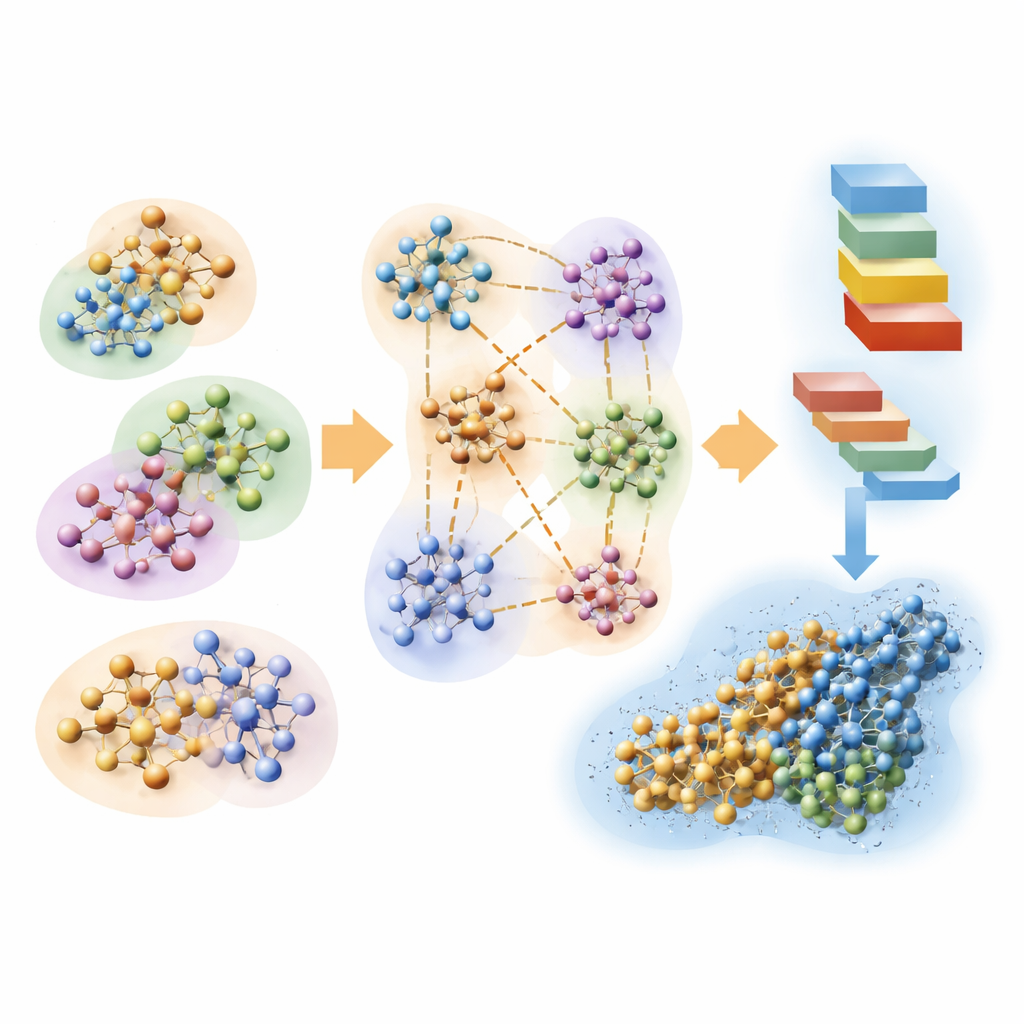
التحقق من أشكال البروتين المتوقعة بالذكاء الاصطناعي عبر الفيزياء
يستكشف الفريق أيضًا كيف يمكن للحسابات الكمّية السريعة أن تساعد في تقييم هياكل البروتين المتوقعة بواسطة أدوات الذكاء الاصطناعي مثل AlphaFold. تنطوي طيّات البروتين طبيعيًا على تشكيل أشكال تقلل طاقتها. باستخدام نهج هارتري–فوكم ذي التحجيم الخطي، يقدّر المؤلفون الطاقات الذرية المحلية على طول عدة بروتينات متوقعة بواسطة AlphaFold، في بيئات مائية واقعية. عندما تقارن أنماط الطاقة المأخوذة من الكمّ مع درجات الثقة لدى AlphaFold، تتطابق بشكل لافت: الطاقة المنخفضة تتزامن مع المناطق التي يعتبرها AlphaFold موثوقة، بينما تشير الطاقات العالية إلى أجزاء غير مؤكدة أو غير مستقرة. هذا يوحي بأن شبكات التنبؤ الحديثة تتعلم ضمنيًا جوانب من تضاريس الطاقة الكمّية الأساسية، وأن الحسابات المُستمدة من المبادئ الأولى يمكن أن تقدم فحصًا مستقلاً قائمًا على الفيزياء لجودة البنى.
مقايضات وحدود وإمكانات جديدة
تنبع مكاسب السرعة من مقايضات مقصودة. استخدام أساس مداري أدنى وقص التفاعلات البعيدة والضعيفة يضحي بالضرورة ببعض الدقة، واستراتيجية القسّم والغلب ليست مثالية للكمّيات التي تعتمد بدقة على التأثيرات بعيدة المدى، مثل طاقات الارتباط الدقيقة في مجمعات البروتين–الرابط الضيقة. يوضح المؤلفون أنه بالنسبة لمثل هذه المهام عالية الدقة يجب تخفيف أو إزالة حدود القص، وتتصرف الطريقة حينها بشكل أقرب إلى كود كمّي تقليدي أبطأ. ومع ذلك، بالنسبة للأنظمة الكبيرة جدًا التي لا يمكن معالجتها كمّياً بدقة كاملة على الإطلاق، يقدم أسلوبهم أرضية وسطى قوية: فهو يوفر رؤى نوعية وغالبًا كمية موثوقة بموارد حاسوبية متواضعة، حتى على عقد حسابية فردية للأنظمة التي تصل إلى نحو مليون ذرة.
ماذا يعني هذا لمستقبل علوم الجزيئات
من خلال إعادة هندسة طريقة كمّية قياسية لتفضيل السرعة مع الحفاظ على توافق جيد مع التجارب، يفتح هذا الإطار الباب أمام دراسات روتينية على المستوى الكمّي لفيروسات كاملة وآلات بروتينية ومجمعات حمض نووي–دواء كبيرة. يتيح خرائط كثافة إلكترونية مفصّلة يمكن مقارنتها مباشرة مع تقنيات التبلور الحديثة، وأطيافًا بصرية واقعية لجزيئات حيوية بأحجام غير مسبوقة، وفحوصًا مستقلة على هياكل البروتين المولدة بالذكاء الاصطناعي. وعلى المدى البعيد، يمكن أن تدعم نفس الأفكار ديناميكيات جزيئية كمّية سريعة، ودراسات حول تأثير الحقول الكهربائية أو المغناطيسية على الجزيئات الحيوية، وتوليد مجموعات بيانات كبيرة ذات دقة كمّية لتدريب نماذج تعلم آلي من الجيل القادم. عمليًا، تقرب هذه الإنجازات الحلم البعيد سابقًا "علم الأحياء الكمّي" — المعاملة المفصلة لآليات الحياة على مستوى الإلكترون الكامل — من الممارسة العلمية اليومية.
الاستشهاد: Wieners, L., Garcia, M.E. A quantum-mechanical framework for million-atom scale biological systems. Commun Chem 9, 170 (2026). https://doi.org/10.1038/s42004-026-02038-y
الكلمات المفتاحية: محاكاة حيوية جزيئية كمّية, هارتري–فوك, توقع بنية البروتين, طيف الأشعة فوق البنفسجية–المرئية, خوارزميات القسّم والغلب