Clear Sky Science · fr
Un cadre quantique pour des systèmes biologiques à l’échelle du million d’atomes
Regarder la vie, un électron à la fois
Protéines, ADN et virus tirent tous leur comportement du mouvement incessant des électrons, mais des simulations véritablement quantiques de molécules aussi volumineuses ont longtemps été trop lentes et limitées aux plus petits systèmes. Ce travail présente une manière d’appliquer la mécanique quantique complète à d’énormes structures biologiques — jusqu’à des dizaines de millions d’atomes — en relâchant soigneusement la précision juste ce qu’il faut pour rendre les calculs rapides, abordables et étonnamment utiles pour des questions de biologie, de médecine et de conception de médicaments.
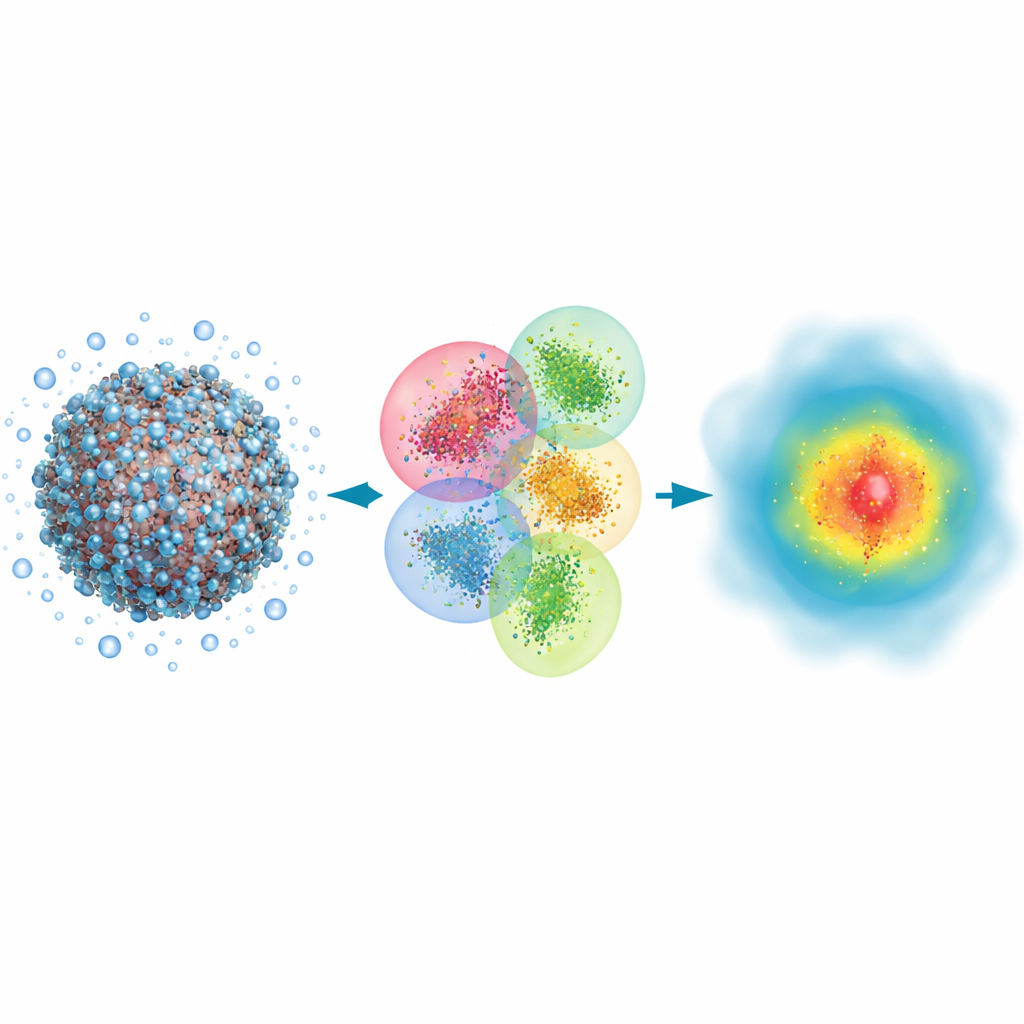
Pourquoi les grandes molécules ont besoin d’yeux quantiques
De nombreux événements biologiques, de la liaison d’un médicament à l’action de la lumière dans la vision, impliquent la rupture et la formation de liaisons chimiques et le déplacement des nuages d’électrons. Les méthodes classiques de simulation peuvent suivre le mouvement global des atomes dans de grosses protéines ou l’ADN, mais elles traitent les électrons de façon indirecte et manquent certains effets plus subtils qui déterminent comment la lumière est absorbée ou à quel point un médicament adhère à sa cible. En revanche, les approches quantiques suivent explicitement les électrons et peuvent prédire des propriétés comme les spectres optiques avec une grande fidélité. Le problème est que les méthodes quantiques traditionnelles ralentissent énormément quand la taille du système augmente, et ont donc été employées surtout pour de petits fragments, laissant entiers virus ou vastes assemblages protéiques hors de portée.
Découper le problème en morceaux maniables
Les auteurs s’appuient sur une approche quantique classique appelée Hartree–Fock, qui décrit les électrons à l’aide d’orbitales mathématiques, et la réaménagent pour privilégier la vitesse plutôt que la précision ultime. Leur idée clé est de diviser une énorme biomolécule et son eau environnante en de nombreux clusters qui se chevauchent. Chaque cluster comporte une région centrale dite cœur où les résultats quantiques sont conservés, et une région tampon qui imite l’influence des atomes voisins. Des calculs quantiques sont ensuite effectués séparément sur chaque cluster, et les morceaux sont recousus pour reconstruire la densité électronique complète du système. En utilisant aussi une représentation très compacte des orbitales et en éliminant les interactions faibles et de longue portée qui contribuent peu au résultat final, la méthode croît à peu près proportionnellement au nombre d’atomes au lieu d’exploser en coût.
Des virus à l’ADN et aux médicaments anticancéreux
Pour démontrer ce que ce cadre allégé permet, les chercheurs traitent plusieurs systèmes emblématiques. Ils calculent la structure électronique complète de trois grands assemblages en solution, y compris un bactériophage — un virus qui infecte les bactéries — avec une boîte de solvant environnante totalisant plus de 45 millions d’atomes et plus de 150 millions d’électrons. Sur un cluster moderne, ce calcul se termine en environ une demi-journée, constituant, à leur connaissance, la plus grande simulation Hartree–Fock jamais réalisée. Ils s’intéressent ensuite à l’absorption de la lumière : en utilisant une extension dépendante du temps de leur méthode, ils simulent des spectres ultraviolet–visible pour des fragments d’ADN allant jusqu’à 21 paires de bases et pour le médicament anticancéreux actinomycine D, libre et lié à l’ADN. Les spectres prédits correspondent étroitement aux mesures expérimentales, montrant que le schéma à précision réduite capture toujours la physique essentielle des interactions lumière–biomolécule.
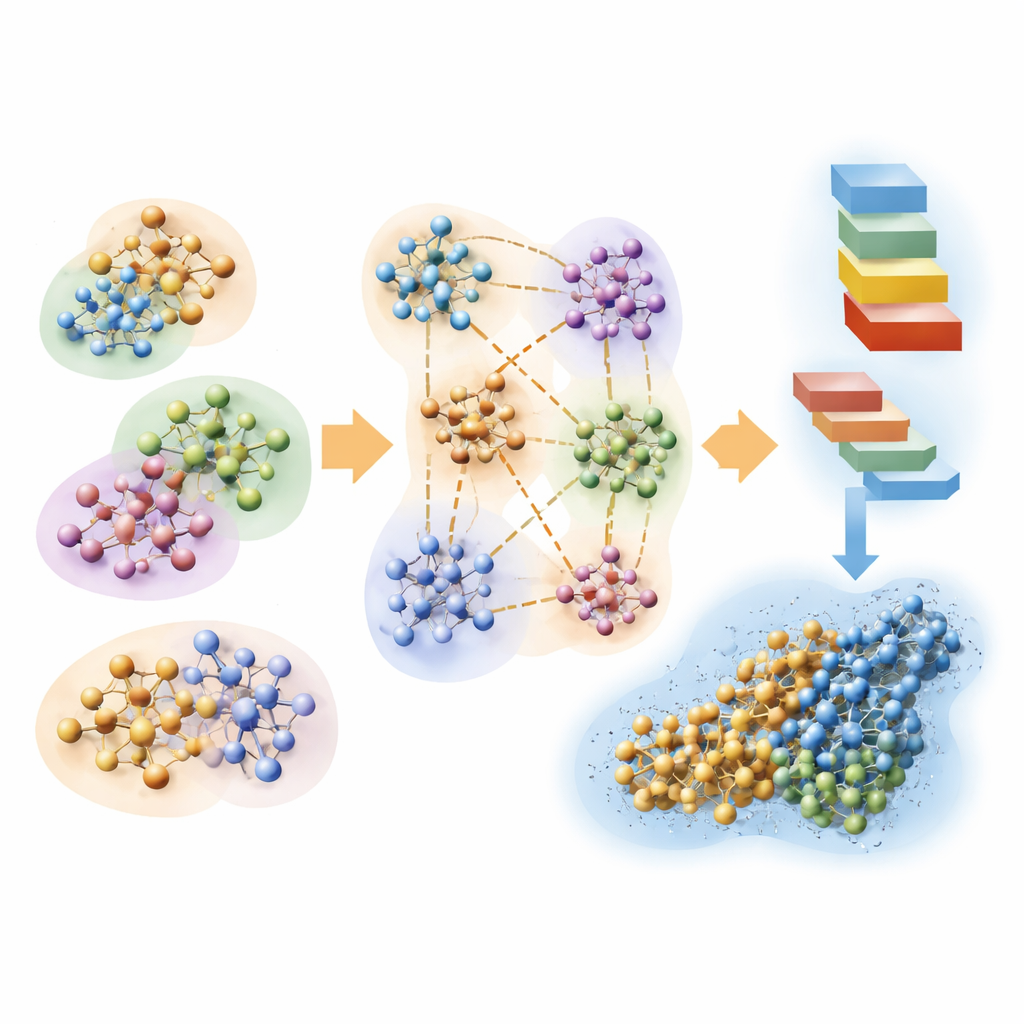
Vérifier les formes protéiques prédictes par l’IA avec la physique
L’équipe explore aussi comment des calculs quantiques rapides peuvent aider à évaluer les structures protéiques prédites par des outils d’intelligence artificielle tels qu’AlphaFold. Les protéines se replient naturellement en formes qui minimisent leur énergie. En utilisant leur approche Hartree–Fock à échelle linéaire, les auteurs estiment les énergies atomiques locales le long de plusieurs protéines prédites par AlphaFold, dans des environnements aqueux réalistes. Lorsque ces profils d’énergie dérivés de la mécanique quantique sont comparés aux scores de confiance d’AlphaFold, ils s’alignent de manière frappante : les basses énergies coïncident avec des régions jugées fiables par AlphaFold, tandis que les hautes énergies signalent des segments incertains ou instables. Cela suggère que les réseaux modernes de prédiction de structures apprennent implicitement des aspects du paysage d’énergie quantique sous-jacent, et que des calculs de premier principe peuvent fournir une vérification indépendante basée sur la physique.
Compromis, limites et nouvelles possibilités
Les gains de vitesse proviennent de compromis conscients. L’utilisation d’une base d’orbitales minimale et la coupure des interactions faibles et lointaines sacrifient nécessairement une partie de la précision, et la stratégie diviser-pour-régner n’est pas idéale pour des grandeurs dépendant finement d’effets de longue portée, comme des énergies de liaison précises dans des complexes protéine–ligand serrés. Les auteurs montrent que pour ces tâches à haute précision, il faut assouplir ou supprimer les coupures, et la méthode se comporte alors davantage comme un code quantique conventionnel et plus lent. Pourtant, pour des systèmes très volumineux où aucun traitement quantique pleinement exact n’est du tout faisable, leur approche offre un terrain intermédiaire puissant : elle fournit des renseignements qualitativement et souvent quantitativement fiables avec des ressources de calcul modestes, jusque sur des nœuds de calcul uniques pour des systèmes d’environ un million d’atomes.
Ce que cela signifie pour l’avenir de la science moléculaire
En réingénierant une méthode quantique standard pour favoriser la vitesse tout en restant en bon accord avec les expériences, ce cadre ouvre la porte à des études de routine au niveau quantique d’entiers virus, de machines protéiques et de grands complexes ADN–médicament. Il permet d’obtenir des cartes de densité électronique détaillées pouvant être comparées directement à la cristallographie de pointe, des spectres optiques réalistes pour des biomolécules d’une taille sans précédent et des contrôles indépendants des structures protéiques générées par l’IA. À l’avenir, les mêmes idées pourraient soutenir des dynamiques moléculaires quantiques rapides, des études sur l’influence des champs électriques ou magnétiques sur les biomolécules, et la génération de grands jeux de données quantiquement exacts pour entraîner les modèles d’apprentissage automatique de nouvelle génération. En termes pratiques, cela rapproche le rêve jadis lointain de la « biologie quantique » — traiter la machinerie de la vie avec le détail électronique complet — de la pratique scientifique quotidienne.
Citation: Wieners, L., Garcia, M.E. A quantum-mechanical framework for million-atom scale biological systems. Commun Chem 9, 170 (2026). https://doi.org/10.1038/s42004-026-02038-y
Mots-clés: simulation quantique biomoléculaire, Hartree–Fock, prédiction de structure protéique, spectres UV-Vis, algorithmes diviser-pour-régner