Clear Sky Science · ru
Квантово-механическая система для биологических систем масштаба миллиона атомов
Заглядывая в жизнь по одному электрону
Белки, ДНК и вирусы во многом определяют своё поведение благодаря неугомонному движению электронов, но полноценные квантовомеханические расчёты таких больших молекул долгое время были слишком медленными и применялись лишь к самым маленьким системам. В этой работе предложен подход, который позволяет применить полную квантовую механику к огромным биологическим структурам — до десятков миллионов атомов — за счёт осторожного ослабления точности настолько, чтобы расчёты стали быстрыми, доступными по ресурсам и на удивление полезными для задач в биологии, медицине и дизайне препаратов.
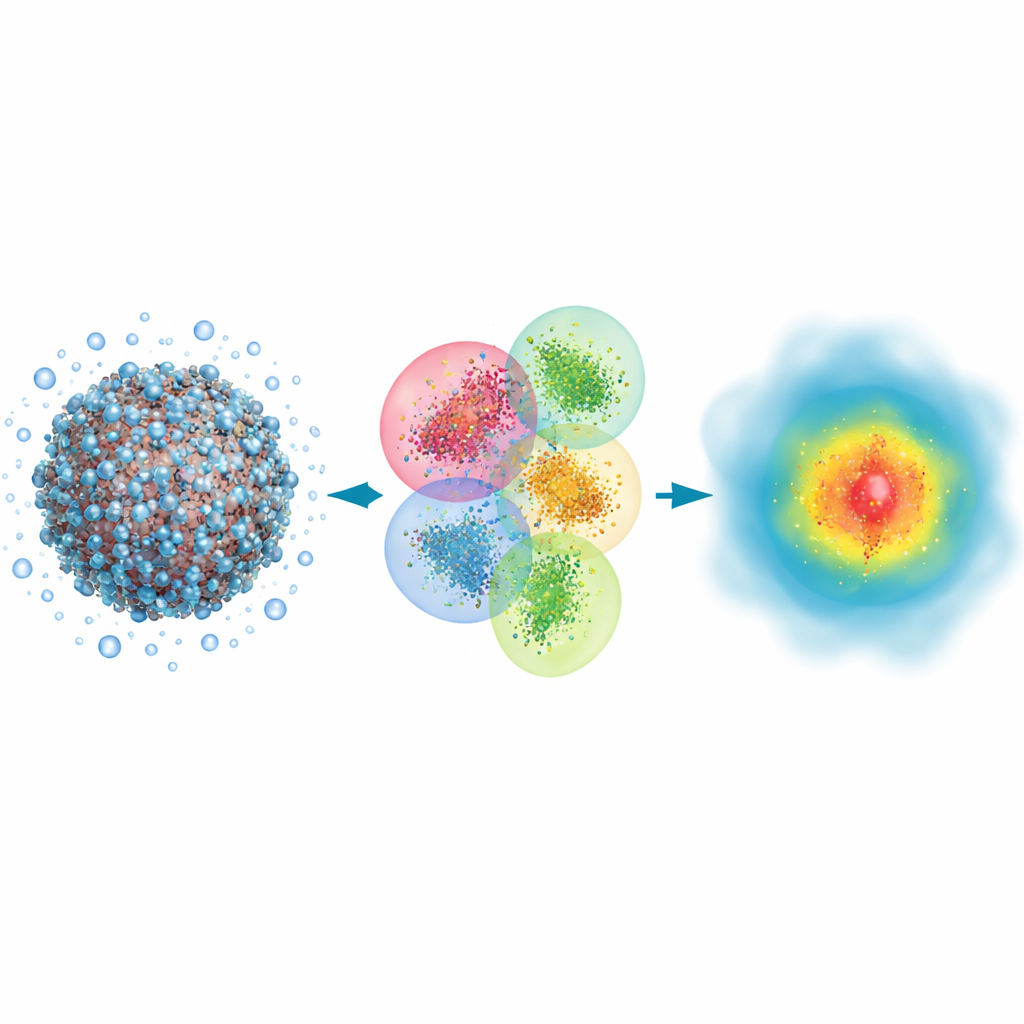
Почему большим молекулам нужны квантовые «глаза»
Многие биологические события — от связывания лекарств до действия света в зрении — включают разрыв и образование химических связей и перераспределение электронных облаков. Классические методы моделирования могут отслеживать общую динамику атомов в больших белках или ДНК, но они лишь косвенно описывают электроны и упускают тонкие эффекты, которые определяют, как поглощается свет или насколько прочно лекарство держится на мишени. Квантово-механические подходы, напротив, явно учитывают электроны и способны предсказывать такие свойства, как оптические спектры, с высокой точностью. Проблема в том, что традиционные квантовые методы стремительно замедляются при росте системы, поэтому их обычно применяли лишь к небольшим фрагментам, оставляя вне досягаемости целые вирусы или крупные сборки белков.
Разбивая задачу на съедобные куски
Авторы опираются на классический квантовый подход — метод Хартри–Фока, который описывает электроны с помощью орбиталей, и перестраивают его в угоду скорости, а не предельной точности. Ключевая идея — разбить огромную биомолекулу с окружающей водой на множество перекрывающихся кластеров. Каждый кластер имеет центральную «ядровую» область, где сохраняются квантовые результаты, и буферную зону, которая имитирует влияние соседних атомов. Квантовые расчёты затем выполняются отдельно для каждого кластера, а куски сшиваются вместе, чтобы восстановить полную электронную плотность системы. Дополнительно используют очень компактное представление орбиталей и отбрасывают слабые дальнодействующие взаимодействия, которые мало влияют на итог — в результате масштабирование затрат примерно пропорционально числу атомов, а не взрывается с ростом системы.
От вирусов до ДНК и противораковых препаратов
Чтобы продемонстрировать возможности этого упрощённого фреймворка, исследователи рассматривают несколько демонстрационных систем. Они вычисляют полную электронную структуру трёх крупных сборок в воде, включая бактериофаг — вирус, инфицирующий бактерии — вместе с окружающим объёмом растворителя в сумме более 45 миллионов атомов и свыше 150 миллионов электронов. На современном кластере такой расчёт завершается примерно за полдня, что, по их сведениям, является крупнейшей когда-либо выполненной симуляцией методом Хартри–Фока. Затем они переходят к поглощению света: используя временное расширение своего метода, они моделируют ультрафиолетово–видимые спектры для фрагментов ДНК длиной до 21 пар нуклеотидов и для противоракового препарата Актиномицин D, как в свободном состоянии, так и в комплексе с ДНК. Предсказанные спектры хорошо согласуются с экспериментальными измерениями, показывая, что схема со сниженной точностью по-прежнему улавливает ключевую физику взаимодействия этих биомолекул с светом.
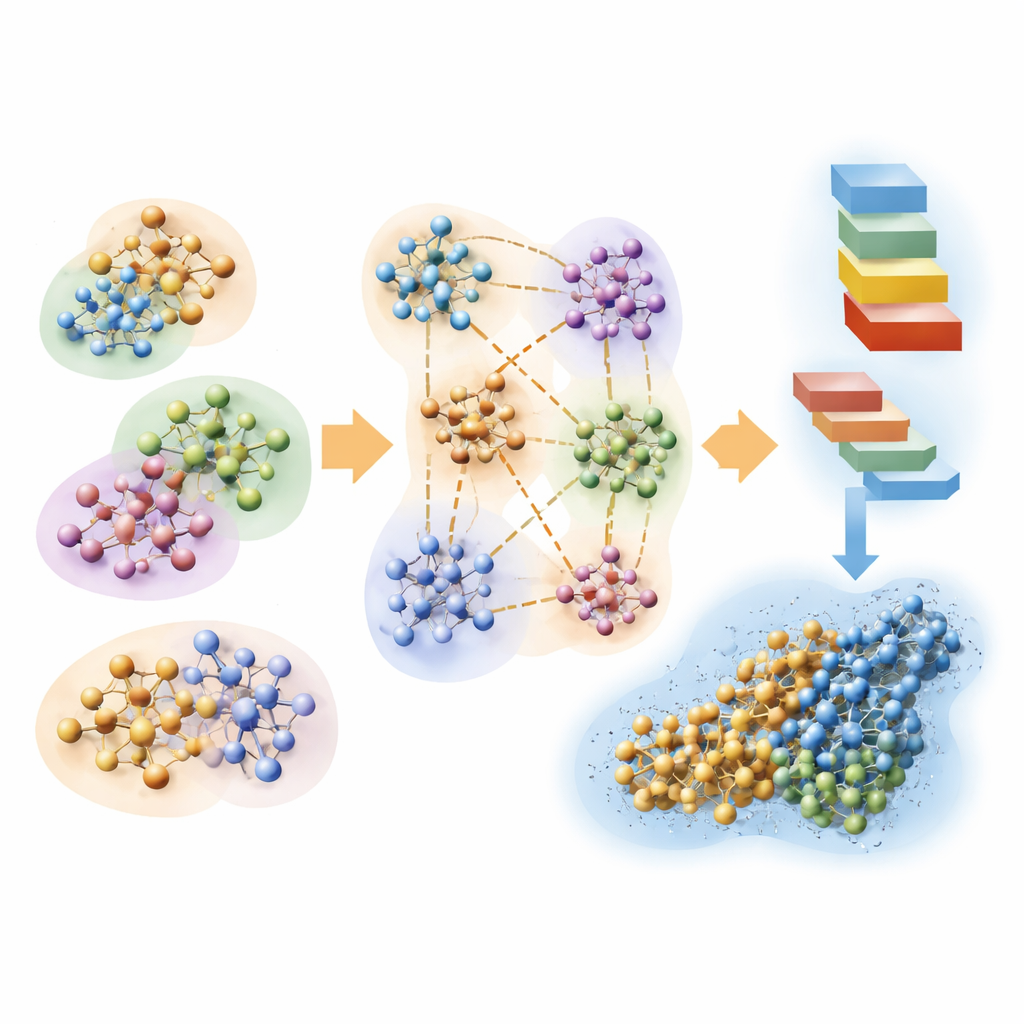
Проверка структур белков, предсказанных ИИ, с помощью физики
Команда также исследует, как быстрые квантовые расчёты могут помочь оценить структуры белков, предсказанные инструментами искусственного интеллекта, такими как AlphaFold. Белки естественным образом сворачиваются в формы, минимизирующие их энергию. Используя линейно масштабируемый подход Хартри–Фока, авторы оценивают локальные атомные энергии вдоль длины нескольких белков, предсказанных AlphaFold, в реалистичных водных средах. Сравнение этих квантово-выведенных энергетических профилей с собственными оценками уверенности AlphaFold показывает поразительное совпадение: низкие энергии совпадают с областями, которые AlphaFold считает надёжными, а высокие энергии указывают на сомнительные или нестабильные сегменты. Это свидетельствует о том, что современные сети предсказания структуры неявно усваивают аспекты лежащего в основе квантового энергетического ландшафта, а расчёты от первых принципов могут служить независимой, физически обоснованной проверкой качества.
Компромиссы, ограничения и новые возможности
Рост скорости достигается осознанными компромиссами. Использование минимального базиса орбиталей и обрезание слабых дальних взаимодействий неизбежно жертвует частью точности, а стратегия «разделяй и властвуй» не идеальна для величин, чувствительных к дальнодействующим эффектам, таких как точные энергии связывания в плотных белок–лигандных комплексах. Авторы показывают, что для таких задач высокой точности пороги приходится ослаблять или убирать, и метод ведёт себя скорее как традиционный, более медленный квантовый код. Тем не менее для очень больших систем, где полностью точная квантовая обработка вообще невозможна, их подход предлагает мощный компромисс: он даёт качественно и часто количественно надёжные выводы при умеренных вычислительных ресурсах, вплоть до одного вычислительного узла для систем примерно до миллиона атомов.
Что это значит для будущего молекулярной науки
Перестроив стандартный квантовый метод в пользу скорости при сохранении хорошего согласия с экспериментом, этот фреймворк открывает дорогу к рутинным квантовомеханическим исследованиям целых вирусов, белковых машин и больших ДНК–лекарственных комплексов. Он обеспечивает детализированные карты электронной плотности, которые можно напрямую сравнивать с современными данными кристаллографии, реалистичные оптические спектры для биомолекул беспрецедентного размера и независимые проверки структур, сгенерированных ИИ. В перспективе те же идеи могут поддержать быстрые квантово-основанные молекулярные динамики, изучение влияния электрических или магнитных полей на биомолекулы и генерацию больших наборов данных с квантовой точностью для обучения следующего поколения моделей машинного обучения. Практически это приближает когда-то далёкую мечту «квантовой биологии» — описывать биологические машины с полной электронной детализацией — к повседневной научной практике.
Цитирование: Wieners, L., Garcia, M.E. A quantum-mechanical framework for million-atom scale biological systems. Commun Chem 9, 170 (2026). https://doi.org/10.1038/s42004-026-02038-y
Ключевые слова: квантовое биомолекулярное моделирование, метод Хартри–Фока, предсказание структуры белков, УФ-Вид спектры, алгоритмы «разделяй и властвуй»