Clear Sky Science · he
מסגרת קוואנטית-מכניקאית למערכות ביולוגיות בקנה מידה של מיליוני אטומים
להציץ בתוך החיים, אלקטרון אחד בכל פעם
חלבונים, DNA ווירוסים תלויים בהתנהגותם בתנועת האלקטרונים, אך סימולציות ברמת הקוואנטום של מולקולות גדולות כאלה היו עד כה איטיות מדי כדי להריץ אותן אלא על המערכות הקטנות ביותר. עבודה זו מציגה דרך להביא מכניקת קוואנטום מלאה למבנים ביולוגיים עצומים—עד עשרות מיליוני אטומים—על ידי הרפיית הדיוק במידה מבוקרת, די כדי שיהיו החישובים מהירים, זולים ומפתיעים כמועילים לשאלות בביו-רפואה ובעיצוב תרופות.
מדוע מולקולות גדולות זקוקות לעיניים קוואנטיות
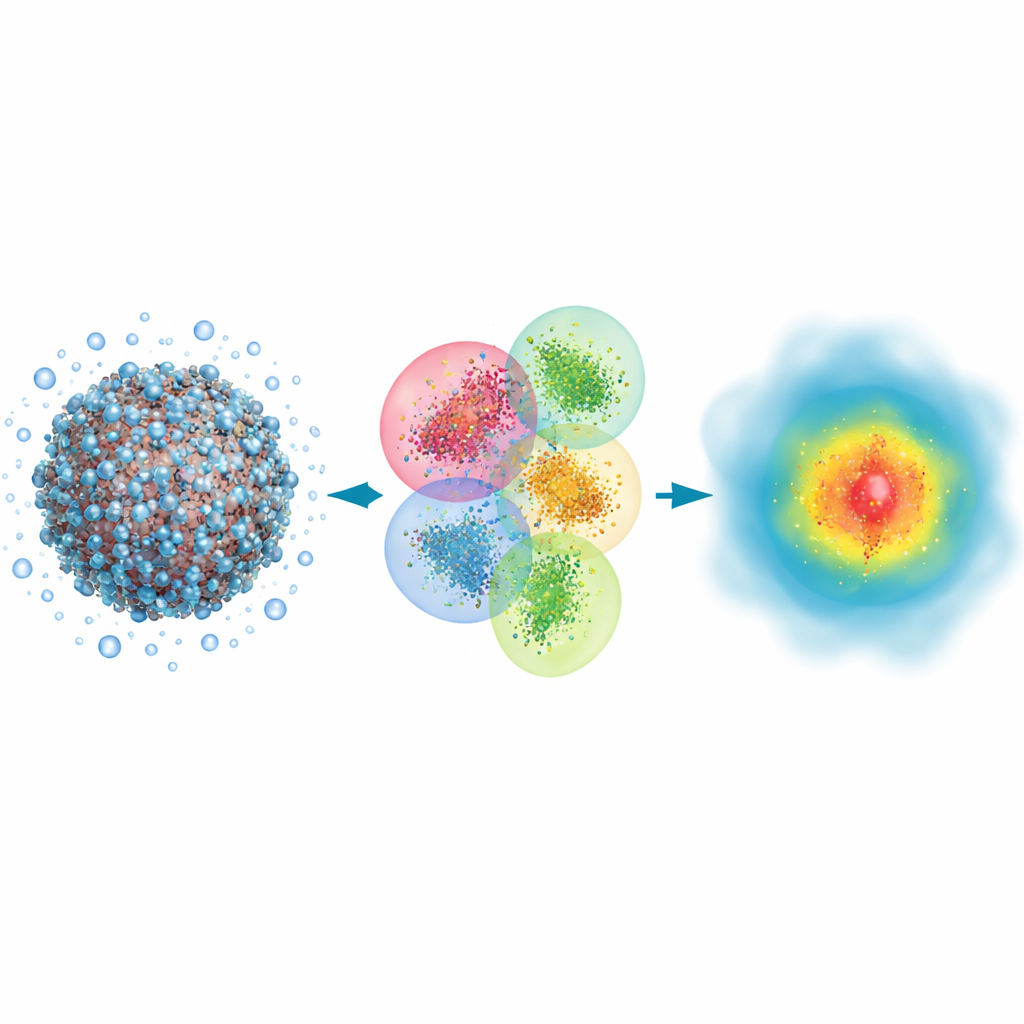
לאירועים ביולוגיים רבים, מהקשירה של תרופה ועד פעולה של אור בראייה, מעורבים שבירת וקישור קשרים כימיים ושינויים בענני האלקטרונים. שיטות סימולציה קלאסיות יכולות לעקוב אחרי התנועה הכוללת של האטומים בחלבונים גדולים או ב-DNA, אך הן מטפלות באלקטרונים באופן עקיף בלבד ומחמיצות כמה מהאפקטים העדינים שקובעים איך אור נספג או כמה חזק תרופה נדבקת למטרתה. בגישה קוואנטית-מכניקאית לעומת זאת, עוקבים במפורש אחרי האלקטרונים וניתן לחזות תכונות כמו ספקטרום אופטי ברמת נאמנות גבוהה. הבעיה היא ששיטות קוואנטיות מסורתיות מאטות קצבאות ככל שמערכת מתרחבת, ולכן בדרך כלל שימשו רק לקטעים קטנים, והשאירו וירוסים שלמים או צברי חלבונים גדולים מחוץ להישג יד.
פירוק הבעיה לחתיכות בגודל נשיכה
המחברים בונים על גישה קלאסית קוואנטית הנקראת הרטי–פוק, שמתארת אלקטרונים באמצעות אורביטלים מתמטיים, ומשנים אותה למען מהירות במקום דיוק מקסימלי. הרעיון המרכזי שלהם הוא לפצל מולקולה ביולוגית ענקית יחד עם סביבת המים שלה למספר רב של אשכולות חופפים. לכל אשכול יש אזור ליבה מרכזי שבו נשמרים התוצאות הקוואנטיות, ואזור חיץ שמדמה את השפעת האטומים השכנים. חישובים קוואנטיים מבוצעים בנפרד על כל אשכול, והחתיכות תופרנה חזרה כדי לשחזר את צפיפות האלקטרונים המלאה של המערכת. על ידי שימוש גם בייצוג קומפקטי מאוד של האורביטלים ובהשלכת אינטראקציות מרוחקות חלשות שתורמות מעט לתוצאה הסופית, השיטה מתדרגת בקירוב ביחס ישר למספר האטומים במקום להתפוצץ בעלות החישוב.
מווירוסים ל-DNA ולתרופות נגד סרטן
כדי להדגים מה המסגרת המצומצמת הזו מסוגלת לעשות, החוקרים מטפלים בכמה מערכות תצוגה. הם מחשבים את המבנה האלקטרוני המלא של שלושה צברים גדולים במים, כולל בקטריופאג׳—וירוס שדוקר חיידקים—יחד עם קופסת ממס סביבתית שמסכמת למעל 45 מיליון אטומים וליותר מ-150 מיליון אלקטרונים. על אשכול מודרני החישוב הזה מסתיים בכח חצי יום, ומהווים, לדעתם, סימולציית הרטי–פוק הגדולה ביותר אי פעם שנערכה. לאחר מכן הם פונים לספיגת אור: באמצעות הרחבה בזמן-תלוי של שיטותיהם הם מדלגים ספקטרום UV-Vis לקטעי DNA עד 21 זוגות בסיס ולתרופה נגד סרטן Actinomycin D, הן חופשיות והן קשורות ל-DNA. הספקטרות החזויות תואמות בקירוב רב למדידות ניסיוניות, מה שמראה שהסכימה של ירידה בדיוק עדיין תופסת את הפיזיקה החיונית של האינטראקציה בין ביומולקולות לאור.
בדיקת צורות חלבון שחזו בינה מלאכותית בעזרת פיזיקה
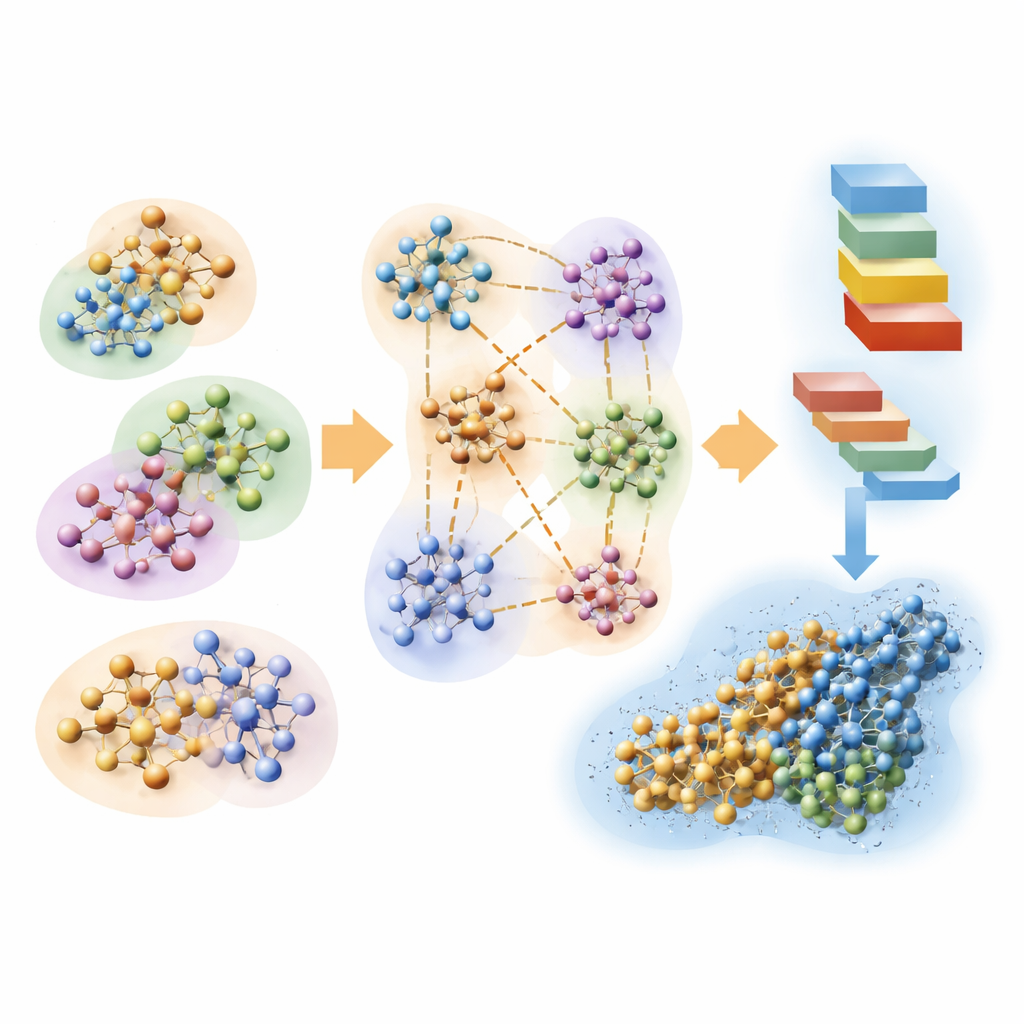
הצוות גם חוקר עד כמה חישובים קוואנטיים מהירים יכולים לסייע בהערכת מבני חלבון שחזו כלים של בינה מלאכותית כמו AlphaFold. חלבונים מתקפלים באופן טבעי לצורות שממזערות את האנרגיה שלהם. באמצעות גישת הרטי–פוק בקנה מדרג ליניארי, המחברים מעריכים אנרגיות אטומיות מקומיות לאורך אורך כמה חלבונים שחזתה AlphaFold, בסביבות מים ריאליסטיות. כאשר דפוסי האנרגיה הנגזרים מקוואנטום מושווים עם ציוני הביטחון של AlphaFold, הם מתיישבים באופן בולט: אנרגיות נמוכות חופפות לאזורים ש-AlphaFold רואה כאמינים, בעוד אנרגיות גבוהות מסמנות מקטעים לא בטוחים או לא יציבים. הממצא מרמז שרשתות חיזוי המבנה המודרניות לומדות באופן מרומז היבטים של נוף האנרגיה הקוואנטי הבסיסי, ושחישובים מעקרונות ראשונים יכולים לספק בדיקת איכות עצמאית מבוססת פיזיקה.
פשרות, מגבלות ואפשרויות חדשות
השיפורים בקצב נובעים מהפשרות מכוונות. שימוש בבסיס אורביטלי מינימלי וחתך אינטראקציות מרוחקות חלשות בהכרח מוותרים על חלק מהדיוק, ואסטרטגיית החלוקה והכיבוש אינה אידיאלית לכמויות התלויות ברגישות באפקטים טווח-ארוך, כגון אנרגיות קשירה מדויקות במורכבי חלבון–ליגנד צמודים. המחברים מראים שעבור משימות הדורשות דיוק גבוה יש להרפות או להסיר את החתכים, והשיטה מתנהגת יותר כמו קוד קוואנטי קונבנציונלי ואיטי. ومع זאת, עבור מערכות גדולות מאוד שבהן אין טיפול קוואנטי מדויק כלל וריאלי, הגישה שלהם מציעה אמצע חזק: היא מספקת תובנות איכותניות ולעתים כמותיות אמינות עם משאבי חישוב צנועים, אפילו בצמתים בודדים עבור מערכות עד בקירוב מיליון אטומים.
מה המשמעות הזו לעתיד מדעי המולקולות
על ידי הנדסה מחודשת של שיטת קוואנטום סטנדרטית לטובת מהירות תוך שמירה על התאמה טובה לניסויים, המסגרת הזו פותחת דלת למחקרים שגרתיים ברמת הקוואנטום של וירוסים שלמים, מכונות חלבון ומורכבי DNA–תרופה גדולים. היא מאפשרת מיפויי צפיפות אלקטרונית מפורטים שניתן להשוות ישירות לקריסטלוגרפיה מתקדמת, ספקטרות אופטיות ריאליסטיות לביומולקולות בגדלים חסרי תקדים ובדיקות עצמאיות למבני חלבון שנוצרו על ידי בינה מלאכותית. בהסתכלות קדימה, אותן רעיונות יכולים לתמוך בדינמיקה מולקולרית מהירה מבוססת קוואנטום, במחקרים על כיצד שדות חשמליים או מגנטיים משפיעים על ביומולקולות, וביצירת מערכי נתונים גדולים מדויקים קוואנטית לאימון דגמי למידה מכונה דור הבא. במונחים מעשיים, זה מקרב את החלום הרחוק של "ביולוגיה קוואנטית"—לטפל במכונות החיים עם פירוט אלקטרוני מלא—אל שגרה מדעית יומיומית.
ציטוט: Wieners, L., Garcia, M.E. A quantum-mechanical framework for million-atom scale biological systems. Commun Chem 9, 170 (2026). https://doi.org/10.1038/s42004-026-02038-y
מילות מפתח: סימולציה קוונטית של מולקולות ביולוגיות, הרטי–פוק, חיזוי מבנה חלבון, ספקטרום UV-Vis, אלגוריתמים של חלוקה וכיבוש