Clear Sky Science · ja
百万原子規模の生体システムのための量子力学的フレームワーク
一度に一つの電子で生命の内部を覗く
タンパク質、DNA、ウイルスはいずれも電子の絶え間ない運動に振る舞いを依存していますが、真に量子レベルのシミュレーションはこれまで巨大分子に対しては遅すぎて、せいぜい小さな系でしか実行できませんでした。本研究は、精度を僅かに緩和することで計算を高速化・低コスト化し、生物学、医学、医薬品設計の問いに対して驚くほど有用な形で、数百万〜数千万原子に及ぶ巨大な生体構造に完全な量子力学を適用する方法を提示します。
なぜ大きな分子に量子的な視点が必要か
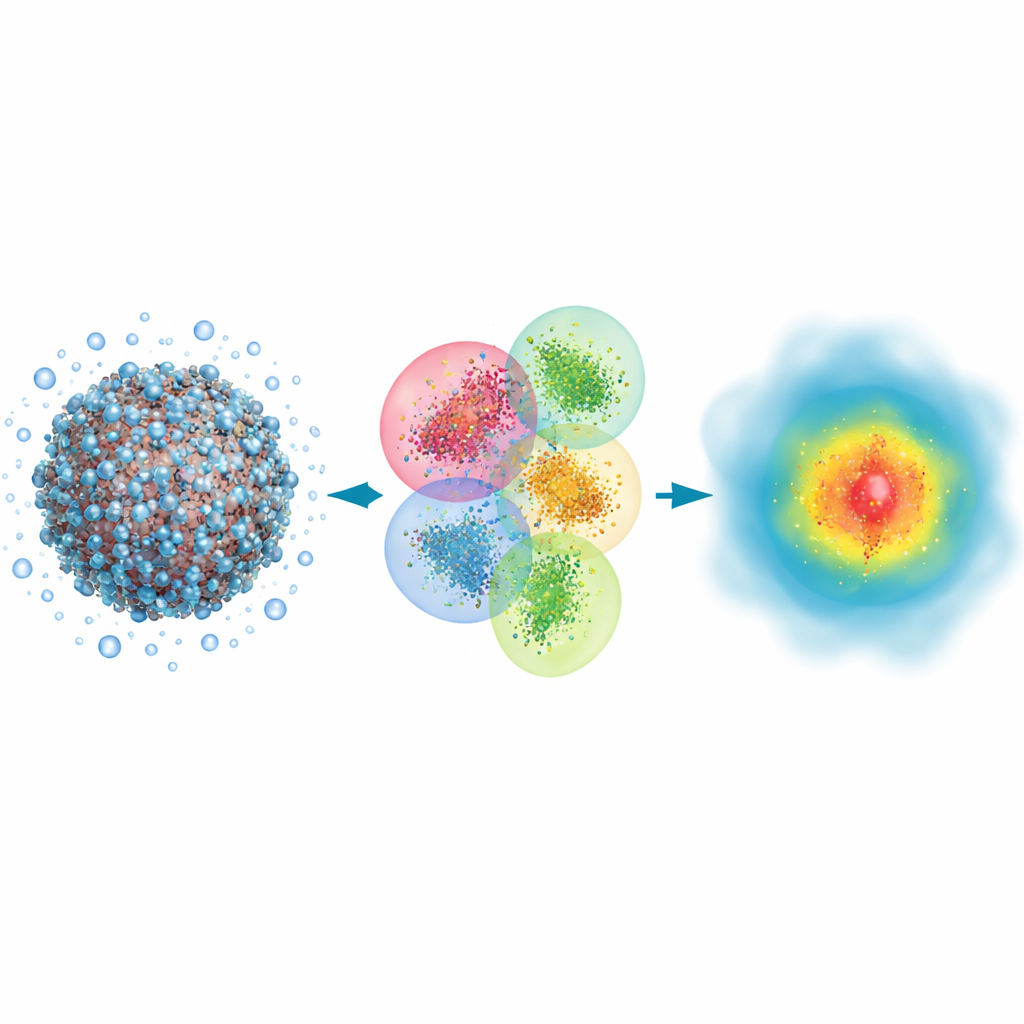
薬物結合から光が視覚に作用する過程に至るまで、多くの生物学的現象は化学結合の切断・形成や電子雲の移動を伴います。古典的なシミュレーション手法は大きなタンパク質やDNAの原子運動を追えますが、電子を間接的にしか扱えないため、光の吸収や薬物が標的にどれほど強く結合するかといった微妙な効果を見落とします。一方、量子力学的手法は電子を明示的に追跡し、光学スペクトルのような性質を高い忠実度で予測できます。問題は従来の量子手法が系の大きさとともに計算時間が爆発的に増大することで、通常は小さな断片にしか適用できず、ウイルス全体や巨大なタンパク質集合体は手の届かないままでした。
問題を咬み切れる大きさに分割する
著者らはハートリー・フォックと呼ばれる古典的な量子手法を土台に、最終的な精度よりも速度を優先する形で再設計しています。彼らの要点は、巨大な生体分子と周囲の水を多くの重なり合うクラスタに分割することです。各クラスタは量子結果を維持する中心のコア領域と、隣接原子の影響を模擬するバッファ領域を持ちます。各クラスタで量子計算を別個に行い、それらをつなぎ合わせて系全体の電子密度を再構築します。さらに軌道を非常にコンパクトに表現し、最終結果への寄与が小さい弱い長距離相互作用を切り捨てることで、計算コストは爆発的に増加するのではなく原子数に概ね比例してスケールします。
ウイルスからDNA、がん薬まで
この合理化されたフレームワークの能力を示すために、研究者たちはいくつかの代表的な系に取り組みます。彼らは水中での三つの大きな集合体の完全な電子構造を計算し、その中には細菌に感染するバクテリオファージ(ウイルス)と、溶媒ボックスを合わせて4,500万原子超、1億5,000万電子以上に達するものが含まれます。現代のクラスタではこの計算は約半日で終わり、著者らの知る限り最大規模のハートリー・フォック計算となります。続いて光吸収に着目し、時間依存拡張を用いて最大21塩基対のDNA断片や抗がん剤アクチノマイシンD(自由状態およびDNA結合状態)の紫外可視スペクトルをシミュレートします。予測されたスペクトルは実験値とよく一致し、精度を落としたスキームでもこれらの生体分子が光とどのように相互作用するかの本質的な物理を捉えていることが示されます。
AIが予測したタンパク質形状を物理で検証する
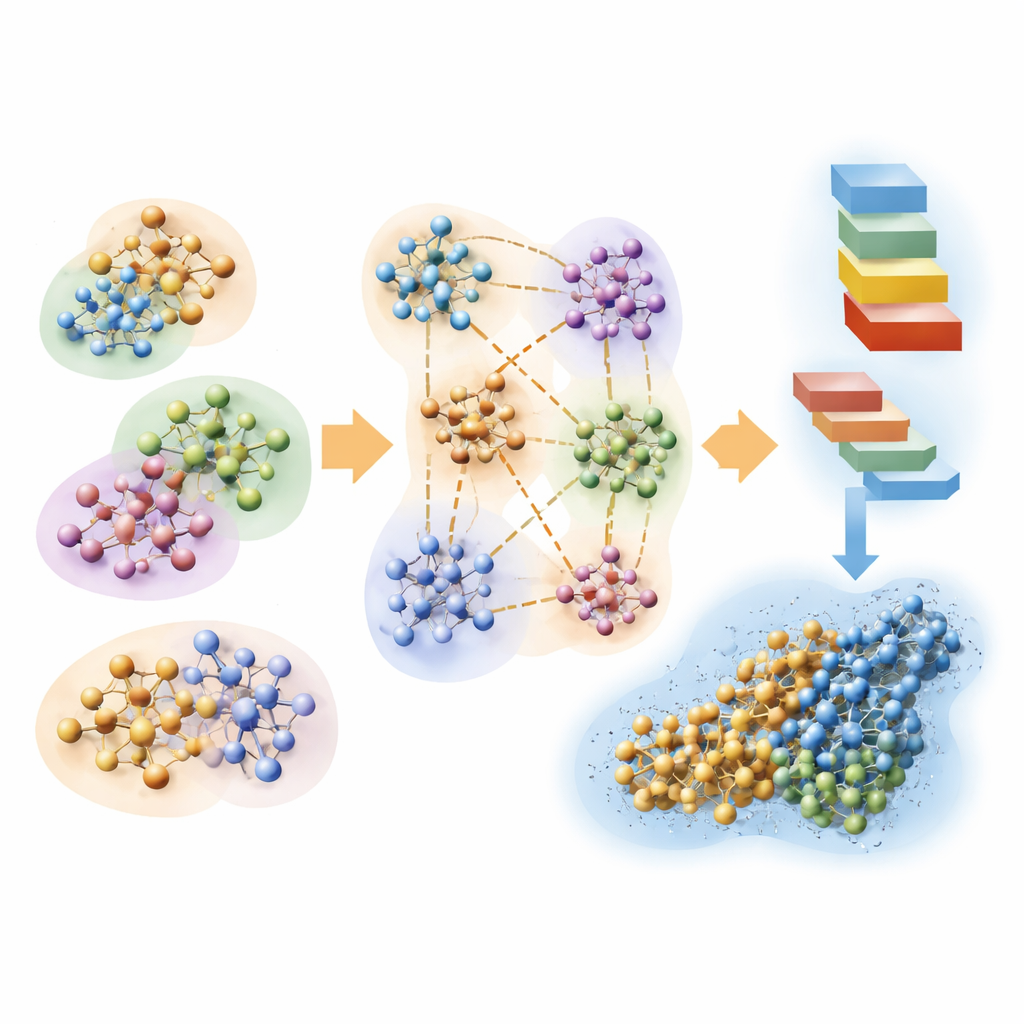
チームはまた、量子計算の高速化がAlphaFoldのような人工知能ツールによるタンパク質構造予測の評価にどう役立つかを調べます。タンパク質は自然にエネルギーを最小化する形に折り畳まれます。線形スケーリングのハートリー・フォック手法を用いて、著者らは現実的な水環境下で複数のAlphaFold予測タンパク質に沿った局所原子エネルギーを推定しました。これらの量子由来のエネルギーパターンをAlphaFold自身の信頼度スコアと比較すると、驚くほど良く一致します。低エネルギー領域はAlphaFoldが信頼できるとする部分と一致し、高エネルギー領域は不確かまたは不安定な区間を示します。これは現代の構造予測ネットワークが暗黙のうちに基礎となる量子エネルギー地形の側面を学んでおり、第一原理計算が独立した物理に基づく品質チェックを提供できることを示唆します。
トレードオフ、限界、そして新たな可能性
速度向上は意図的な妥協から生まれます。最小限の軌道基底を使い、弱く遠い相互作用を切ることは必然的に精度の一部を犠牲にしますし、分割統治戦略は厳密な結合エネルギーのような長距離効果に微妙に依存する量には最適ではありません。著者らは、そうした高精度が求められる課題ではカットオフを緩めるか取り除く必要があり、手法は従来の遅い量子コードに近い振る舞いをすることを示しています。それでも、完全に正確な量子処理がまったく実現不可能な非常に大きな系に対しては、このアプローチは強力な中間解を提供します。質的かつ多くの場合定量的に信頼できる洞察を控えめな計算資源で与え、単一の計算ノードで約百万原子程度まで扱える場合もあります。
分子科学の未来にとっての意味
標準的な量子手法を速度優先に再設計しつつ実験と良く整合させることで、このフレームワークはウイルス全体、分子機械的タンパク質、大規模なDNA–薬物複合体の常例的な量子レベル研究への扉を開きます。最先端の結晶構造解析と直接比較可能な詳細な電子密度マップ、前例のないサイズの生体分子に対する現実的な光学スペクトル、AI生成タンパク質構造の独立した検証を可能にします。将来に向けては、同じ発想が高速な量子ベースの分子動力学、電場や磁場が生体分子に与える影響の研究、次世代機械学習モデルを訓練するための大規模な量子正確データセットの生成を支える可能性があります。実践的に言えば、生命の機構を電子の詳細まで扱うというかつて遠い夢であった「量子生物学」を日常的な科学実践に近づけるものです。
引用: Wieners, L., Garcia, M.E. A quantum-mechanical framework for million-atom scale biological systems. Commun Chem 9, 170 (2026). https://doi.org/10.1038/s42004-026-02038-y
キーワード: 量子生体分子シミュレーション, ハートリー・フォック, タンパク質構造予測, 紫外可視スペクトル, 分割統治アルゴリズム