Clear Sky Science · tr
Epigenetik belleğin stokastik modellenmesi
Hücreler Kim Olduklarını Nasıl Hatırlıyor
Vücudunuzdaki her hücre temelde aynı DNA’yı taşır, ama bir beyin hücresi deri ya da bağışıklık hücresinden çok farklı davranır. Bu kalıcı “kimlik hissi” hücreler her bölündüğünde kopyalanmalı; başarısız olduğunda kanser gibi hastalıklar ortaya çıkabilir. Bu makale, araştırmacıların epigenetik belleği—belirli genlerin uzun vadede açık mı kapalı mı kalması gerektiğini hücrelerin hatırlamasını sağlayan DNA ve onun paketlenmesine ait biyokimyasal işaretleri—anlamak için matematiksel araçları nasıl kullandığını açıklar.
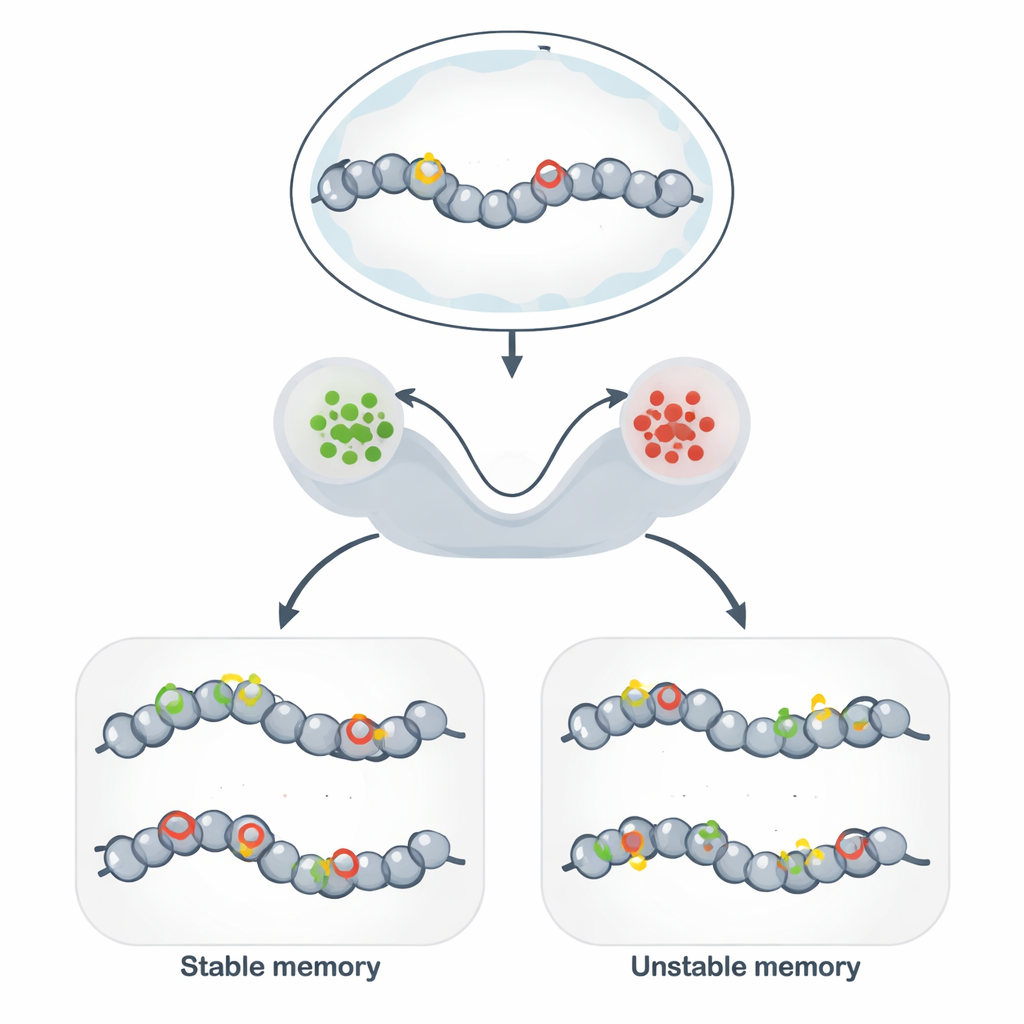
DNA’nın Ötesinde: Genom Üzerinde Kalıcı İşaretler
Epigenetik bellek, genetik olarak özdeş hücrelerin çok sayıda hücre bölünmesi boyunca farklı ve kararlı davranışları sürdürmesine olanak tanır. DNA dizisini değiştirmek yerine hücreler DNA’yı ve çevresindeki proteinleri yerel yapıyı gevşeten veya sıkılaştıran kimyasal etiketlerle süsler. Etiketler açık bir yapı lehine olduğunda yakınlardaki genler genellikle aktiftir; kompakt yapı lehine olduğunda genler susturulur. Bu mekanizma hücre tipi kimliğinin, bağışıklık yanıtlarının devamlılığının, bazı beyin hafızası biçimlerinin ve kararlı hücre durumlarını “programlamayı” amaçlayan sentetik biyoloji araçlarının temelini oluşturur.
Rastgelelik Neden Gözardı Edilemez
Moleküler ölçekte hücre gürültülü bir ortamdır: anahtar moleküller genellikle az sayıda bulunur ve rastgele çarpışırlar. Gen aktivitesinin zaman içindeki değişimini düz eğrilerle tanımlayan geleneksel modeller iki vadili, tepeyle ayrılmış bir peyzaja benzer birden fazla kararlı durum öngörebilir. Bu tür modellerde sistem bir vadiye yuvarlandığında orada sonsuza kadar kalması beklenir. Ama gerçekte rastgele moleküler olaylar ara sıra sistemi tepenin üzerinden diğer bir vadiye atlayacak şekilde itebilir. Makale, reaksiyonları rastgele olaylar olarak ele alan ve bu tür geçişlerin ne sıklıkla gerçekleştiğini nicelleştiren stokastik (olasılıksal) çerçeveleri tanıtır; örneğin bir durumun gürültünün sıçramaya neden olmasıyla tipik olarak ne kadar sürdüğünü ölçen ortalama ilk geçiş süreleri gibi.
Moleküler Kaosa Matematiksel Mercekler
Derleme bu rastgeleliği modellemenin iki temel yolunu açıklar. Stokastik kimyasal reaksiyon ağları kesin molekül sayılarını izler ve sistemi mevcut duruma bağlı olasılıkla her reaksiyonun tetiklendiği bir Markov süreci olarak ele alır. Bu yaklaşım kararlı gen ifade durumları arasındaki nadir geçişleri sadakatle yakalayabilir ancak hesaplama açısından ağırdır. İkinci model sınıfı stokastik diferansiyel denklemler kullanır; bunlar molekül sayılarını sürekli büyüklükler olarak ve Gauss türü gürültüyle sallanan değerler şeklinde yaklaşıklar. Kimyasal Langevin denklemi ve lineer gürültü yaklaşımı gibi varyantlar bazı doğruluk kayıpları karşılığında analitik açıklık sunar; araştırmacıların sistem parametrelerinin kararlı bir durum çevresindeki dalgalanmaları nasıl şekillendirdiğini ve durumlar arasındaki geçişlerin olasılığını türetmesine olanak verir.
Kromatin Devreleri Olarak Bellek Donanımı
Bu soyut modelleri biyolojiye bağlamak için yazarlar histon proteinleri ve DNA üzerindeki kimyasal işaretlerin birbirini güçlendirdiği kromatin modifikasyon devrelerine odaklanır. Aktif kromatini teşvik eden ve baskılayıcı kromatini teşvik eden histon etiketleri, aynı etiketi komşu bölgelere yayan enzimleri çekebilir ve güçlü pozitif geri besleme oluşturabilir. Stokastik modeller, bu kendini güçlendirmenin silinmeye göre hızlı olduğu durumlarda sistemin geniş anlamda “AÇIK” ve “KAPALI” olarak iki uzun ömürlü durum geliştirdiğini—ikili bellek gibi davrandığını gösterir. DNA replikasyonu sırasında kopyalanan ve son derece kararlı bir etiket olan DNA metilasyonunun eklenmesi, sistemi uzun süreli baskılanma yönünde daha da kaydırır ve susturulmuş bir durumun sürme süresini dramatik şekilde uzatabilir.
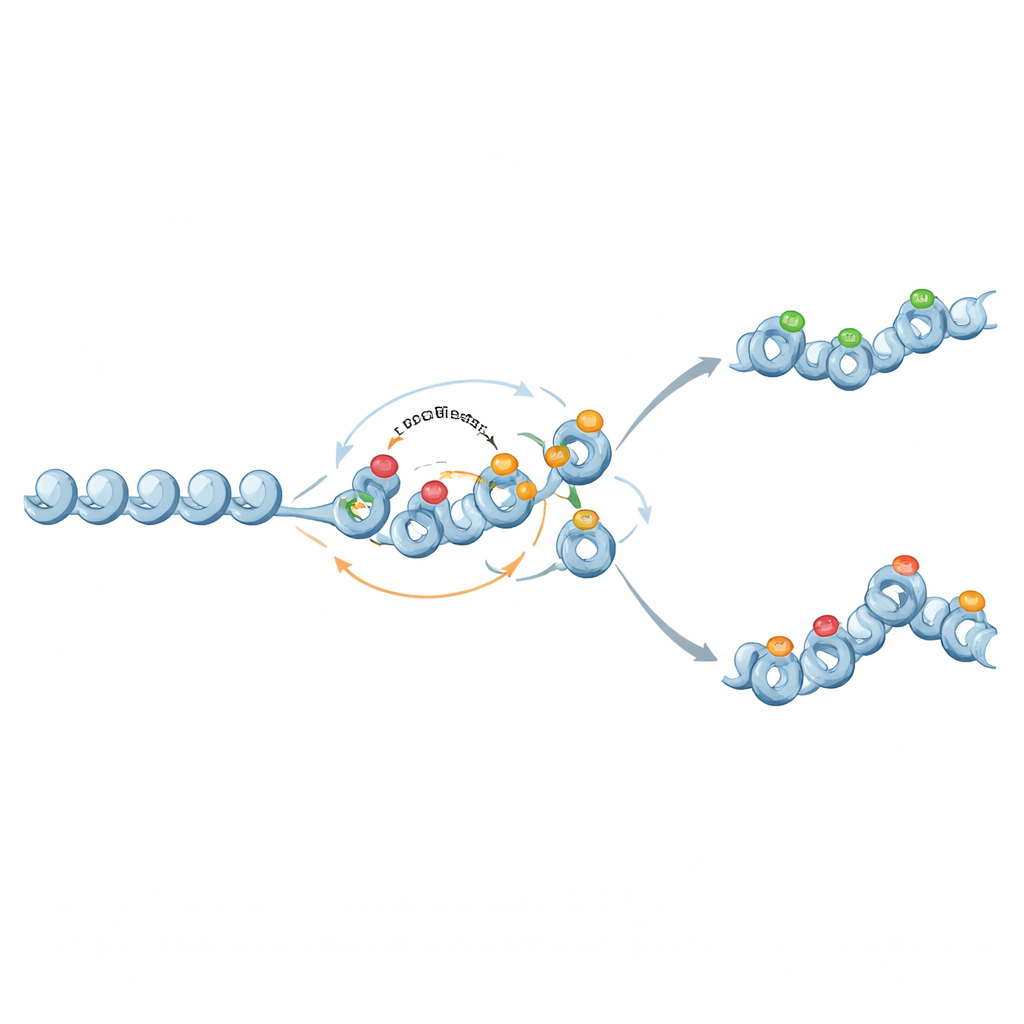
İkili Anahtarlardan Ölçekli Belleklere
İlginç şekilde aynı moleküler bileşenler daha nüanslı, analog belleği de destekleyebilir. Baskılayıcı histon işaretlerinden DNA metilasyonuna olan geri besleme zayıfladığında ve metilasyon neredeyse kalıcı fakat kendini güçlendirmeyen bir hale geldiğinde, metilasyon ortalama gen ifade düzeyini belirleyen sabit bir zemin görevi görür. Histon işaretleri bu zemin üzerinde dalgalanır; bazen iki kararlı kromatin durumu ve ara metilasyon seviyelerinde geniş ifade dağılımları ortaya çıkar. Bu şekilde kromatin devreleri hem bir genin aktivitesinin ne kadar kararlı olduğunu hem de hücreler arasında ifadenin ne kadar değişken olabileceğini ayarlayabilir.
Bu Modeller Tıpta ve Tasarımda Neden Önemli
Yazarlar epigenetik belleği anlamanın moleküler gürültüyü ve temel süreçlerin zamanlamasını açıkça modellemeyi gerektirdiği sonucuna varır. Sentezleri, hücrelerin aktif veya baskılanmış durumlarda kalma süresini en güçlü şekilde kontrol eden reaksiyon hızlarını ve geri besleme döngülerini vurgular. Bu içgörü, hücre döngüsü hızını, enzim düzeylerini veya belirli kromatin işaretlerini değiştirerek model öngörülerini test eden deneyleri yönlendirebilir. Uzun vadede bu tür modeller, güvenilir şekilde yeniden programlanabilen, istenen bir kaderi koruyan veya kontrollü biçimde bilgi depolayan hücreler tasarlamaya yardımcı olabilir—rejeneratif tıp, kanser terapisi ve programlanabilir bağışıklık yanıtları için yeni olasılıkların kapısını açar.
Atıf: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Anahtar kelimeler: epigenetik bellek, kromatin modifikasyonları, DNA metilasyonu, stokastik modelleme, gen düzenlemesi