Clear Sky Science · nl
Stochastische modellering van epigenetisch geheugen
Hoe cellen onthouden wie ze zijn
Elke cel in uw lichaam draagt in wezen hetzelfde DNA, toch gedraagt een zenuwcel zich heel anders dan een huid- of immuuncel. Dit blijvende “gevoel van identiteit” moet bij elke celdeling worden gekopieerd, en als dat faalt kunnen ziekten zoals kanker ontstaan. Dit artikel legt uit hoe onderzoekers wiskundige hulpmiddelen gebruiken om epigenetisch geheugen te begrijpen — de biochemische markeringen op DNA en zijn verpakking die cellen in staat stellen op lange termijn te onthouden of bepaalde genen aan of uit moeten blijven.
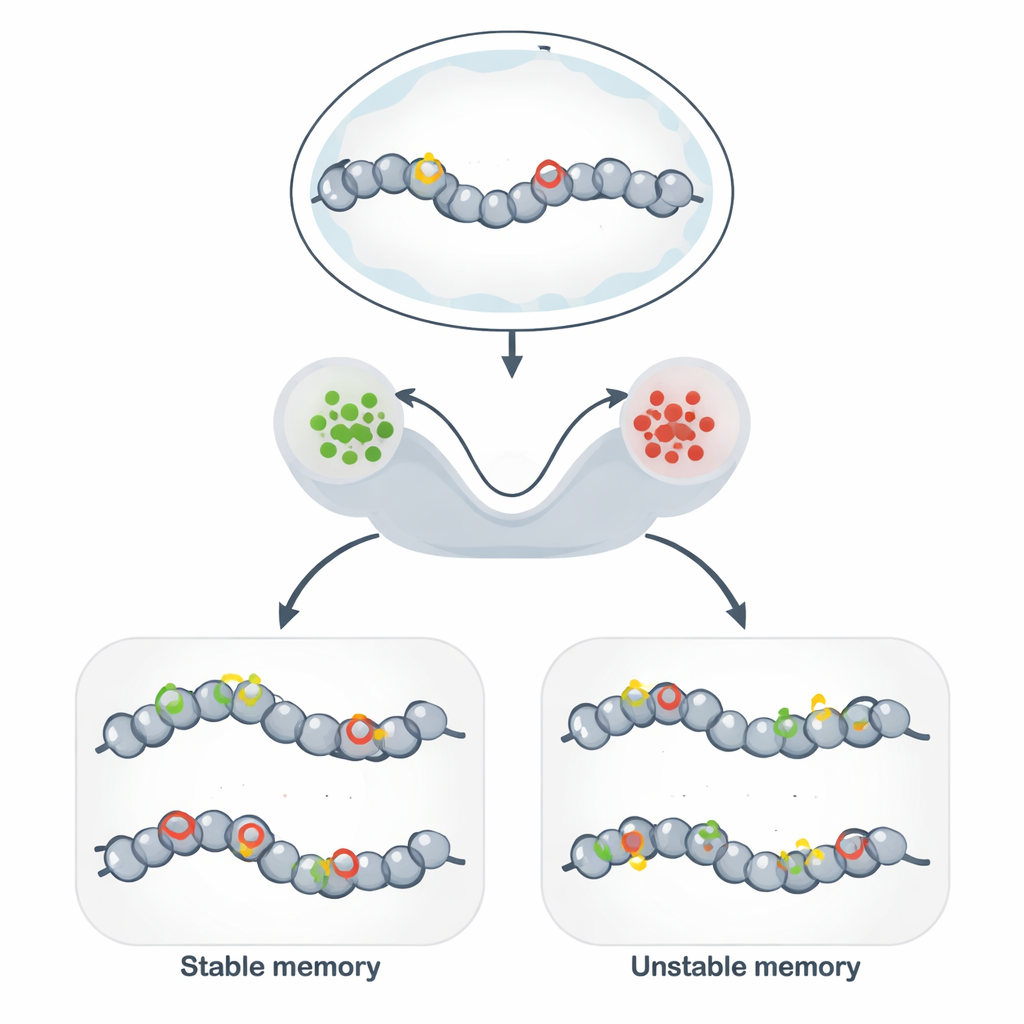
Voorbij DNA: stabiele markeringen op het genoom
Epigenetisch geheugen stelt genetisch identieke cellen in staat verschillende, stabiele gedragingen te behouden over vele celdelingen. In plaats van de DNA-volgorde te veranderen, voorzien cellen DNA en de omliggende eiwitten van chemische labels die de lokale structuur losser of strakker maken. Wanneer labels een open structuur bevorderen, zijn nabijgelegen genen vaak actief; wanneer ze een compacte structuur bevorderen, worden genen stilgelegd. Dit mechanisme ligt ten grondslag aan celtype-identiteit, het aanhouden van immuunresponsen, sommige vormen van hersenherinnering en veelbelovende instrumenten voor synthetische biologie die erop gericht zijn stabiele celtoestanden te ‘programmeren’.
Waarom willekeur niet genegeerd kan worden
Op moleculair niveau is de cel een lawaaierige omgeving: sleutelmoleculen komen vaak in kleine aantallen voor en botsen willekeurig op elkaar. Traditionele modellen die vloeiende krommen gebruiken om te beschrijven hoe genactiviteit in de tijd verandert, kunnen meerdere stabiele toestanden voorspellen, zoals twee valleien gescheiden door een heuvel. In zulke modellen zou, zodra het systeem in een vallei rolt, het daar voor altijd moeten blijven. Maar in werkelijkheid kunnen toevallige moleculaire gebeurtenissen het systeem soms over de heuvel duwen naar een andere vallei. Het artikel introduceert stochastische (waarschijnlijkheids-)kaders die reacties als willekeurige gebeurtenissen behandelen en kwantificeren hoe vaak zulke overschakelingen voorkomen, bijvoorbeeld via gemiddelde eerst-passage-tijden die meten hoe lang een toestand doorgaans duurt voordat ruis een sprong veroorzaakt.
Wiskundige lenzen op moleculaire chaos
De recensie beschrijft twee hoofdmanieren om deze willekeur te modelleren. Stochastische chemische reactienetwerken volgen exacte molecuultellingen en behandelen het systeem als een Markov-proces, waarbij elke reactie afgaat met een waarschijnlijkheid die afhangt van de huidige toestand. Deze benadering kan zeldzame overschakelingen tussen stabiele genexpressietoestanden getrouw vastleggen maar is computationeel zwaar. Een tweede klasse modellen gebruikt stochastische differentiaalvergelijkingen, die molecuultellingen benaderen als continue grootheden die worden geschud door Gaussiaanse ruis. Varianten zoals de chemische Langevin-vergelijking en de lineaire ruisbenadering ruilen wat nauwkeurigheid in voor analytische duidelijkheid, waardoor onderzoekers kunnen afleiden hoe systeemeigenschappen fluctuaties rond een stabiele toestand vormen en hoe waarschijnlijk overgangen tussen toestanden worden.
Chromatine-circuits als geheugenhardware
Om deze abstracte modellen aan biologie te koppelen richten de auteurs zich op chromatine-modificatiecircuits: netwerken van chemische markeringen op histoneiwitten en DNA die elkaar versterken. Histonlabels die actief chromatine bevorderen en labels die gerepresveerd chromatine bevorderen, kunnen elk enzymen aantrekken die hetzelfde label naar naburige locaties verspreiden, waardoor krachtige positieve feedback ontstaat. Stochastische modellen tonen aan dat wanneer deze zelfversterking snel is vergeleken met het wissen, het systeem twee langlevende toestanden ontwikkelt — globaal “AAN” en “UIT” — die als binair geheugen functioneren. Het toevoegen van DNA-methylatie, een zeer stabiel label dat tijdens DNA-replicatie wordt gekopieerd, bevoordeelt het systeem verder richting langdurige repressie en kan dramatisch verlengen hoe lang een onderdrukte toestand aanhoudt.
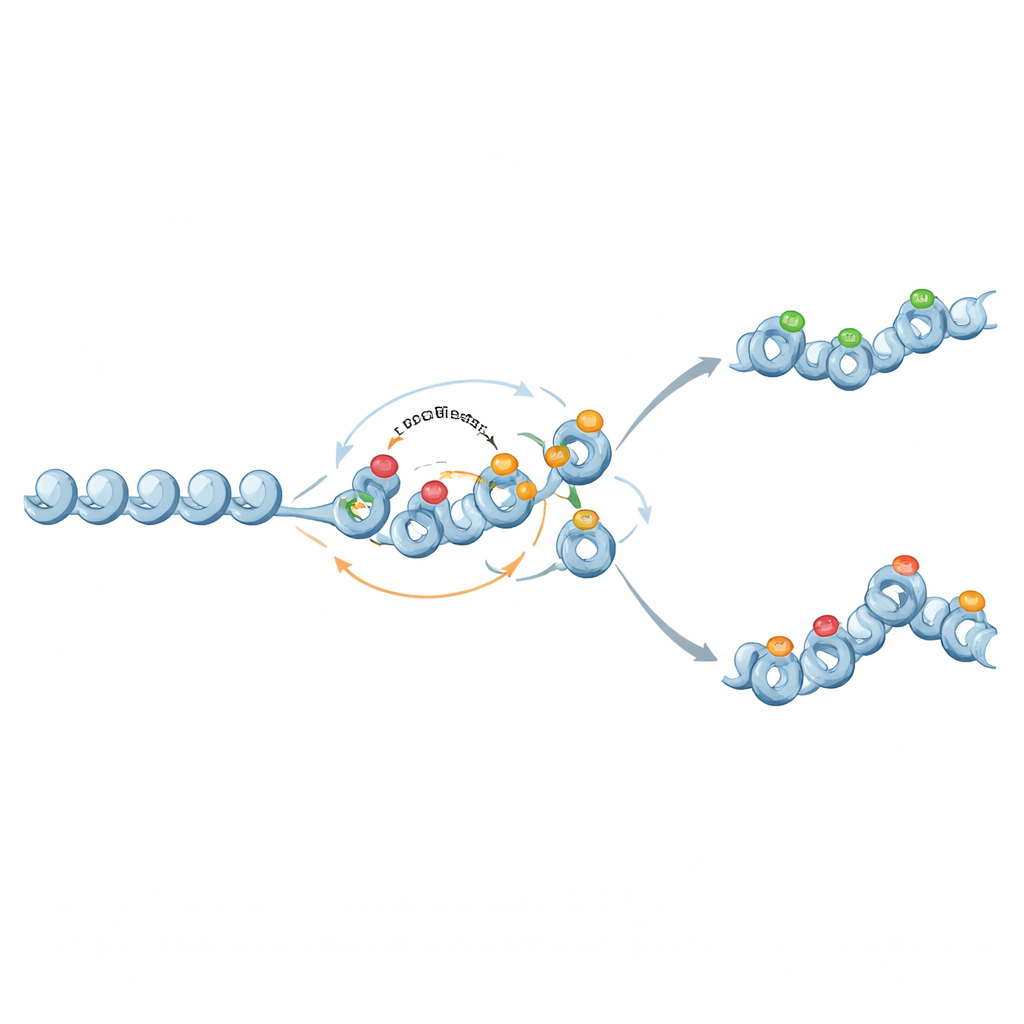
Van binaire schakelaars naar genuanceerd geheugen
Interessant is dat dezelfde moleculaire spelers ook meer genuanceerd, analoog geheugen kunnen ondersteunen. Wanneer feedback van repressieve histonmerken naar DNA-methylatie verzwakt is en methylatie bijna permanent maar niet zelfversterkend wordt, fungeert methylatie als een vast decor dat een gemiddeld genexpressieniveau bepaalt. Histonmerken fluctueren dan bovenop dit decor en kunnen soms twee stabiele chromatine-toestanden en brede expressieverdelingen bij tussenliggende methylatieniveaus produceren. Op deze manier kunnen chromatine-circuits zowel afstemmen hoe stabiel de activiteit van een gen is als hoe variabel de expressie ervan tussen cellen kan zijn.
Waarom deze modellen belangrijk zijn voor geneeskunde en ontwerp
De auteurs concluderen dat het begrijpen van epigenetisch geheugen expliciet modelleren van moleculaire ruis en de timing van sleutelprocessen vereist. Hun synthese belicht welke reactiesnelheden en feedbacklussen het meest bepalend zijn voor de verblijftijd van cellen in actieve of gereprimeerde toestanden. Dit inzicht kan experimenten sturen die de snelheid van de celcyclus, enzymniveaus of specifieke chromatine-markeringen veranderen om modelvoorspellingen te testen. Op lange termijn kunnen dergelijke modellen helpen cellen te ontwerpen die betrouwbaar gereprogrammeerd kunnen worden, een gewenste bestemming behouden of informatie op een beheersbare manier opslaan — wat mogelijkheden opent voor regeneratieve geneeskunde, kankertherapie en programmeerbare immuunresponsen.
Bronvermelding: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Trefwoorden: epigenetisch geheugen, chromatine-modificaties, DNA-methylatie, stochastische modellering, genregulatie