Clear Sky Science · sv
Stokastisk modellering av epigenetiskt minne
Hur celler minns vilka de är
Varje cell i din kropp bär i huvudsak på samma DNA, ändå uppträder en cell i hjärnan mycket annorlunda än en hud- eller immuncell. Denna bestående ”känsla av identitet” måste kopieras varje gång celler delar sig, och när den brister kan sjukdomar som cancer uppstå. Denna artikel förklarar hur forskare använder matematiska verktyg för att förstå epigenetiskt minne — de biokemiska markeringarna på DNA och dess förpackning som gör att celler långsiktigt kommer ihåg om specifika gener ska vara på eller av.
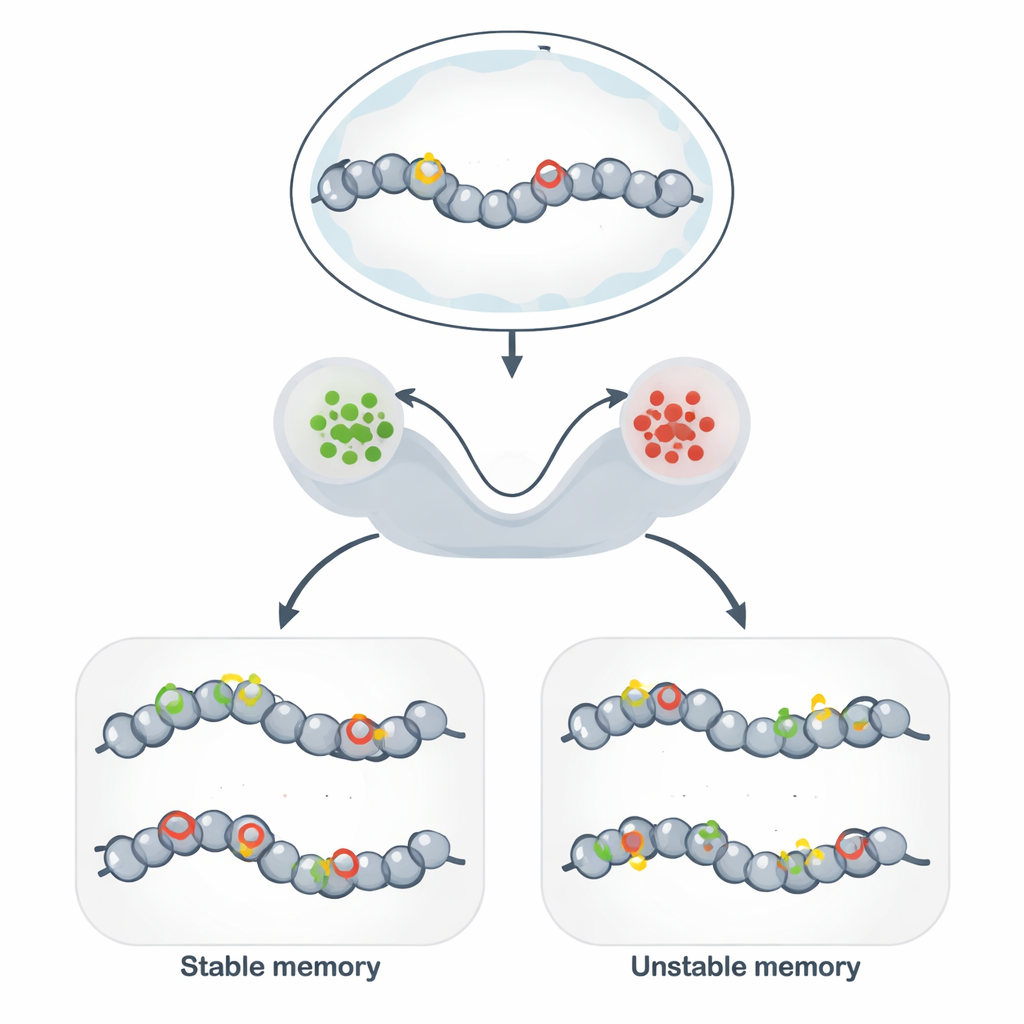
Bortom DNA: Stabilt märkta platser i genomet
Epigenetiskt minne gör det möjligt för genetiskt identiska celler att upprätthålla olika, stabila beteenden över många celldelningar. Istället för att ändra DNA-sekvensen dekorerar celler DNA och dess omgivande proteiner med kemiska taggar som luckrar upp eller drar ihop den lokala strukturen. När taggarna gynnar en öppen struktur tenderar närliggande gener att vara aktiva; när de gynnar en kompakt struktur tystas gener. Denna mekanism ligger bakom celltypens identitet, bestående immunsvar, vissa former av minnesfunktion i hjärnan och lovande verktyg inom syntetisk biologi som syftar till att ”programmera” stabila celltillstånd.
Varför slumpen inte kan ignoreras
På molekylär nivå är cellen en brusig miljö: viktiga molekyler förekommer ofta i små antal och stöter slumpmässigt ihop. Traditionella modeller som använder släta kurvor för att beskriva hur genaktivitet förändras över tid kan förutsäga flera stabila tillstånd, som två dalar separerade av en kulle. I sådana modeller, när systemet väl rullar ner i en dal, borde det stanna där för evigt. Men i verkligheten kan slumpmässiga molekylära händelser ibland sparka systemet över kullen till en annan dal. Artikeln presenterar stokastiska (sannolikhetsbaserade) ramar som behandlar reaktioner som slumpmässiga händelser och kvantifierar hur ofta sådana växlingar inträffar, till exempel genom medelvärdet för förstapassage-tider som mäter hur länge ett tillstånd vanligtvis varar innan brus utlöser ett hopp.
Matematiska linser på molekylärt kaos
Översikten beskriver två huvudsakliga sätt att modellera denna slumpmässighet. Stokastiska nätverk för kemiska reaktioner följer exakta molekylantal och behandlar systemet som en Markovprocess, där varje reaktion inträffar med en sannolikhet som beror på det nuvarande tillståndet. Detta tillvägagångssätt kan troget fånga sällsynta växlingar mellan stabila genuttryckstillstånd men är beräkningsmässigt tungt. En andra klass av modeller använder stokastiska differentialekvationer, som approximativt behandlar molekylantal som kontinuerliga storheter skakade av Gaussiskt brus. Varianter som den kemiska Langevinekvationen och linjär brusapproximation byter bort viss noggrannhet mot analytisk tydlighet, vilket tillåter forskare att härleda hur systemparametrar formar fluktuationer kring ett stabilt tillstånd och hur sannolika övergångar mellan tillstånd blir.
Kromatinkretsar som minnesmaskinvara
För att koppla dessa abstrakta modeller till biologin fokuserar författarna på kretsar för kromatinmodifiering: nätverk av kemiska markeringar på histonproteiner och DNA som förstärker varandra. Histonmärken som främjar aktivt kromatin, och de som främjar repressivt kromatin, kan vardera rekrytera enzymer som sprider samma märke till närliggande platser, vilket skapar kraftfull positiv återkoppling. Stokastiska modeller visar att när denna självförstärkning är snabb jämfört med radering utvecklar systemet två långlivade tillstånd — grovt ”PÅ” och ”AV” — som fungerar som binärt minne. Att lägga till DNA-metylering, en särskilt stabil märkning som kopieras under DNA-replikation, snedvrider systemet ytterligare mot långlivad repression och kan dramatiskt förlänga hur länge ett tystat tillstånd består.
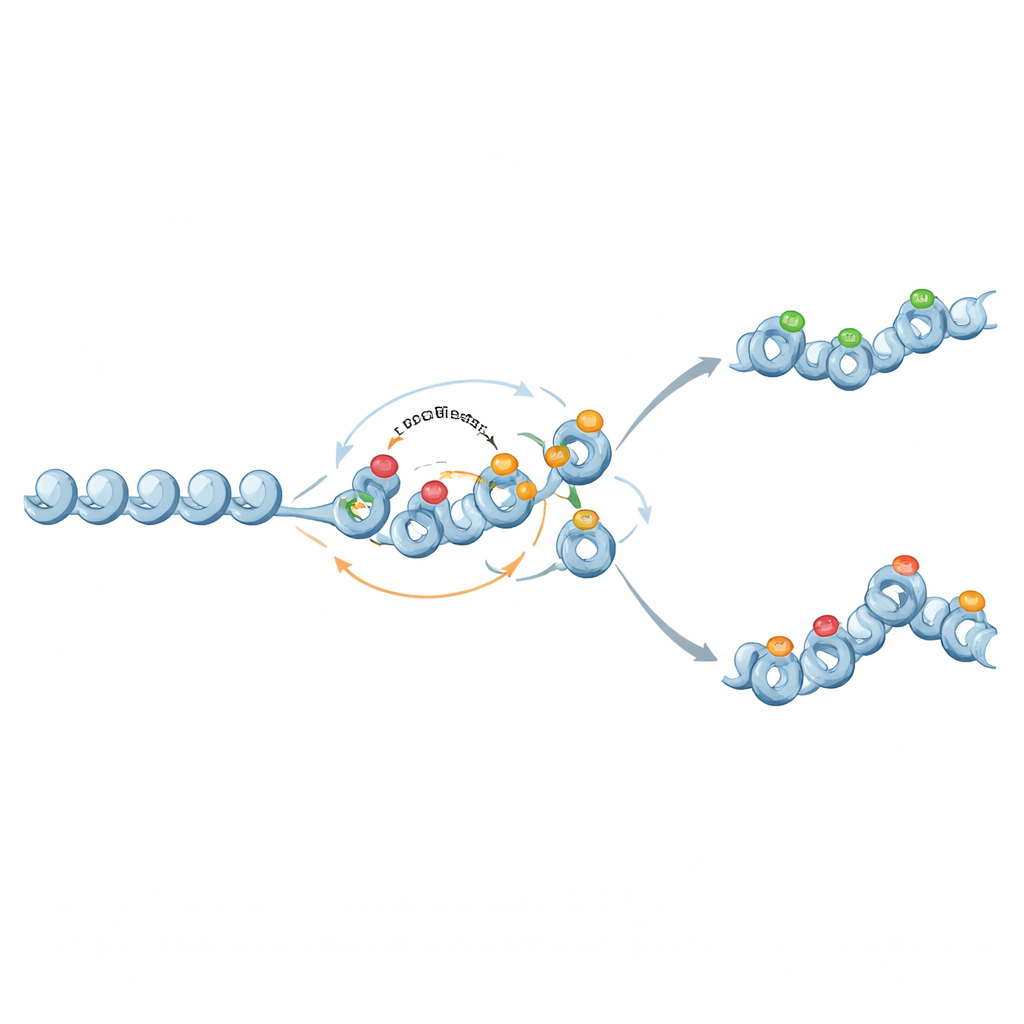
Från binära brytare till graderade minnen
Intressant nog kan samma molekylära komponenter också stödja mer nyanserat, analogt minne. När återkopplingen från repressiva histonmärken till DNA-metylering försvagas och metyleringen blir nästan permanent men icke-självförstärkande, fungerar metyleringen som en fast bakgrund som sätter en genuttrycksnivås medelvärde. Histonmärken fluktuerar då ovanpå denna bakgrund, ibland och kan ge upphov till två stabila kromatintillstånd och breda uttrycksdistributioner vid intermediära metyleringsnivåer. På detta sätt kan kromatinkretsar ställa in både hur stabil en gens aktivitet är och hur variabelt dess uttryck kan vara mellan celler.
Varför dessa modeller betyder något för medicin och design
Författarna avslutar med att konstatera att förståelsen av epigenetiskt minne kräver explicit modellering av molekylärt brus och tidpunkten för nyckelprocesser. Deras syntes lyfter fram vilka reaktionshastigheter och återkopplingsslingor som starkast kontrollerar hur länge celler vistas i aktiva eller repressiva tillstånd. Denna insikt kan vägleda experiment där man ändrar cellcykelns hastighet, enzymnivåer eller specifika kromatinmärken för att testa modellprediktioner. På sikt kan sådana modeller hjälpa till att konstruera celler som kan omprogrammeras på ett pålitligt sätt, behålla ett önskat öde eller lagra information på ett kontrollerbart vis — vilket öppnar möjligheter för regenerativ medicin, cancerbehandling och programmerbara immunsvar.
Citering: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Nyckelord: epigenetiskt minne, kromatinmodifieringar, DNA-metylering, stokastisk modellering, genreglering