Clear Sky Science · it
Modellizzazione stocastica della memoria epigenetica
Come le cellule ricordano chi sono
Ogni cellula del tuo corpo porta sostanzialmente lo stesso DNA, eppure una cellula cerebrale si comporta in modo molto diverso rispetto a una cellula della pelle o del sistema immunitario. Questo duraturo “senso di identità” deve essere copiato ogni volta che le cellule si dividono e, quando fallisce, possono insorgere malattie come il cancro. Questo articolo spiega come i ricercatori usano strumenti matematici per comprendere la memoria epigenetica—i marchi biochimici sul DNA e sul suo impacchettamento che permettono alle cellule di ricordare a lungo se particolari geni devono rimanere attivi o spenti.
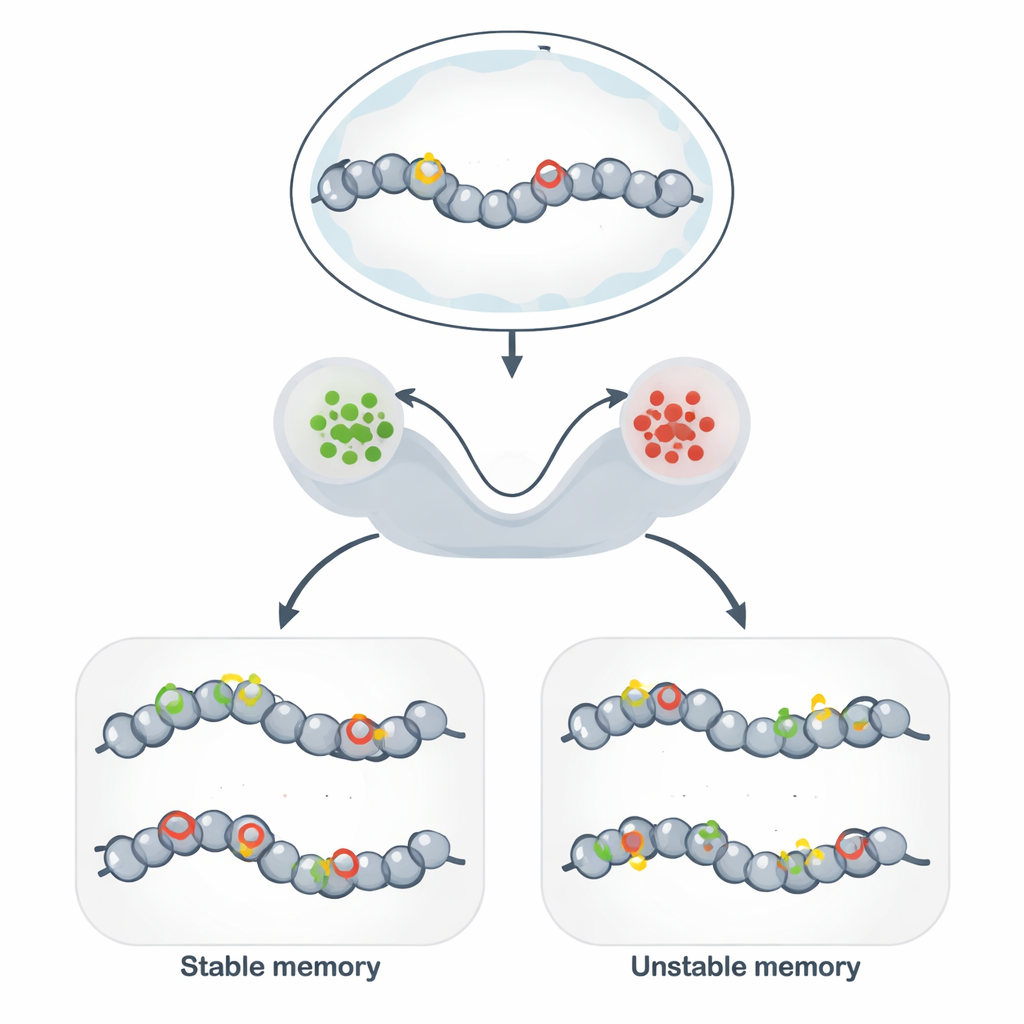
Oltre il DNA: marchi stabili sul genoma
La memoria epigenetica permette a cellule geneticamente identiche di mantenere comportamenti diversi e stabili per molte divisioni cellulari. Invece di modificare la sequenza del DNA, le cellule decorano il DNA e le proteine circostanti con tag chimici che allentano o irrigidiscono la struttura locale. Quando i tag favoriscono una struttura aperta, i geni vicini tendono ad essere attivi; quando favoriscono una struttura compatta, i geni vengono silenziati. Questo meccanismo è alla base dell’identità del tipo cellulare, della persistenza delle risposte immunitarie, di alcune forme di memoria cerebrale e di strumenti promettenti per la biologia sintetica che mirano a “programmare” stati cellulari stabili.
Perché il caso non può essere ignorato
Alla scala molecolare la cellula è un ambiente rumoroso: molecole chiave spesso esistono in piccoli numeri e si scontrano casualmente. I modelli tradizionali che usano curve regolari per descrivere come l’attività genica cambia nel tempo possono prevedere stati stabili multipli, come due valli separate da una collina. In tali modelli, una volta che il sistema scivola in una valle dovrebbe rimanervi per sempre. Ma nella realtà eventi molecolari casuali possono occasionalmente spingere il sistema oltre la collina verso un’altra valle. L’articolo introduce quadri stocastici (probabilistici) che trattano le reazioni come eventi casuali e quantificano con quale frequenza avvengono tali cambi di stato, per esempio attraverso i tempi medi di prima attraversata che misurano quanto a lungo uno stato dura tipicamente prima che il rumore provochi un salto.
Lenti matematiche sul caos molecolare
La recensione descrive due modi principali per modellare questa casualità. Le reti di reazioni chimiche stocastiche tracciano i conteggi esatti delle molecole e trattano il sistema come un processo di Markov, in cui ogni reazione scatta con una probabilità che dipende dallo stato presente. Questo approccio può catturare fedelmente i rari switch tra stati stabili di espressione genica ma è computazionalmente pesante. Una seconda classe di modelli usa equazioni differenziali stocastiche, che approssimano i conteggi molecolari come quantità continue soggette a rumore gaussiano. Varianti come l’equazione di Langevin chimica e l’approssimazione del rumore lineare scambiano parte dell’accuratezza per una chiarezza analitica, permettendo ai ricercatori di ricavare come i parametri del sistema influenzano le fluttuazioni attorno a uno stato stabile e quanto probabili diventano le transizioni tra stati.
I circuiti della cromatina come hardware della memoria
Per collegare questi modelli astratti alla biologia, gli autori si concentrano sui circuiti di modifica della cromatina: reti di marchi chimici su proteine istoniche e DNA che si rafforzano a vicenda. I tag istonici che promuovono la cromatina attiva e quelli che promuovono la cromatina repressa possono ciascuno reclutare enzimi che diffondono lo stesso marchio a siti vicini, creando un potente feedback positivo. I modelli stocastici mostrano che quando questo autorinforzo è rapido rispetto alla cancellazione, il sistema sviluppa due stati di lunga durata—grossolanamente “ACCESO” e “SPENTO”—che funzionano come memoria binaria. L’aggiunta della metilazione del DNA, un marchio altamente stabile copiato durante la replicazione del DNA, sposta ulteriormente il sistema verso la repressione di lunga durata e può estendere in modo significativo quanto a lungo persiste uno stato silenziato.
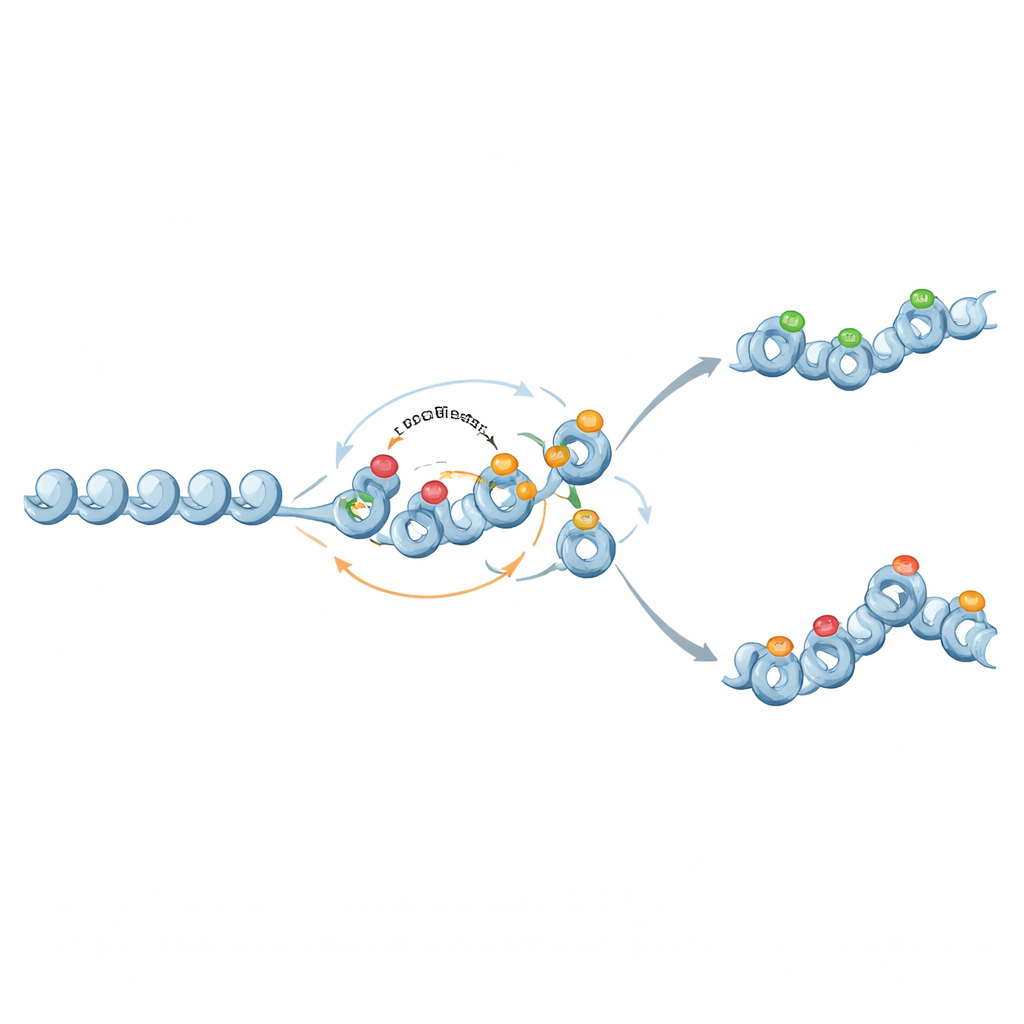
Dagli interruttori binari alle memorie graduate
È interessante che gli stessi elementi molecolari possano anche sostenere una memoria più sfumata e analogica. Quando il feedback dai marchi istonici repressivi alla metilazione del DNA è indebolito e la metilazione diventa quasi permanente ma non auto-amplificante, la metilazione agisce come uno sfondo fisso che imposta un livello medio di espressione genica. I marchi istonici quindi fluttuano su questo sfondo, talvolta producendo due stati cromatinici stabili e ampie distribuzioni di espressione a livelli intermedi di metilazione. In questo modo i circuiti della cromatina possono modulare sia quanto è stabile l’attività di un gene sia quanto la sua espressione può variare tra le cellule.
Perché questi modelli contano per medicina e design
Gli autori concludono che comprendere la memoria epigenetica richiede di modellare esplicitamente il rumore molecolare e i tempi dei processi chiave. La loro sintesi mette in evidenza quali tassi di reazione e quali anelli di retroazione controllano più fortemente il tempo di permanenza delle cellule in stati attivi o repressi. Questa intuizione può guidare esperimenti che alterano la velocità del ciclo cellulare, i livelli enzimatici o specifici marchi cromatinici per testare le previsioni dei modelli. A lungo termine, tali modelli potrebbero aiutare a progettare cellule che possano essere riprogrammate in modo affidabile, mantenere un destino desiderato o immagazzinare informazioni in modo controllabile—aprendo possibilità per la medicina rigenerativa, la terapia del cancro e risposte immunitarie programmabili.
Citazione: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Parole chiave: memoria epigenetica, modificazioni della cromatina, metilazione del DNA, modellizzazione stocastica, regolazione genica