Clear Sky Science · ja
エピジェネティック記憶の確率的モデリング
細胞はどのように自らを記憶するか
体内のほぼすべての細胞は同じDNAを持ちながら、脳細胞が皮膚細胞や免疫細胞と全く異なる振る舞いをします。この持続的な「同一性の感覚」は細胞分裂のたびに複製されなければならず、失敗するとがんのような疾患が生じ得ます。本稿は、特定の遺伝子が長期にわたってオンかオフかを細胞が記憶する手がかりとなる、DNAやそのパッケージに付く生化学的な印(エピジェネティックマーク)を理解するために研究者がどのように数学的手法を用いるかを解説します。
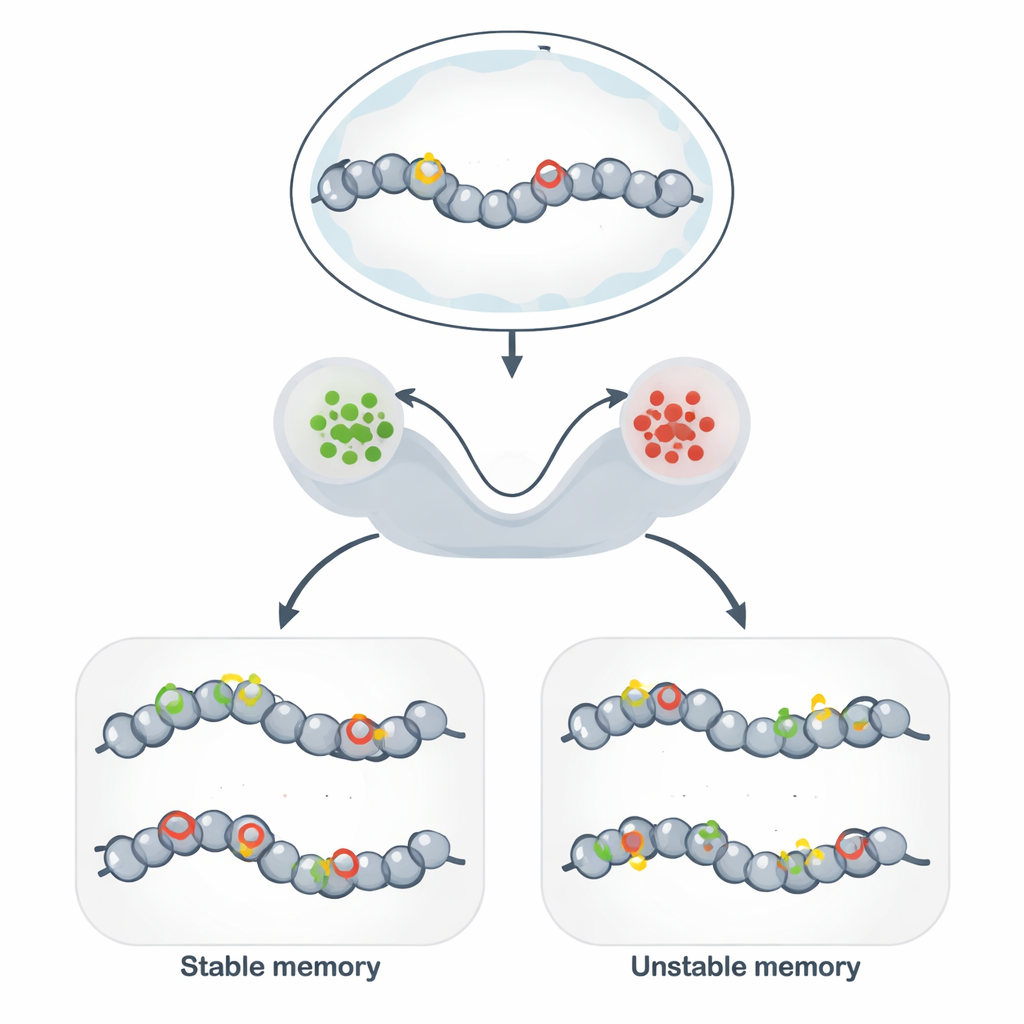
DNAを超えて:ゲノム上の安定した印
エピジェネティック記憶により、遺伝的に同一な細胞が多数の細胞分裂を経ても異なる安定した振る舞いを維持できます。これはDNA配列を変えるのではなく、DNAとその周囲のタンパク質に化学的なタグを付けて局所構造を緩めたり締めたりすることで実現されます。タグが開いた構造を促すと近傍の遺伝子は活性化しやすく、締まった構造を促すと遺伝子はサイレンスされます。この仕組みは細胞型の同一性、免疫応答の持続、脳の一部の記憶形式、そして安定した細胞状態を「プログラム」しようとする合成生物学の有望な手法の基盤となっています。
なぜランダム性を無視できないのか
分子スケールでは細胞内はノイズに満ちています:重要な分子はしばしば少数しか存在せず、ランダムに衝突します。遺伝子活性の時間変化を滑らかな曲線で記述する従来のモデルは、二つの谷が山で分かれたような複数の安定状態を予測できます。そうしたモデルでは一度谷に落ちればそこに永遠に留まるはずです。しかし現実にはランダムな分子事象が時折システムを山越えさせ、別の谷へ押しやることがあります。この記事は反応をランダム事象として扱い、そのようなスイッチがどの頻度で起きるかを定量化する確率的(確率論的)フレームワークを紹介します。たとえば平均初到達時間(mean first-passage time)によって、ノイズがジャンプを誘発するまで典型的にどれくらいの時間その状態が続くかを測ります。
分子のカオスを数学的に見るレンズ
レビューでは、このランダム性をモデル化する主な二つの手法を説明します。確率的化学反応ネットワークは分子数を正確に追跡し、各反応が現在の状態に依存する確率で発生するマルコフ過程として系を扱います。このアプローチは遺伝子発現の安定状態間で起きるまれなスイッチを忠実に再現できますが、計算コストが高くなります。第二のモデル群は確率微分方程式を用い、分子数をガウスノイズで揺らぐ連続量として近似します。化学ランジュバン方程式や線形ノイズ近似のような変法は精度の一部を犠牲にする代わりに解析的明快さを与え、系パラメータが安定状態周りの揺らぎや状態間遷移の確率にどのように影響するかを導出可能にします。
記憶を担うハードウェアとしてのクロマチン回路
これら抽象的モデルを生物学に結びつけるため、著者らはクロマチン修飾回路に着目します:ヒストンタンパク質やDNA上の化学的な印が互いに相互補強するネットワークです。活性化を促すヒストンタグや抑制を促すヒストンタグは、それぞれ同じタグを隣接部位に広げる酵素を呼び寄せることができ、強力な正のフィードバックを生みます。確率的モデルは、この自己強化が消去より速い場合に系が二つの長寿命状態、概ね「ON」と「OFF」を発現し、二値の記憶として機能することを示します。DNAメチル化のような、DNA複製時にコピーされる非常に安定なタグが加わると、抑制側への偏りが増し、沈黙状態の持続時間が劇的に延びることがあります。
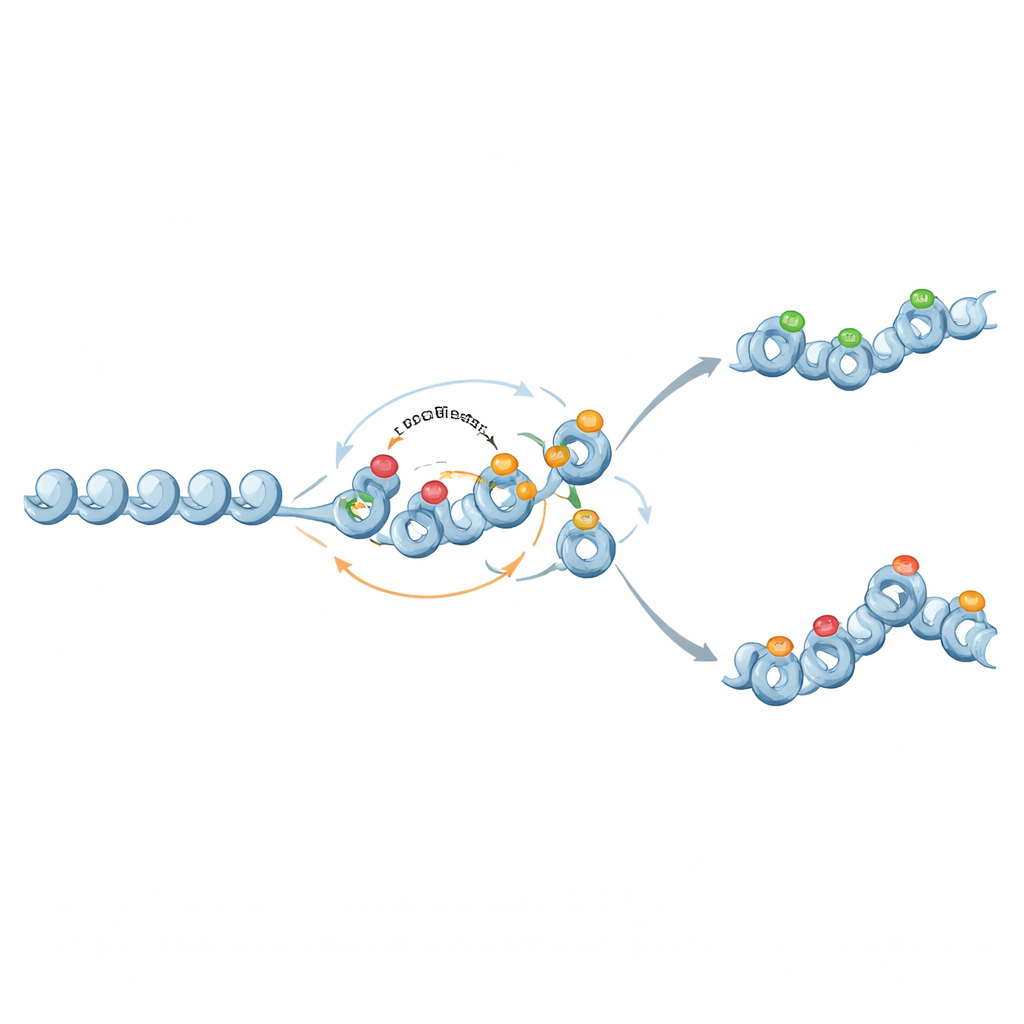
二値スイッチから段階的記憶へ
興味深いことに、同じ分子成分はより微妙で連続的な(アナログな)記憶も支え得ます。抑制的ヒストンマークからDNAメチル化へのフィードバックが弱まり、メチル化がほぼ永久的だが自己増幅的でない場合、メチル化は平均的な遺伝子発現レベルを設定する固定された背景として働きます。その上でヒストンマークが揺らぎ、時に二つの安定したクロマチン状態を生み、中間的なメチル化レベルで広がった発現分布を生じさせます。このようにしてクロマチン回路は、遺伝子活性の安定性と細胞間での発現のばらつきを同時に調節できます。
これらのモデルが医学と設計にもたらす意義
著者らは結論として、エピジェネティック記憶を理解するには分子ノイズと主要プロセスの時間的側面を明示的にモデル化することが必要だと述べます。彼らの総合は、細胞が活性または抑制状態にとどまる時間を最も強く制御する反応速度やフィードバック回路を浮き彫りにします。この知見は細胞周期速度、酵素量、特定のクロマチンマークを変える実験の設計に道を付け、モデル予測を検証する手助けになります。長期的には、こうしたモデルは信頼して再プログラムできる細胞、望ましい運命を保持する細胞、あるいは制御可能な形で情報を記憶する細胞を設計するのに役立ち、再生医療、がん治療、プログラム可能な免疫応答の可能性を開くでしょう。
引用: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
キーワード: エピジェネティック記憶, クロマチン修飾, DNAメチル化, 確率的モデリング, 遺伝子制御