Clear Sky Science · de
Stochastische Modellierung epigenetischen Gedächtnisses
Wie Zellen sich an ihre Identität erinnern
Jede Zelle in Ihrem Körper trägt im Wesentlichen dieselbe DNA, trotzdem verhält sich eine Gehirnzelle sehr anders als eine Haut- oder Immunzelle. Dieses andauernde „Gefühl der Identität“ muss bei jeder Zellteilung kopiert werden, und wenn es versagt, können Krankheiten wie Krebs entstehen. Dieser Artikel erklärt, wie Forscher mathematische Werkzeuge einsetzen, um epigenetisches Gedächtnis zu verstehen — die biochemischen Markierungen auf DNA und ihrer Verpackung, die Zellen erlauben, sich langfristig zu merken, ob bestimmte Gene ein- oder ausgeschaltet bleiben sollen.
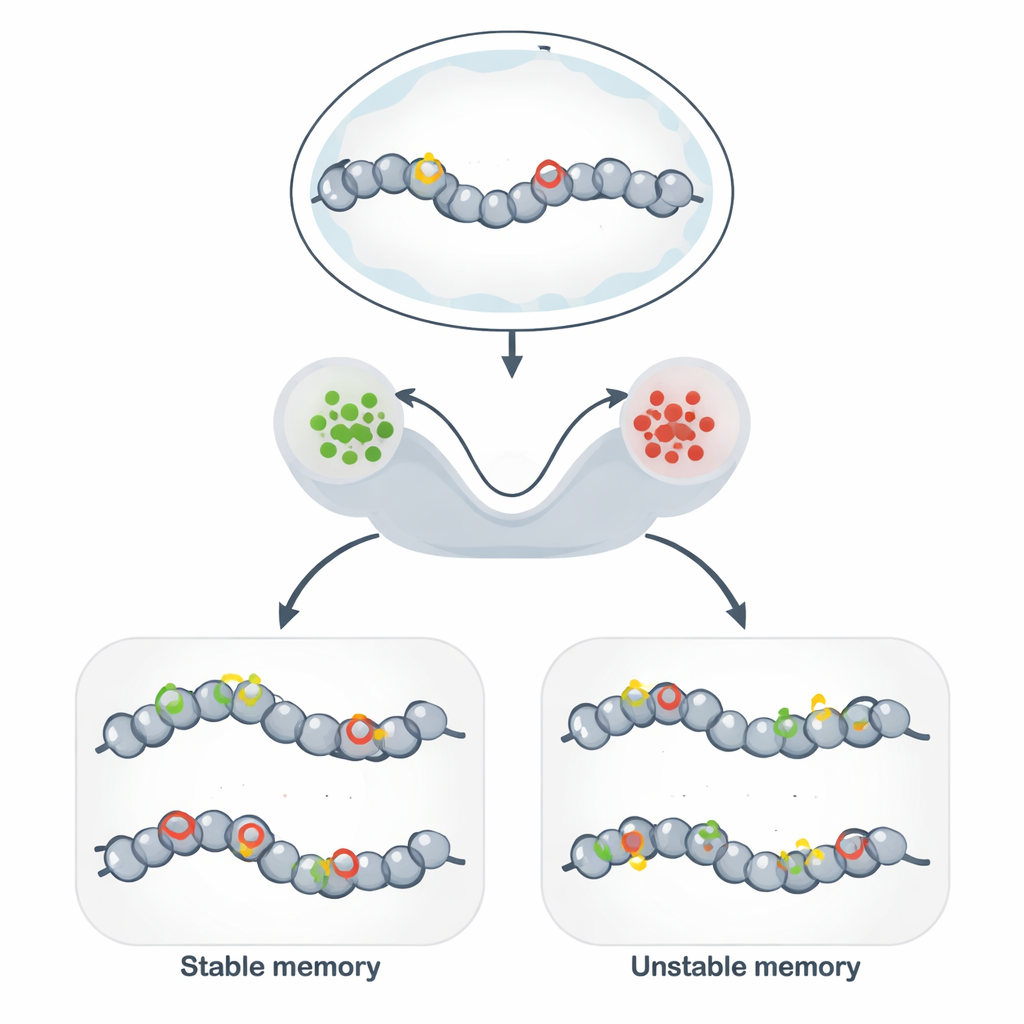
Jenseits der DNA: Stabile Markierungen im Genom
Epigenetisches Gedächtnis ermöglicht es genetisch identischen Zellen, über viele Zellteilungen hinweg unterschiedliche, stabile Verhaltensweisen beizubehalten. Anstatt die DNA-Sequenz zu verändern, versehen Zellen DNA und die umgebenden Proteine mit chemischen Tags, die die lokale Struktur lockern oder verdichten. Wenn Tags eine offene Struktur begünstigen, sind nahegelegene Gene tendenziell aktiv; wenn sie eine kompakte Struktur fördern, werden Gene stummgeschaltet. Dieser Mechanismus liegt der Zelltypidentität, der Persistenz von Immunantworten, einigen Formen des Gedächtnisses im Gehirn und vielversprechenden Werkzeugen der synthetischen Biologie zugrunde, die darauf abzielen, stabile Zellzustände „zu programmieren“.
Warum Zufälligkeit nicht ignoriert werden kann
Auf molekularer Ebene ist die Zelle ein lauter Ort: Schlüsselmoleküle liegen oft in geringer Anzahl vor und stoßen zufällig aufeinander. Traditionelle Modelle, die glatte Kurven verwenden, um zu beschreiben, wie sich Genaktivität im Zeitverlauf ändert, können mehrere stabile Zustände vorhersagen, etwa zwei Täler getrennt durch einen Hügel. In solchen Modellen sollte das System, einmal in ein Tal gerollt, dort für immer bleiben. In Wirklichkeit können jedoch zufällige molekulare Ereignisse das System gelegentlich über den Hügel in ein anderes Tal katapultieren. Der Artikel stellt stochastische (wahrscheinlichkeitsbasierte) Rahmen vor, die Reaktionen als Zufallsereignisse behandeln und quantifizieren, wie oft solche Umschläge auftreten — etwa mithilfe von mittleren First-Passage-Zeiten, die messen, wie lange ein Zustand typischerweise anhält, bevor Rauschen einen Sprung auslöst.
Mathematische Linsen für molekulares Chaos
Die Übersicht beschreibt zwei Hauptansätze zur Modellierung dieser Zufälligkeit. Stochastische Netzwerke chemischer Reaktionen verfolgen exakte Molekülzahlen und behandeln das System als Markov-Prozess, bei dem jede Reaktion mit einer Wahrscheinlichkeit feuert, die vom gegenwärtigen Zustand abhängt. Dieser Ansatz kann seltene Umschläge zwischen stabilen Expressionszuständen treu abbilden, ist aber rechenintensiv. Eine zweite Modellklasse verwendet stochastische Differentialgleichungen, die Molekülzahlen als kontinuierliche Größen approximieren, die von gaußschem Rauschen geschüttelt werden. Varianten wie die chemische Langevin-Gleichung und die lineare Rauschapproximation tauschen etwas Genauigkeit gegen analytische Klarheit ein und erlauben es Forschern zu bestimmen, wie Systemparameter Schwankungen um einen stabilen Zustand formen und wie wahrscheinlich Übergänge zwischen Zuständen werden.
Chromatin-Schaltkreise als Speicher-Hardware
Um diese abstrakten Modelle mit der Biologie zu verbinden, konzentrieren sich die Autoren auf Chromatin-Modifikationsschaltkreise: Netzwerke chemischer Markierungen an Histonproteinen und DNA, die sich gegenseitig verstärken. Histon-Tags, die aktives Chromatin fördern, und solche, die repressives Chromatin begünstigen, können jeweils Enzyme rekrutieren, die das gleiche Tag an benachbarte Stellen verbreiten und so starke positive Rückkopplung erzeugen. Stochastische Modelle zeigen, dass bei schneller Selbstverstärkung im Vergleich zur Löschung das System zwei langlebige Zustände entwickelt — grob „AN“ und „AUS“ — die als binärer Speicher fungieren. Die Hinzufügung von DNA-Methylierung, einem sehr stabilen Tag, der während der DNA-Replikation kopiert wird, verschiebt das System zusätzlich in Richtung langlebiger Repression und kann die Persistenz eines stillgelegten Zustands drastisch verlängern.
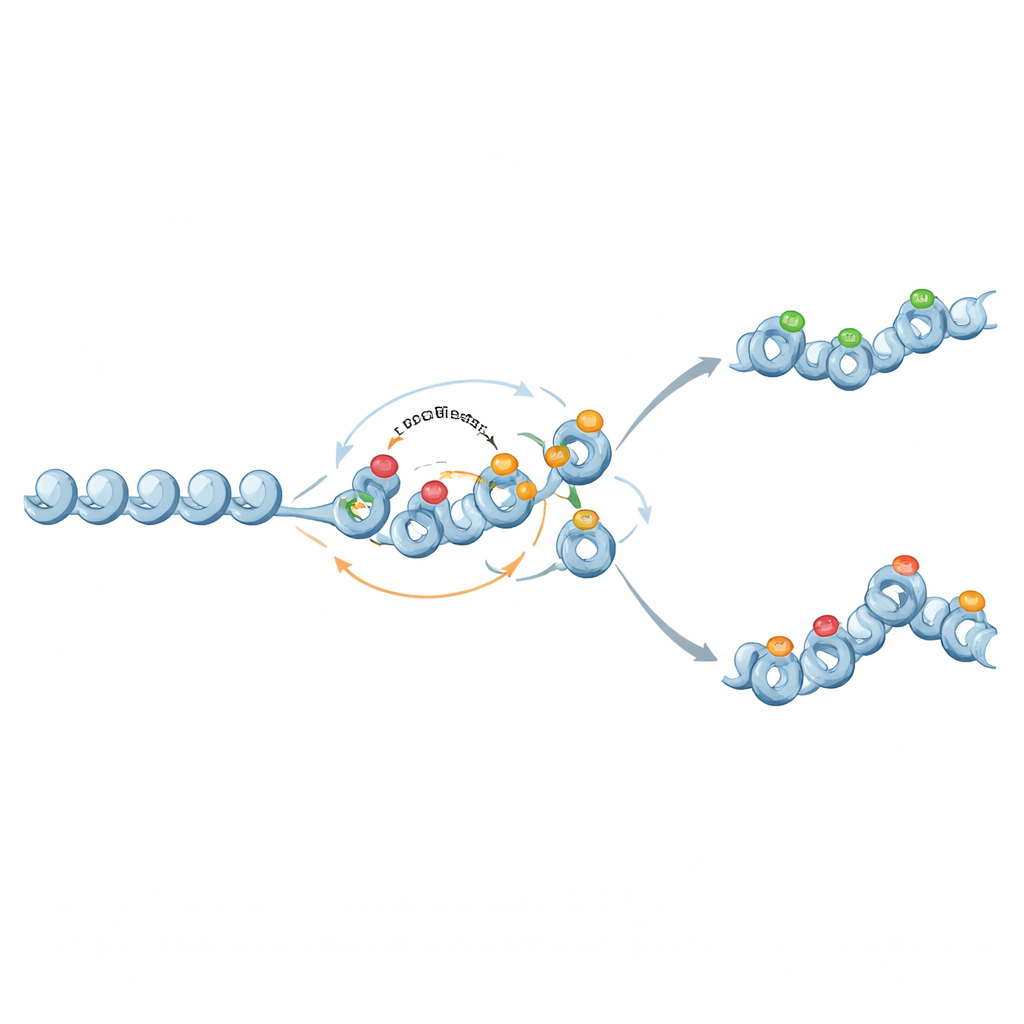
Von binären Schaltern zu abgestuften Gedächtnissen
Interessanterweise können dieselben molekularen Komponenten auch nuanciertere, analoge Formen des Gedächtnisses unterstützen. Wenn die Rückkopplung von repressiven Histonmarken zu DNA-Methylierung geschwächt ist und Methylierung nahezu dauerhaft, aber nicht selbstverstärkend wird, wirkt Methylierung als feste Kulisse, die ein mittleres Genexpressionsniveau einstellt. Histonmarken schwanken dann auf dieser Kulisse, wobei sie manchmal zwei stabile Chromatinzustände und breite Expressionsverteilungen bei intermediären Methylierungsgraden erzeugen. Auf diese Weise können Chromatin-Schaltkreise sowohl die Stabilität der Genaktivität als auch die Variabilität der Expression über Zellen hinweg feinjustieren.
Warum diese Modelle für Medizin und Design wichtig sind
Die Autoren schließen, dass das Verständnis epigenetischen Gedächtnisses die explizite Modellierung molekularen Rauschens und das Timing zentraler Prozesse erfordert. Ihre Synthese hebt hervor, welche Reaktionsraten und Rückkopplungsschleifen die Verweildauer von Zellen im aktiven oder repressiven Zustand am stärksten steuern. Diese Einsichten können Experimente leiten, die Zellzyklusgeschwindigkeit, Enzymlevel oder spezifische Chromatin-Marken verändern, um Modellvorhersagen zu prüfen. Langfristig könnten solche Modelle helfen, Zellen zu entwerfen, die sich zuverlässig umprogrammieren lassen, ein gewünschtes Schicksal beibehalten oder Informationen kontrollierbar speichern — und so Möglichkeiten für regenerative Medizin, Krebstherapien und programmierbare Immunantworten eröffnen.
Zitation: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Schlüsselwörter: epigenetisches Gedächtnis, Chromatin-Modifikationen, DNA-Methylierung, stochastische Modellierung, Genregulation