Clear Sky Science · fr
Modélisation stochastique de la mémoire épigénétique
Comment les cellules se souviennent de ce qu’elles sont
Toutes les cellules de votre corps portent essentiellement le même ADN, et pourtant une cellule cérébrale se comporte très différemment d’une cellule de la peau ou du système immunitaire. Ce « sens de l’identité » durable doit être recopié à chaque division cellulaire, et lorsqu’il fait défaut, des maladies comme le cancer peuvent apparaître. Cet article explique comment les chercheurs utilisent des outils mathématiques pour comprendre la mémoire épigénétique — les marques biochimiques sur l’ADN et son emballage qui permettent aux cellules de conserver à long terme l’état d’activation ou de répression de certains gènes.
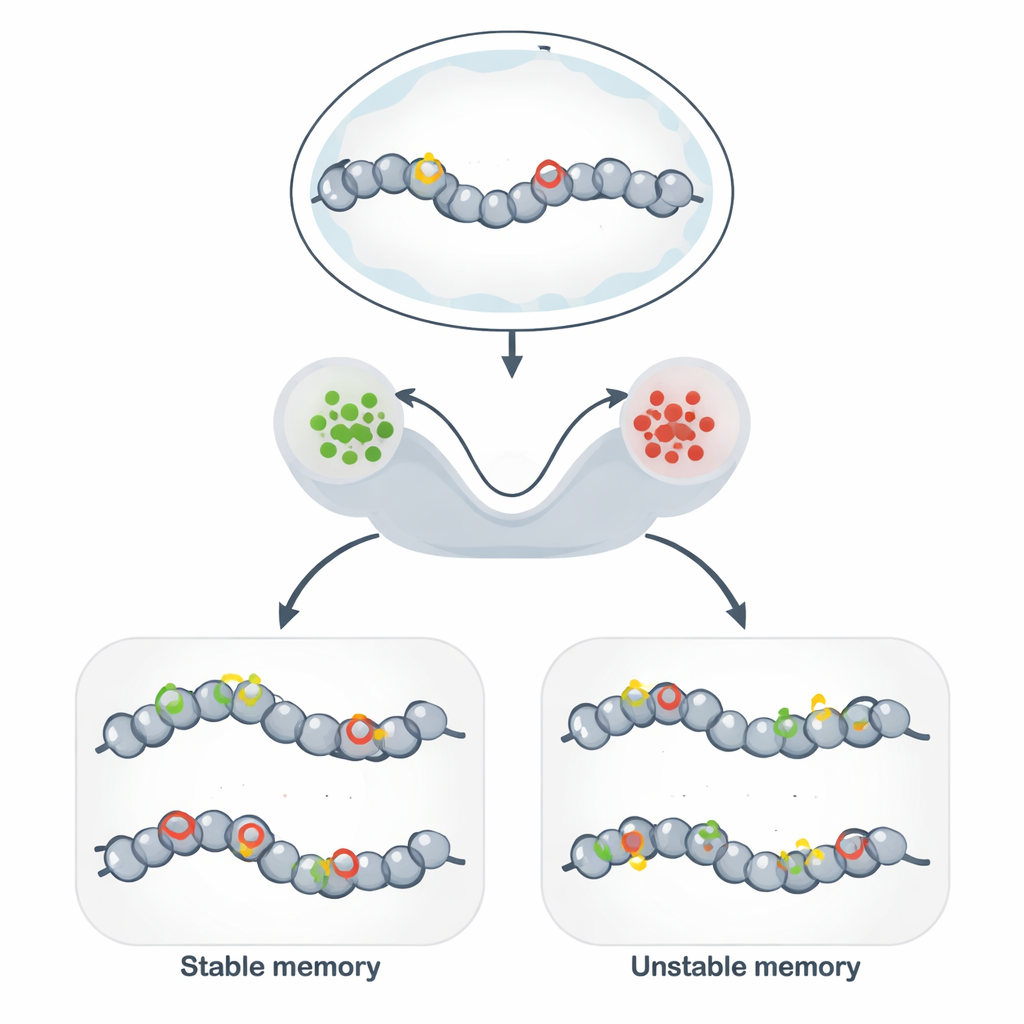
Au-delà de l’ADN : des marques stables sur le génome
La mémoire épigénétique permet à des cellules génétiquement identiques de maintenir des comportements différents et stables sur de nombreuses divisions cellulaires. Plutôt que de modifier la séquence d’ADN, les cellules décorent l’ADN et les protéines qui l’entourent avec des étiquettes chimiques qui desserrent ou resserrent la structure locale. Lorsque ces marques favorisent une structure ouverte, les gènes voisins ont tendance à être actifs ; lorsqu’elles favorisent une structure compacte, les gènes sont silencieux. Ce mécanisme sous-tend l’identité des types cellulaires, la persistance des réponses immunitaires, certaines formes de mémoire cérébrale, ainsi que des outils prometteurs de biologie synthétique visant à « programmer » des états cellulaires stables.
Pourquoi le hasard ne peut être ignoré
À l’échelle moléculaire, la cellule est un milieu bruyant : des molécules clés existent souvent en petit nombre et se rencontrent au hasard. Les modèles traditionnels qui utilisent des courbes lisses pour décrire l’évolution de l’activité génique au cours du temps peuvent prédire plusieurs états stables, comme deux vallées séparées par une colline. Dans de tels modèles, une fois que le système roule dans une vallée, il devrait y rester pour toujours. Mais en réalité, des événements moléculaires aléatoires peuvent occasionnellement pousser le système par-dessus la colline vers l’autre vallée. L’article présente des cadres stochastiques (probabilistes) qui traitent les réactions comme des événements aléatoires et quantifient la fréquence de ces basculements, par exemple à l’aide de temps moyens de premier passage qui mesurent combien de temps un état dure typiquement avant que le bruit n’entraîne une transition.
Lentilles mathématiques sur le chaos moléculaire
La revue décrit deux approches principales pour modéliser ce hasard. Les réseaux de réactions chimiques stochastiques suivent les comptes exacts de molécules et considèrent le système comme un processus de Markov, où chaque réaction se produit avec une probabilité dépendant de l’état présent. Cette approche peut capturer fidèlement les changements rares entre états d’expression génique stables mais est coûteuse en calcul. Une seconde classe de modèles utilise des équations différentielles stochastiques, qui approximent les nombres de molécules par des quantités continues agitéees par un bruit gaussien. Des variantes telles que l’équation de Langevin chimique et l’approximation du bruit linéaire sacrifient un peu de précision pour une clarté analytique, permettant aux chercheurs de dériver comment les paramètres du système façonnent les fluctuations autour d’un état stable et la probabilité des transitions entre états.
Les circuits de chromatine comme matériel de mémoire
Pour relier ces modèles abstraits à la biologie, les auteurs se concentrent sur les circuits de modification de la chromatine : des réseaux de marques chimiques sur les histones et l’ADN qui se renforcent mutuellement. Les marques d’histones favorisant une chromatine active, et celles favorisant une chromatine réprimée, peuvent chacune recruter des enzymes qui propagent la même marque aux sites voisins, créant un rétrocontrôle positif puissant. Les modèles stochastiques montrent que lorsque cette auto-renforcement est rapide par rapport à l’effacement, le système développe deux états de longue durée — globalement « ON » et « OFF » — qui fonctionnent comme une mémoire binaire. L’ajout de la méthylation de l’ADN, une marque très stable copiée lors de la réplication, biaise encore le système vers la répression durable et peut prolonger considérablement la durée d’un état silencieux.
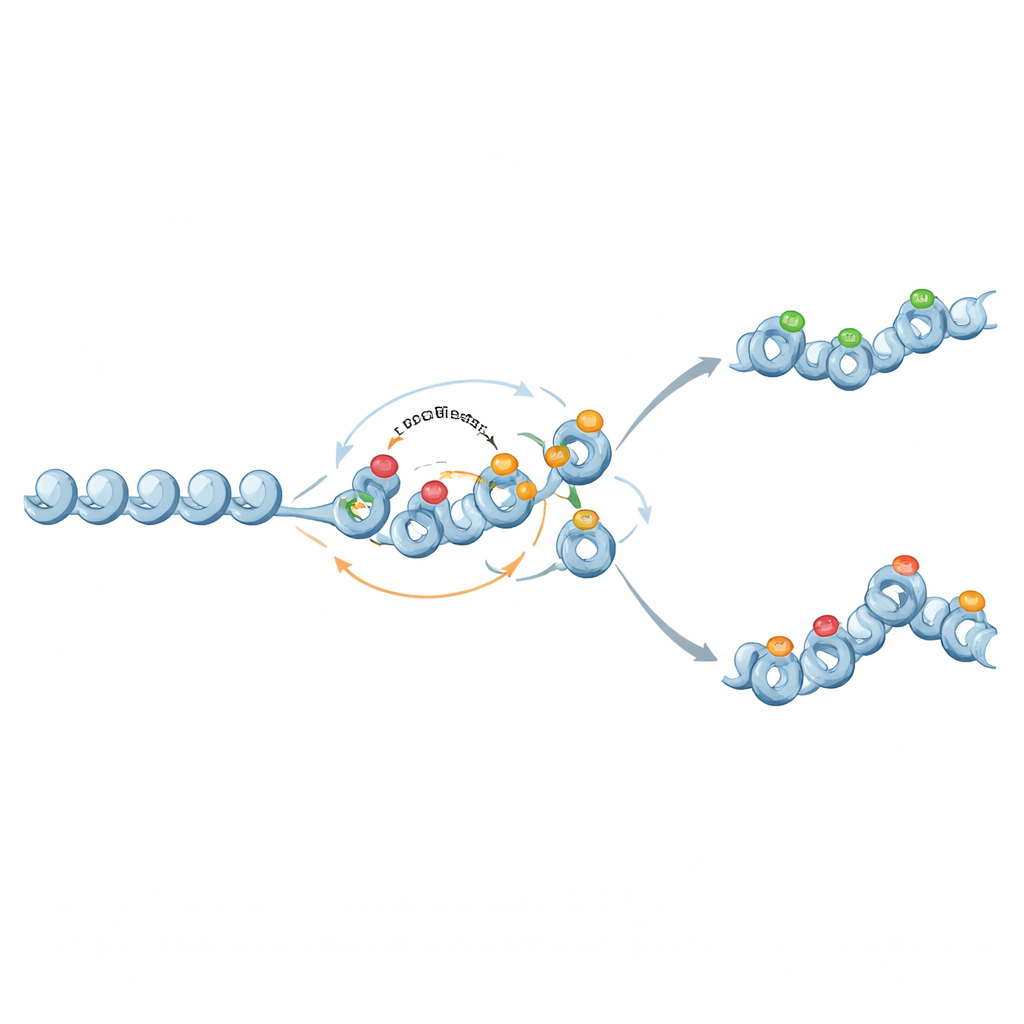
Des commutateurs binaires aux mémoires graduées
De manière intéressante, les mêmes acteurs moléculaires peuvent aussi soutenir une mémoire plus nuancée, analogique. Lorsque le rétrocontrôle des marques histones répressives vers la méthylation de l’ADN est affaibli et que la méthylation devient quasi permanente mais non auto-amplificatrice, la méthylation agit comme un décor fixe qui définit un niveau moyen d’expression génique. Les marques d’histones fluctuent alors par-dessus ce décor, produisant parfois deux états chromatiniens stables et des distributions larges d’expression à des niveaux intermédiaires de méthylation. De cette façon, les circuits de chromatine peuvent régler à la fois la stabilité de l’activité d’un gène et la variabilité de son expression entre cellules.
Pourquoi ces modèles comptent pour la médecine et la conception
Les auteurs concluent que comprendre la mémoire épigénétique nécessite de modéliser explicitement le bruit moléculaire et le calendrier des processus clés. Leur synthèse met en évidence les vitesses de réaction et les boucles de rétroaction qui contrôlent le plus fortement le temps de résidence des cellules dans des états actifs ou réprimés. Cette connaissance peut orienter des expériences modifiant la vitesse du cycle cellulaire, les niveaux d’enzymes ou des marques chromatiniennes spécifiques pour tester les prédictions des modèles. À long terme, de tels modèles pourraient aider à concevoir des cellules reprogrammables de façon fiable, à maintenir un destin désiré ou à stocker de l’information d’une manière contrôlable — ouvrant des perspectives pour la médecine régénérative, la thérapie anticancéreuse et des réponses immunitaires programmables.
Citation: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Mots-clés: mémoire épigénétique, modifications de la chromatine, méthylation de l’ADN, modélisation stochastique, régulation génique