Clear Sky Science · pt
Modelagem estocástica da memória epigenética
Como as Células Lembram Quem São
Todas as células do seu corpo carregam, essencialmente, o mesmo DNA, e ainda assim uma célula do cérebro se comporta de forma muito diferente de uma célula da pele ou do sistema imunológico. Esse “senso de identidade” duradouro precisa ser copiado cada vez que as células se dividem, e quando falha, doenças como o câncer podem surgir. Este artigo explica como pesquisadores usam ferramentas matemáticas para entender a memória epigenética — as marcas bioquímicas no DNA e em seu empacotamento que permitem às células lembrar a longo prazo se genes específicos devem permanecer ligados ou desligados.
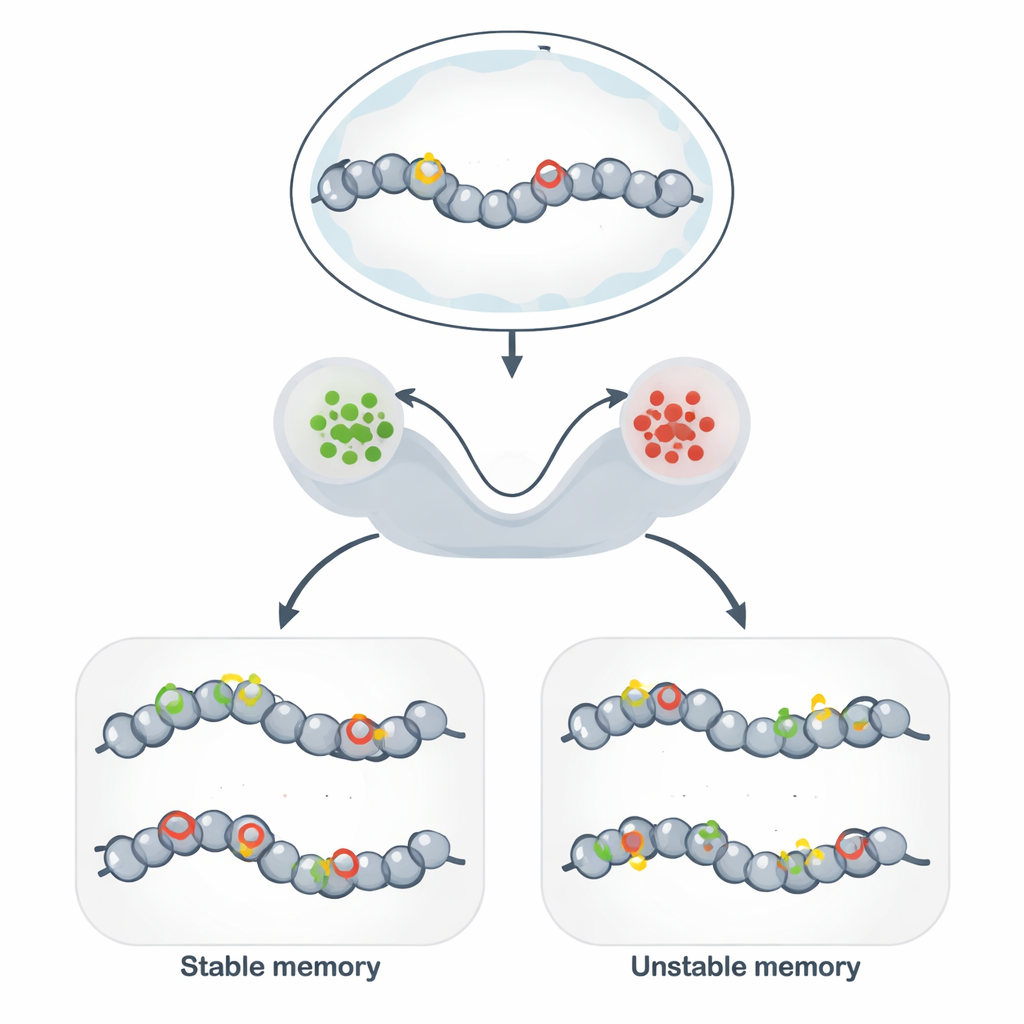
Além do DNA: Marcas Estáveis no Genoma
A memória epigenética permite que células geneticamente idênticas mantenham comportamentos diferentes e estáveis por muitas divisões celulares. Em vez de alterar a sequência do DNA, as células decoram o DNA e as proteínas ao seu redor com marcas químicas que afrouxam ou apertam a estrutura local. Quando as marcas favorecem uma estrutura aberta, genes próximos tendem a estar ativos; quando favorecem uma estrutura compacta, os genes são silenciados. Esse mecanismo fundamenta a identidade do tipo celular, a persistência de respostas imunes, algumas formas de memória cerebral e ferramentas promissoras para biologia sintética que visam “programar” estados celulares estáveis.
Por que o Acaso Não Pode Ser Ignorado
Na escala molecular, a célula é um ambiente ruidoso: moléculas-chave frequentemente existem em números pequenos e colidem umas com as outras ao acaso. Modelos tradicionais que usam curvas suaves para descrever como a atividade gênica muda ao longo do tempo podem prever múltiplos estados estáveis, como dois vales separados por uma colina. Nesses modelos, uma vez que o sistema cai em um vale, deveria permanecer lá para sempre. Mas, na realidade, eventos moleculares aleatórios podem ocasionalmente empurrar o sistema para o outro lado da colina, para outro vale. O artigo apresenta estruturas estocásticas (probabilísticas) que tratam reações como eventos aleatórios e quantificam com que frequência tais trocas ocorrem, por exemplo por meio de tempos médios de primeira passagem que medem quanto tempo um estado normalmente dura antes do ruído desencadear uma transição.
Lentes Matemáticas sobre o Caos Molecular
A revisão descreve duas maneiras principais de modelar essa aleatoriedade. Redes estocásticas de reações químicas acompanham contagens exatas de moléculas e tratam o sistema como um processo de Markov, em que cada reação ocorre com uma probabilidade que depende do estado presente. Essa abordagem pode capturar fielmente trocas raras entre estados estáveis de expressão gênica, mas é computacionalmente pesada. Uma segunda classe de modelos usa equações diferenciais estocásticas, que aproximam contagens moleculares como quantidades contínuas agitadas por ruído gaussiano. Variantes como a equação de Langevin química e a aproximação de ruído linear trocam um pouco de precisão por clareza analítica, permitindo aos pesquisadores derivar como parâmetros do sistema moldam as flutuações ao redor de um estado estável e quão prováveis se tornam as transições entre estados.
Circuitos de Cromatina como Hardware de Memória
Para conectar esses modelos abstratos à biologia, os autores enfocam circuitos de modificação da cromatina: redes de marcas químicas em proteínas histonas e no DNA que se reforçam mutuamente. Marcas de histonas que promovem cromatina ativa e aquelas que promovem cromatina reprimida podem recrutar enzimas que espalham a mesma marca para sítios vizinhos, criando realimentação positiva poderosa. Modelos estocásticos mostram que, quando esse autorreforço é rápido em comparação com a remoção, o sistema desenvolve dois estados de longa duração — grosso modo “LIGADO” e “DESLIGADO” — que funcionam como memória binária. A adição da metilação do DNA, uma marca altamente estável copiada durante a replicação do DNA, viésa ainda mais o sistema para a repressão de longa duração e pode estender dramaticamente quanto tempo um estado silenciado persiste.
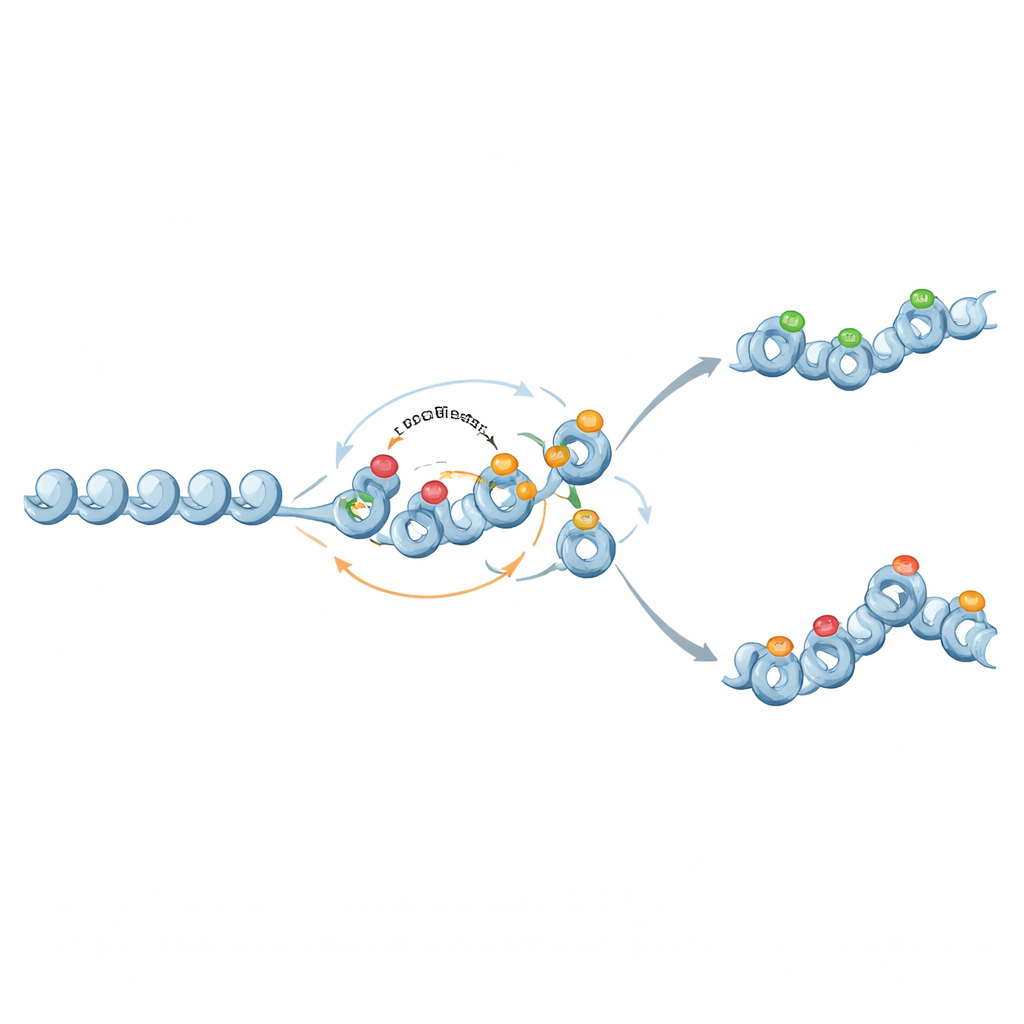
De Chaves Binárias a Memórias Graduais
Curiosamente, os mesmos componentes moleculares também podem suportar memórias mais sutis e analógicas. Quando o feedback de marcas histonas repressivas para a metilação do DNA é enfraquecido e a metilação se torna quase permanente, mas não autoamplificadora, a metilação age como um pano de fundo fixo que define um nível médio de expressão gênica. As marcas histonas então flutuam sobre esse pano de fundo, às vezes produzindo dois estados cromatínicos estáveis e distribuições amplas de expressão em níveis intermediários de metilação. Dessa forma, os circuitos de cromatina podem ajustar tanto o quão estável é a atividade de um gene quanto quão variável sua expressão pode ser entre células.
Por que Esses Modelos Importam para Medicina e Engenharia
Os autores concluem que entender a memória epigenética requer modelar explicitamente o ruído molecular e o tempo dos processos-chave. Sua síntese destaca quais taxas de reação e laços de realimentação controlam com mais força o tempo de residência das células em estados ativos ou reprimidos. Essa visão pode orientar experimentos que alterem a velocidade do ciclo celular, níveis de enzimas ou marcas cromatínicas específicas para testar previsões dos modelos. A longo prazo, tais modelos podem ajudar a projetar células que possam ser reprogramadas de forma confiável, manter um destino desejado ou armazenar informação de maneira controlável — abrindo possibilidades para medicina regenerativa, terapia contra o câncer e respostas imunes programáveis.
Citação: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Palavras-chave: memória epigenética, modificações da cromatina, metilação do DNA, modelagem estocástica, regulação gênica