Clear Sky Science · ar
النمذجة العشوائية للذاكرة اللاجينية
كيف تتذكر الخلايا هويتها
تحمل كل خلية في جسمك تقريبًا نفس الحمض النووي، ومع ذلك تتصرَّف خلية الدماغ بشكل مختلف تمامًا عن خلية الجلد أو الجهاز المناعي. يجب نسخ هذا “الإحساس بالهوية” المستمر في كل مرة تنقسم فيها الخلايا، وعندما يفشل ذلك قد تنشأ أمراض مثل السرطان. يشرح هذا المقال كيف يستخدم الباحثون أدوات رياضية لفهم الذاكرة اللاجينية — العلامات الكيميائية على الحمض النووي وعبوته التي تتيح للخلايا تذكر على المدى الطويل ما إذا كانت جينات معينة ينبغي أن تبقى مفعلة أو مطفأة.
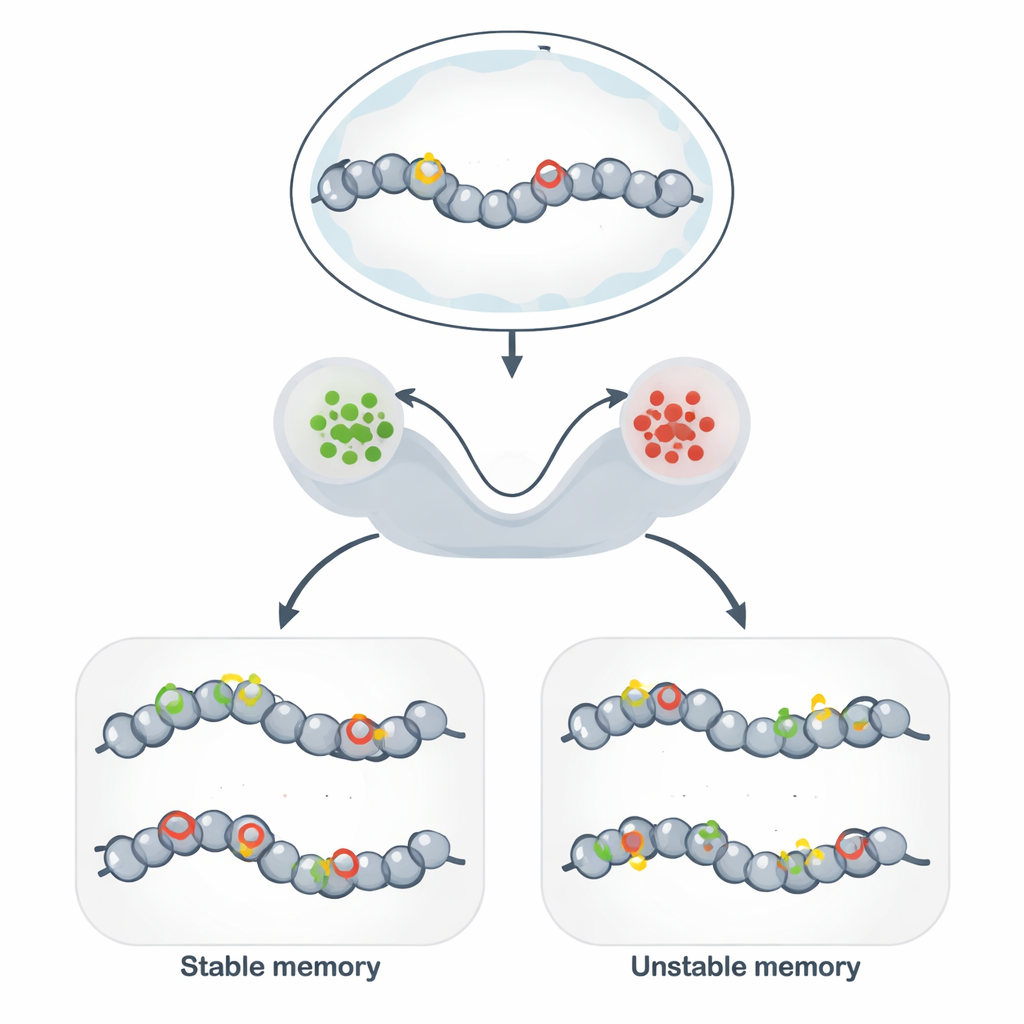
ما بعد DNA: علامات ثابتة على الجينوم
تسمح الذاكرة اللاجينية للخلايا المتطابقة وراثيًا بالحفاظ على سلوكيات مختلفة ومستقرة عبر العديد من انقسامات الخلايا. بدلًا من تغيير تسلسل الـDNA، تُزيّن الخلايا الحمض النووي والبروتينات المحيطة به بعلامات كيميائية تُرخّص أو تضيق البنية المحلية. عندما تُفضل العلامات بنية مفتوحة، تميل الجينات القريبة إلى النشاط؛ وعندما تُفضّل بنية مضغوطة، تُسكت الجينات. يستند هذا الميكانيزم إلى هوية نوع الخلية، واستمرار الاستجابات المناعية، وبعض أشكال الذاكرة الدماغية، وأدوات واعدة في البيولوجيا التركيبية التي تهدف إلى «برمجة» حالات خلوية مستقرة.
لماذا لا يمكن تجاهل العشوائية
على المقياس الجزيئي، الخلية مكان صاخب: الجزيئات الأساسية غالبًا ما توجد بأعداد قليلة وتتصادف عشوائيًا. النماذج التقليدية التي تستخدم منحنيات ناعمة لوصف كيف يتغير نشاط الجين مع الزمن يمكن أن تتنبأ بحالات مستقرة متعددة، مثل واديتين مفصولتين بتلّة. في مثل هذه النماذج، بمجرد أن يتدحرج النظام إلى وادٍ فإنه من المفترض أن يبقى هناك إلى الأبد. لكن في الواقع، يمكن للأحداث الجزيئية العشوائية أحيانًا أن تدفع النظام عبر التل إلى وادٍ آخر. يقدم المقال أطرًا عشوائية (احتمالية) تتعامل مع التفاعلات كأحداث عشوائية وتقيس عدد مرات حدوث مثل هذه التحولات، على سبيل المثال عبر أزمنة العبور الأول المتوسط التي تقيس كم يدوم وضع ما عادة قبل أن يحفزه الضجيج على القفز.
عدسات رياضية على الفوضى الجزيئية
يصف الاستعراض طريقتين رئيسيتين لنمذجة هذه العشوائية. شبكات التفاعلات الكيميائية العشوائية تتتبع أعداد الجزيئات بدقة وتعامل النظام كعملية ماركوفية، حيث يحدث كل تفاعل باحتمال يعتمد على الحالة الحالية. يمكن لهذا النهج أن يلتقط بدقة التحولات النادرة بين حالات التعبير الجيني المستقرة لكنه مكلف حسابيًا. فئة ثانية من النماذج تستخدم معادلات تفاضلية عشوائية، التي تقرب أعداد الجزيئات ككميات مستمرة مهزوزة بضوضاء غاوسية. تنويعات مثل معادلة لانجفين الكيميائية ومقاربة الضوضاء الخطية تتنازل عن بعض الدقة لصالح وضوح تحليلي، مما يسمح للباحثين باستنتاج كيف تشكّل معلمات النظام التقلبات حول حالة مستقرة ومدى احتمال التحولات بين الحالات.
دوائر الكروماتين كعتاد للذاكرة
لربط هذه النماذج المجردة بالبيولوجيا، يركّز المؤلفون على دوائر تعديل الكروماتين: شبكات من العلامات الكيميائية على بروتينات الهيستون والحمض النووي التي تعزز بعضها بعضًا. يمكن لعلامات الهستون التي تعزّز الكروماتين النشط وتلك التي تعزّز الكروماتين المكبوت أن تجتذب إنزيمات تنشر نفس العلامة إلى المواقع المجاورة، مكونة تغذية راجعة إيجابية قوية. تُظهر النماذج العشوائية أنه عندما تكون هذه التعزيزات الذاتية سريعة مقارنةً بمسح العلامات، يتطور النظام إلى حالتين طويلتي الأمد — عموماً «مفعّل» و«مطفأ» — تعملان كذاكرة ثنائية. إضافة مثيلة الـDNA، وهي علامة مستقرة للغاية تُنسخ أثناء تضاعف الحمض النووي، تميل أكثر بالنظام نحو الكبت طويل الأمد ويمكن أن تطيل بشكل كبير مدة استمرار الحالة المُسكتَة.
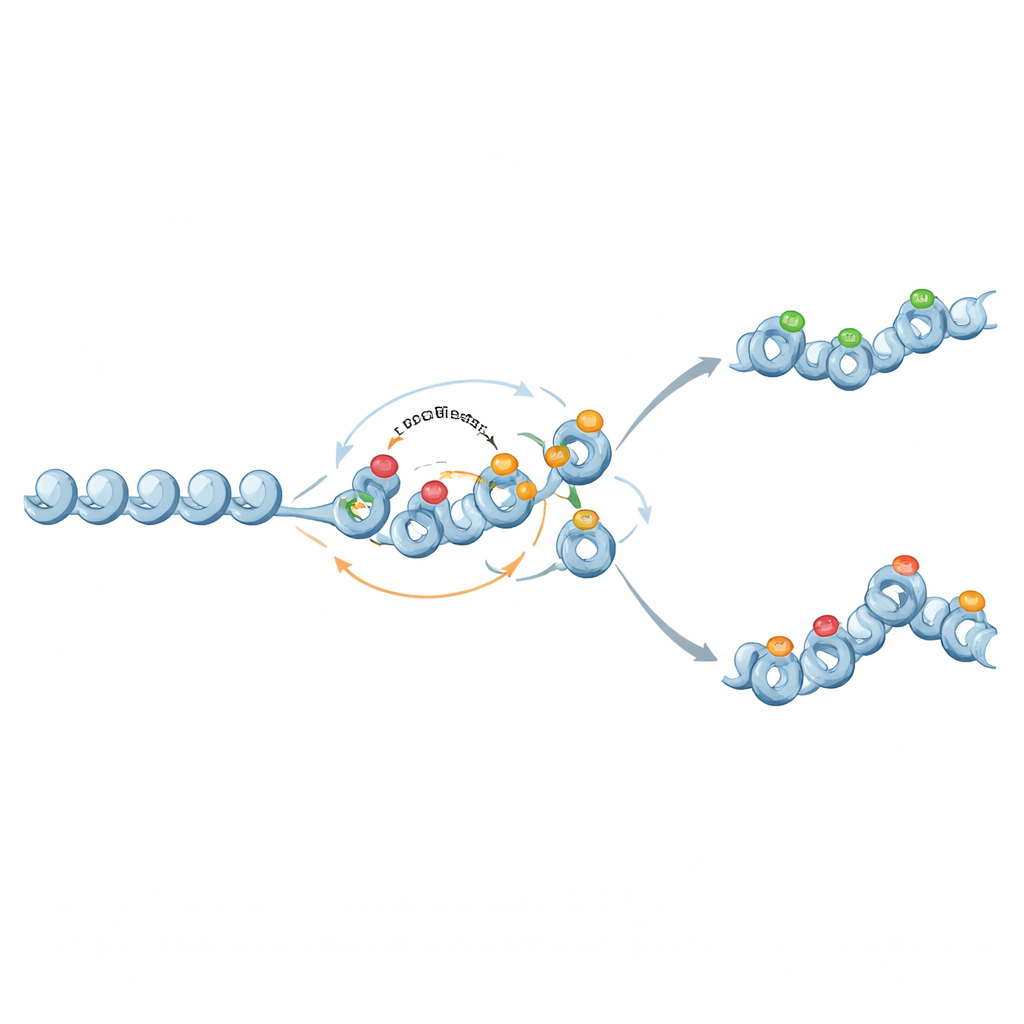
من مفاتيح ثنائية إلى ذكريات متدرجة
من المثير للاهتمام أن نفس اللاعبين الجزيئيين يمكنهم أيضًا دعم ذاكرة أكثر دقة وتماثلية. عندما تضعف التغذية الراجعة من علامات الهستون القمعية إلى مثيلة الـDNA وتصبح المثيلة شبه دائمة لكنها لا تعزز نفسها تلقائيًا، تعمل المثيلة كخلفية ثابتة تحدد مستوى تعبير جيني متوسطًا. ثم تتقلب علامات الهستون فوق هذه الخلفية، منتجة أحيانًا حالتين كروماتينيتين مستقرتين وتوزيعات تعبير واسعة عند مستويات مثيلة متوسطة. بهذه الطريقة، يمكن لدوائر الكروماتين ضبط مدى استقرار نشاط الجين ومدى تباين التعبير عنه عبر الخلايا.
لماذا تهم هذه النماذج للطب والتصميم
يخلص المؤلفون إلى أن فهم الذاكرة اللاجينية يتطلب نمذجة الضجيج الجزيئي و توقيت العمليات الرئيسية صراحةً. يبرز تركيبهم أي معدلات تفاعل ودوائر تغذية راجعة تتحكم بقوة في زمن بقاء الخلايا في حالات مفعلة أو مكبوتة. يمكن أن توجه هذه الأفكار تجارب تغير سرعة دورة الخلية أو مستويات الإنزيمات أو علامات كروماتينية محددة لاختبار تنبؤات النماذج. على المدى الطويل، قد تساعد هذه النماذج في هندسة خلايا يمكن إعادة برمجتها بشكل موثوق، أو تحتفظ بمصير مرغوب أو تخزن معلومات بطريقة قابلة للتحكم — فاتحة إمكانيات للطب التجديدي، وعلاج السرطان، واستجابات مناعية قابلة للبرمجة.
الاستشهاد: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
الكلمات المفتاحية: الذاكرة اللاجينية, تعديلات الكروماتين, مثيلة الحمض النووي, النمذجة العشوائية, تنظيم الجينات