Clear Sky Science · ru
Стохастическое моделирование эпигенетической памяти
Как клетки помнят, кем они являются
В каждой клетке вашего тела по сути одинаковая ДНК, однако нервная клетка ведёт себя совершенно иначе, чем клетка кожи или иммунная клетка. Это длительное «чувство идентичности» нужно копировать при каждом делении клеток, и когда этот процесс нарушается, могут возникать болезни, такие как рак. В статье объясняется, как исследователи используют математические инструменты для понимания эпигенетической памяти — биохимических меток на ДНК и её упаковке, которые позволяют клеткам надолго запоминать, должны ли конкретные гены оставаться включёнными или выключенными.
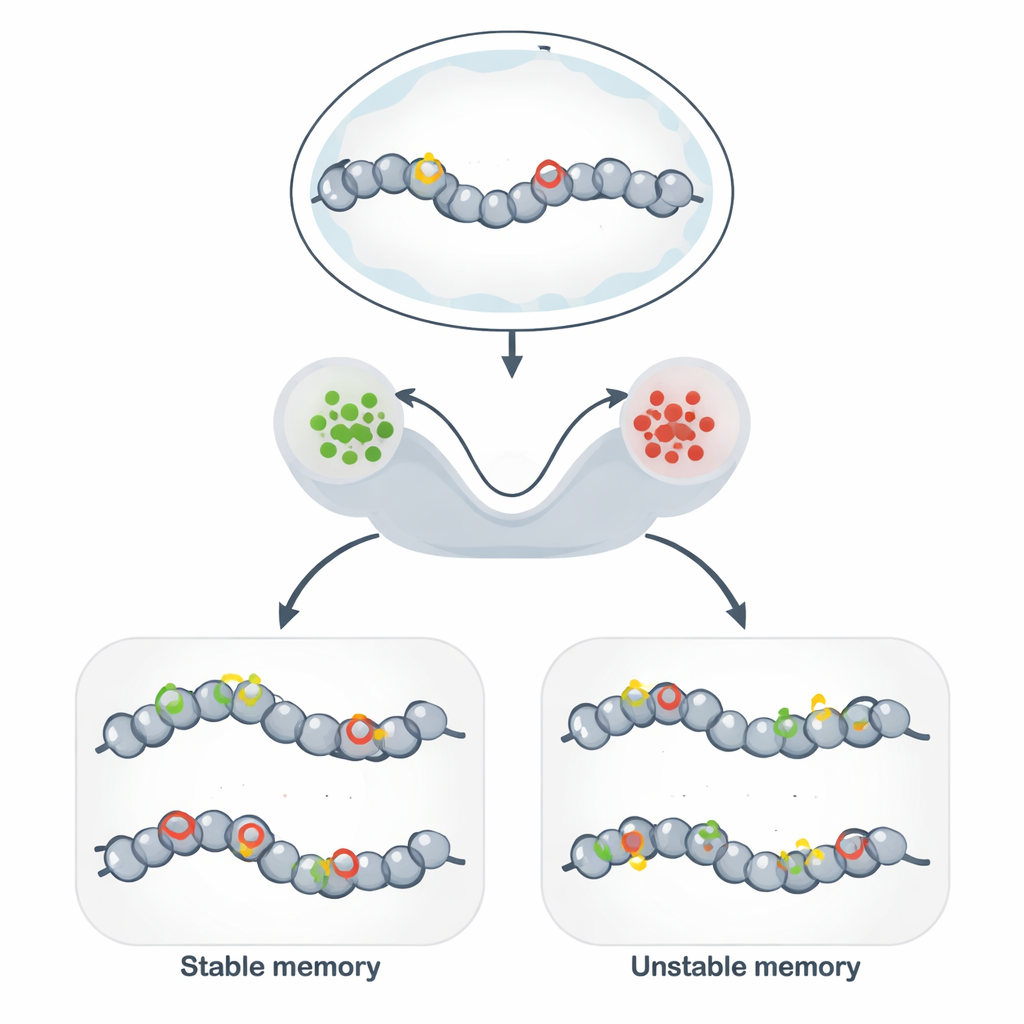
Вне ДНК: стабильные метки на геноме
Эпигенетическая память позволяет генетически идентичным клеткам поддерживать разные устойчивые поведения на протяжении многих делений. Вместо изменения последовательности ДНК клетки украшают ДНК и окружающие белки химическими метками, которые ослабляют или уплотняют локальную структуру. Когда метки способствуют открытой структуре, соседние гены, как правило, активны; когда метки приводят к компактной структуре, гены подавляются. Этот механизм лежит в основе клеточной идентичности, сохранения иммунных ответов, некоторых форм памяти мозга и потенциальных инструментов синтетической биологии, нацеленных на «программирование» стабильных состояний клеток.
Почему случайность нельзя игнорировать
На молекулярном уровне в клетке царит шум: ключевые молекулы часто присутствуют в небольших количествах и сталкиваются друг с другом случайным образом. Традиционные модели, которые используют плавные кривые для описания изменения активности генов со временем, могут предсказывать несколько устойчивых состояний, подобно двум долинам, разделённым холмом. В таких моделях, оказавшись в долине, система должна оставаться там навсегда. Но в реальности случайные молекулярные события иногда могут подтолкнуть систему через холм в другую долину. В статье представлены стохастические (вероятностные) подходы, которые рассматривают реакции как случайные события и количественно оценивают, как часто происходят такие переключения — например, через среднее время первого прохождения, измеряющее, как долго состояние обычно сохраняется до того, как шум вызовет переход.
Математические линзы на молекулярный хаос
Обзор описывает два основных подхода к моделированию этой случайности. Стохастические сети химических реакций отслеживают точные количества молекул и рассматривают систему как марковский процесс, в котором каждая реакция происходит с вероятностью, зависящей от текущего состояния. Этот подход достоверно захватывает редкие переключения между устойчивыми состояниями экспрессии генов, но вычислительно затратен. Второй класс моделей использует стохастические дифференциальные уравнения, которые аппроксимируют количества молекул как непрерывные величины, подверженные гауссовскому шуму. Варианты, такие как химическое уравнение Ланжевена и приближение линейного шума, жертвуют частью точности ради аналитической ясности, позволяя исследователям вывести, как параметры системы формируют флуктуации вокруг устойчивого состояния и какова вероятность переходов между состояниями.
Цепи хроматина как аппарат памяти
Чтобы связать эти абстрактные модели с биологией, авторы фокусируются на схемах модификаций хроматина: сетях химических меток на гистонах и ДНК, которые усиливают друг друга. Модификации гистонов, способствующие открытой хроматиновой структуре, и те, что способствуют репрессии, могут привлекать ферменты, распространяющие ту же метку на соседние участки, создавая мощную положительную обратную связь. Стохастические модели показывают, что когда такое самоукрепление происходит быстрее стирания меток, система формирует два долгоживущих состояния — в широком смысле «ВКЛ» и «ВЫКЛ» — которые функционируют как бинарная память. Добавление метилирования ДНК, очень стабильной метки, копируемой во время репликации ДНК, дополнительно смещает систему в сторону длительной репрессии и может существенно увеличивать срок сохранения подавленного состояния.
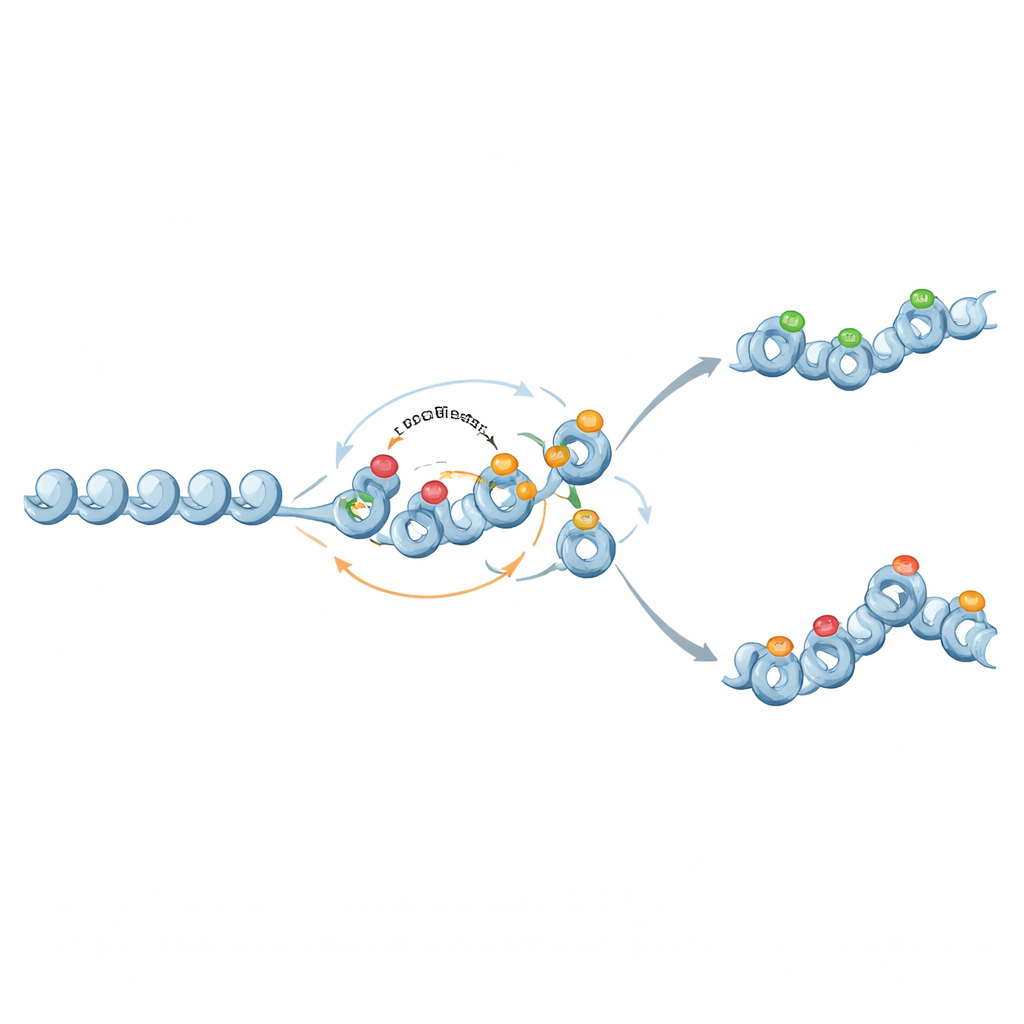
От бинарных переключателей к градуированным запоминаниям
Интересно, что те же молекулярные компоненты также могут поддерживать более тонкую, аналоговую память. Когда обратная связь от репрессивных меток гистонов к метилированию ДНК ослаблена, а метилирование становится почти постоянным, но не самоусиливающимся, метилирование выступает как фиксированный фон, задающий средний уровень экспрессии гена. Гистоновые метки тогда флуктуируют на этом фоне, иногда создавая два устойчивых состояния хроматина и широкие распределения экспрессии при промежуточных уровнях метилирования. Таким образом, схемы хроматиновых модификаций могут настраивать как стабильность активности гена, так и вариабельность его экспрессии между клетками.
Почему эти модели важны для медицины и инженерии
Авторы приходят к выводу, что понимание эпигенетической памяти требует явного моделирования молекулярного шума и временных характеристик ключевых процессов. Их синтез выделяет, какие скорости реакций и петли обратной связи сильнее всего контролируют время пребывания клеток в активном или репрессированном состоянии. Это понимание может направлять эксперименты, меняющие скорость клеточного цикла, уровни ферментов или конкретные хроматиновые метки для проверки предсказаний моделей. В долгосрочной перспективе такие модели могут помочь проектировать клетки, которые можно надёжно перепрограммировать, удерживать в желаемом состоянии или использовать для хранения информации управляемым образом — открывая возможности для регенеративной медицины, терапии рака и программируемых иммунных ответов.
Цитирование: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Ключевые слова: эпигенетическая память, модификации хроматина, метилирование ДНК, стохастическое моделирование, регуляция генов