Clear Sky Science · he
מִידוּל סטוכסטי של זיכרון אפיגנטי
איך תאים זוכרים מי הם
לכל תא בגופך יש במידה רבה את אותו DNA, אך תא מוח מתנהג באופן שונה לחלוטין מתא עור או תאי מערכת החיסון. ה"תחושת זהות" הקבועה הזו חייבת להיות מועתקת בכל חלוקת תא, וכאשר ההעתקה נכשלת עלולות להיווצר מחלות כמו סרטן. מאמר זה מסביר כיצד חוקרים משתמשים בכלים מתמטיים כדי להבין זיכרון אפיגנטי — הסימנים הביוכימיים על ה‑DNA ועל האריזה שלו שמאפשרים לתאים לזכור בטווח הארוך האם גנים מסוימים צריכים להישאר דלוקים או כבויים.
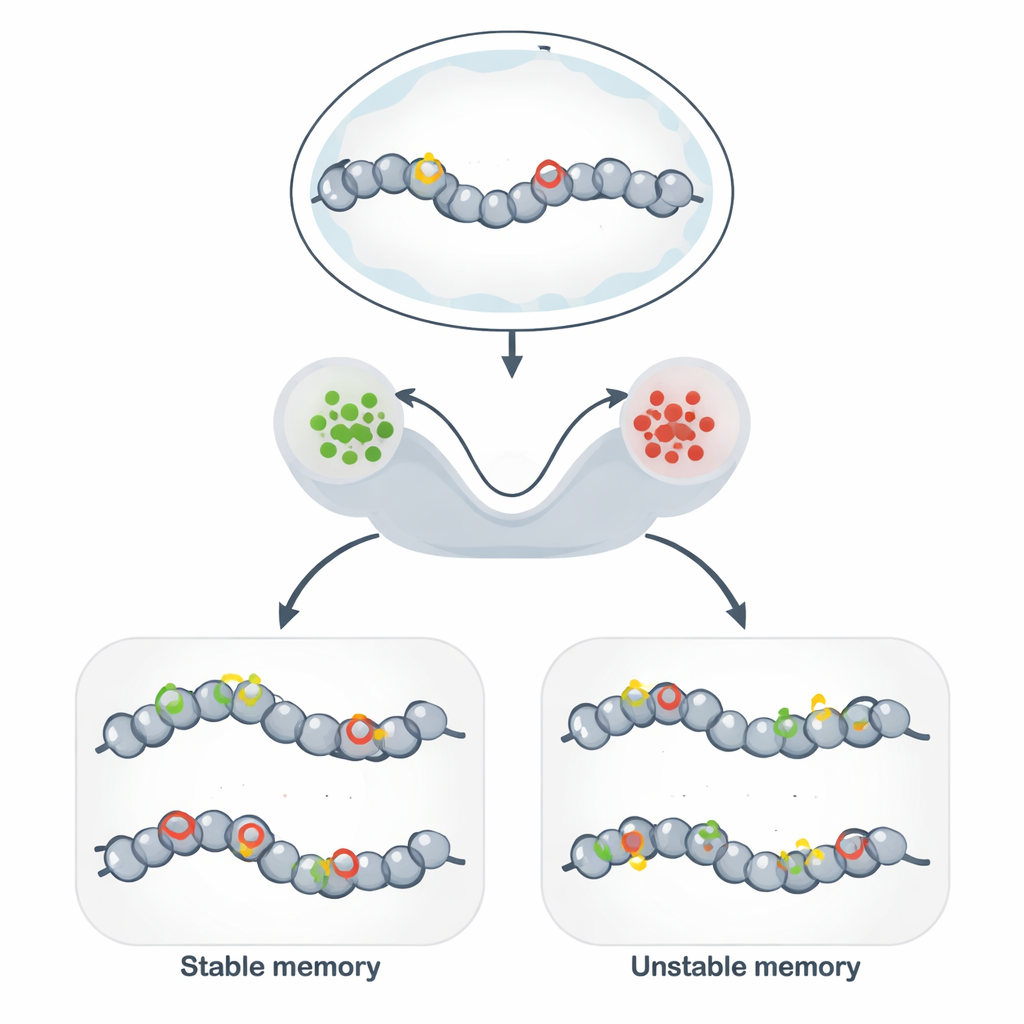
מעבר ל‑DNA: סימנים יציבים על הגנום
הזיכרון האפיגנטי מאפשר לתאים זהים גנטית לשמר התנהגויות שונות ויציבות לאורך חלוקות תא רבות. במקום לשנות את רצף ה‑DNA, תאים מקשטים את ה‑DNA ואת החלבונים שמסביבו בתגיות כימיות שמרפות או מהדקות את המבנה המקומי. כאשר התגיות תומכות במבנה פתוח, גנים סמוכים נוטים להיות פעילים; כאשר התגיות מקדמות מבנה דחוס, הגנים מושתקים. מנגנון זה עומד מאחורי זהות סוג התא, המשכיות תגובות חיסוניות, צורות מסוימות של זיכרון מוחי וכלים מבטיחים לביולוגיה סינתטית שמטרתם "לְתַכנת" מצבי תא יציבים.
למה אי־סדר סטוכסטי אינו ניתן להתעלמות
בקנה מידה מולקולרי, התא הוא מקום רועש: מולקולות מפתח לרוב קיימות במספרים קטנים ומתנגשׂות זו בזו באקראי. מודלים מסורתיים שמשתמשים בעקומות חלקות כדי לתאר כיצד פעילות גן משתנה עם הזמן יכולים לחזות מצבים יציבים מרובים, כמו שתי ואדיות המופרדות על ידי גבעה. במודלים כאלה, ברגע שהמערכת מתגלגלת לתוך ואדיה היא אמורה להישאר שם לנצח. אך במציאות, אירועים מולקולריים אקראיים עלולים מעת לעת לדחוף את המערכת מעל הגבעה אל ואדיה אחרת. המאמר מציג מסגרות סטוכסטיות (הסתברותיות) שמתייחסות לתגובות כאירועים אקראיים ומכמתות כמה פעמים מתרחשים מעברים כאלה, למשל באמצעות זמני מעבר ממוצעים ראשונים שמודדים כמה זמן מצב נמשך בדרך‑כלל לפני שהרעש מעורר קפיצה.
עדשות מתמטיות על הכאוס המולקולרי
הסקירה מתארת שתי דרכים עיקריות למידול הרעש הזה. רשתות תגובות כימיות סטוכסטיות עוקבות אחרי מספרי המולקולות המדויקים ומתייחסות למערכת כתהליך מארקובי, שבו כל תגובה מתרחשת עם הסתברות התלוית במצב הנוכחי. גישה זו יכולה ללכוד באופן נאמן מעברים נדירים בין מצבי ביטוי גנים יציבים אך כבדה מבחינה חישובית. מחלקה שנייה של מודלים משתמשת במשוואות דיפרנציאליות סטוכסטיות, שמקרבות את ספירות המולקולות ככמויות רציפות המטלטלות על ידי רעש גאוסי. וריאנטים כגון משוואת לנגוואן הכימית וקירוב רעש ליניארי מקריבים מעט דיוק בעד בהירות אנליטית, ומאפשרים לחוקרים לגזור כיצד פרמטרי המערכת מעצבים את התנודות סביב מצב יציב וכמה סבירים המעברים בין מצבים.
מעגלי כרומטין כחומרת זיכרון
כדי לקשר את המודלים המופשטים לביולוגיה, המחברים מתמקדים במעגלי מודיפיקציית כרומטין: רשתות של סימנים כימיים על חלבוני היסטון וה‑DNA שמחזקים זה את זה. תגיות היסטון המקדמות כרומטין פעיל ותגיות המקדמות כרומטין מושתק יכולות כל אחת לשאוב אנזימים שמפיצים את אותה תגית לאתרים שכנים, ויוצרות משוב חיובי חזק. מודלים סטוכסטיים מראים שכאשר ההגברה העצמית הזו מהירה יחסית למחיקה, המערכת מפתחת שני מצבים ארוכי‑טווח — במובן הרחב "דלוק" ו"כבוי" — הפועלים כמערכת זיכרון בינארית. הוספת מתילציה של DNA, תג יציב מאד שמיועתק במהלך שכפול ה‑DNA, משאירה עוד נטייה לדיכוי ארוך‑טווח ועלולה להאריך באופן דרמטי את משך קיום המצב המשׂתק.
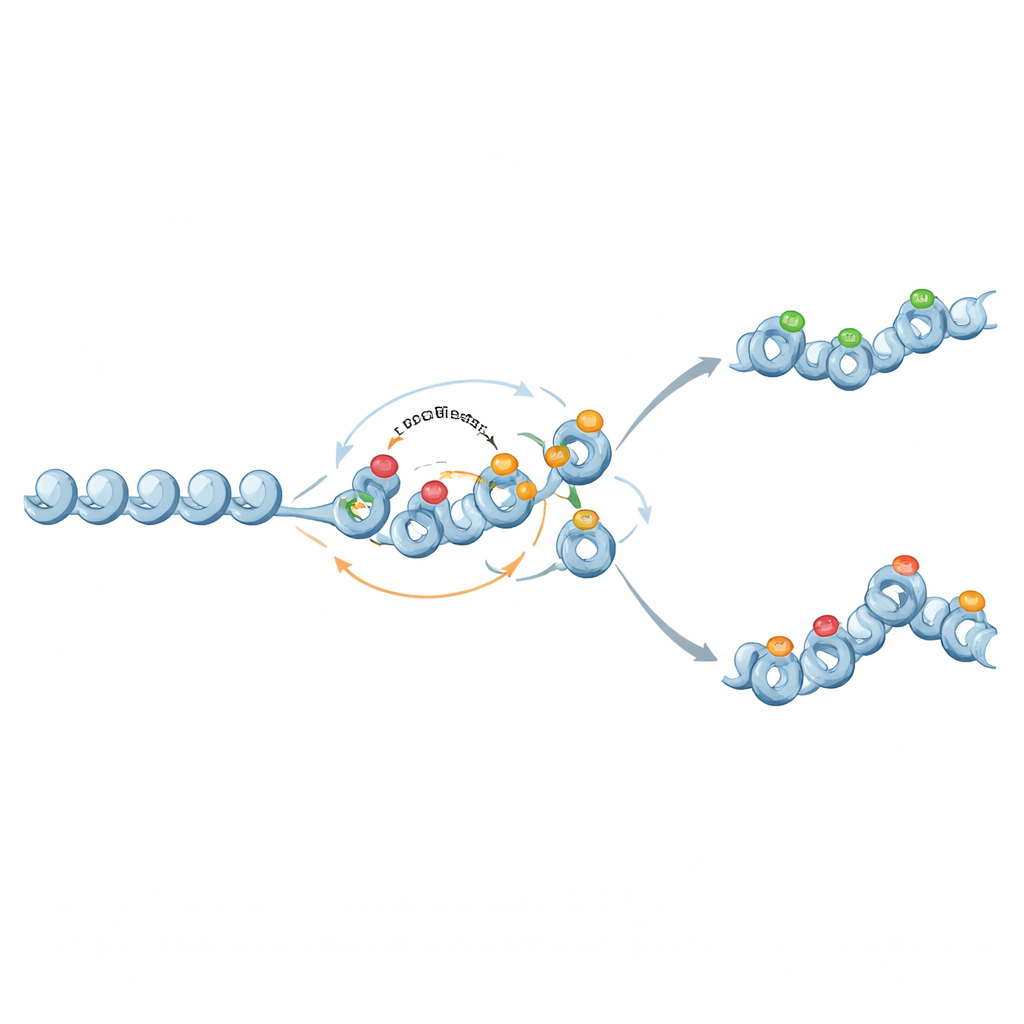
ממתגים בינאריים לזכרונות מדורגים
באופן מעניין, אותן שחקניות מולקולריות יכולות גם לתמוך בזיכרון יותר גוני, אנלוגי. כאשר המשוב מתגובות היסטון מדכאות למתילציה של DNA מוחלש והמתילציה נעשית כמעט קבועה אך לא מחזקת את עצמה, המתילציה פועלת כרקע קבוע שמכוון את רמת הביטוי הממוצעת של גן. תגיות היסטון אז מתנדנדות מעל הרקע הזה, ולפעמים מייצרות שני מצבי כרומטין יציבים והתפלגויות ביטוי רחבות ברמות מתילציה בינוניות. כך, מעגלי כרומטין יכולים לכוונן גם כמה יציבה פעילות גן תהיה וגם כמה שונה יכולה להיות ביטויו בתאים שונים.
מדוע המודלים הללו חשובים לרפואה ולעיצוב
המחברים מסכמים שהבנת זיכרון אפיגנטי דורשת מיפוי מפורש של רעש מולקולרי ותזמון של תהליכים מרכזיים. הסינתזה שלהם מדגישה אילו קצבי תגובה ומשובי משוב משפיעים ביותר על משך המגורים של תאים במצבים פעילים או מושתקים. תובנה זו יכולה להנחות ניסויים שמשנים את קצב מחזור החיים של התא, רמות אנזימים או תגי כרומטין מסוימים כדי לבחון תחזיות מודליות. בטווח הארוך, מודלים כאלה עשויים לסייע לעצב תאים שניתן לשנות באמינות, להחזיק גורל רצוי או לאחסן מידע באופן ישלט — ולפתוח אפשרויות לרפואה מתחדשת, טיפולים בסרטן ותגובות חיסוניות ניתנות לתכנות.
ציטוט: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
מילות מפתח: זיכרון אפיגנטי, שינויים בכרומטין, מתילציה של DNA, מִידוּל סטוכסטי, ויסות גנים