Clear Sky Science · pl
Modelowanie stochastyczne pamięci epigenetycznej
Jak komórki pamiętają, kim są
Każda komórka w twoim ciele nosi zasadniczo tę samą sekwencję DNA, a jednak komórka mózgowa zachowuje się zupełnie inaczej niż komórka skóry czy układu odpornościowego. To trwałe „poczucie tożsamości” musi być kopiowane przy każdym podziale komórki, a gdy zawodzi, mogą pojawić się choroby, takie jak rak. Artykuł wyjaśnia, jak naukowcy używają narzędzi matematycznych do zrozumienia pamięci epigenetycznej — biochemicznych znaków na DNA i jego opakowaniu, które pozwalają komórkom długo pamiętać, czy konkretne geny powinny być włączone czy wyciszone.
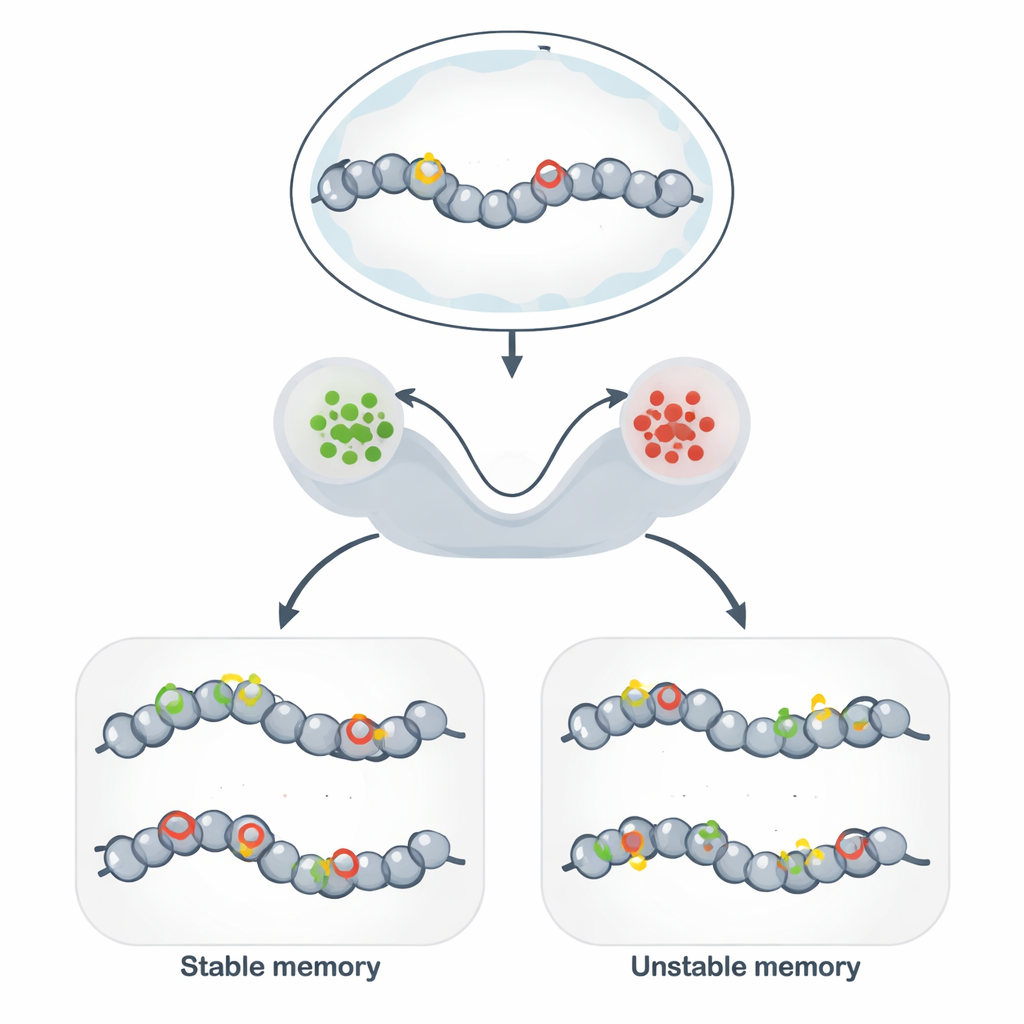
Poniżej DNA: stabilne znaki na genomie
Pamięć epigenetyczna pozwala genetycznie identycznym komórkom utrzymywać różne, stabilne zachowania przez wiele podziałów komórkowych. Zamiast zmieniać sekwencję DNA, komórki dekorują DNA i otaczające je białka chemicznymi etykietami, które poluzowują lub zaciskają lokalną strukturę. Gdy oznaczenia sprzyjają otwartej strukturze, pobliskie geny zwykle są aktywne; gdy sprzyjają zwartej strukturze, geny są wyciszane. Mechanizm ten leży u podstaw tożsamości typów komórek, utrzymywania odpowiedzi odpornościowych, niektórych form pamięci mózgowej oraz obiecujących narzędzi biologii syntetycznej, które mają „zaprogramować” stabilne stany komórek.
Dlaczego przypadkowości nie można ignorować
Na skali molekularnej komórka jest hałaśliwym środowiskiem: kluczowe cząsteczki często występują w niewielkiej liczbie i zderzają się ze sobą losowo. Tradycyjne modele używające gładkich krzywych do opisu zmiany aktywności genów w czasie mogą przewidywać wiele stanów stabilnych, jak dwie doliny oddzielone wzgórzem. W takich modelach, gdy system wpadnie do doliny, powinien tam pozostać na zawsze. W rzeczywistości jednak losowe zdarzenia molekularne mogą od czasu do czasu przepchnąć system przez wzgórze do innej doliny. Artykuł przedstawia stochastyczne (probabilistyczne) ramy, które traktują reakcje jako zdarzenia losowe i kwantyfikują, jak często zachodzą takie przejścia — na przykład przez średnie czasy pierwszego przekroczenia, które mierzą, jak długo stan zwykle trwa, zanim szum wywoła skok.
Matematyczne soczewki na molekularny chaos
Przegląd opisuje dwa główne sposoby modelowania tej przypadkowości. Stochastyczne sieci reakcji chemicznych śledzą dokładne liczby cząsteczek i traktują system jako proces Markowa, w którym każda reakcja zachodzi z prawdopodobieństwem zależnym od bieżącego stanu. Podejście to wiernie odwzorowuje rzadkie przeskoki między stabilnymi stanami ekspresji genów, ale jest obliczeniowo kosztowne. Druga klasa modeli wykorzystuje stochastyczne równania różniczkowe, które aproksymują liczby cząsteczek jako wielkości ciągłe poddane fluktuacjom z gaussowskim szumem. Warianty, takie jak chemiczne równanie Langevina i przybliżenie liniowego szumu, kosztem części dokładności zyskują jasność analityczną, pozwalając badaczom wyprowadzać, jak parametry systemu kształtują fluktuacje wokół stanu stabilnego i jak prawdopodobne stają się przejścia między stanami.
Obwody chromatynowe jako sprzęt pamięci
Aby powiązać te abstrakcyjne modele z biologią, autorzy koncentrują się na układach modyfikacji chromatyny: sieciach chemicznych znaków na histonach i DNA, które wzajemnie się wzmacniają. Modyfikacje histonów promujące aktywną chromatynę oraz te promujące jej represję mogą rekrutować enzymy, które rozsiewają ten sam znak na sąsiednich miejscach, tworząc silne sprzężenie dodatnie. Modele stochastyczne pokazują, że gdy to samowzmacnianie jest szybkie w porównaniu z procesami kasowania, system rozwija dwa długotrwałe stany — w przybliżeniu „WŁ.” i „WYŁ.” — które działają jak pamięć binarna. Dodanie metylacji DNA, bardzo stabilnego znaku kopiowanego podczas replikacji DNA, dodatkowo przesuwa system w stronę długotrwałej represji i może dramatycznie wydłużyć czas trwania stanu wyciszonego.
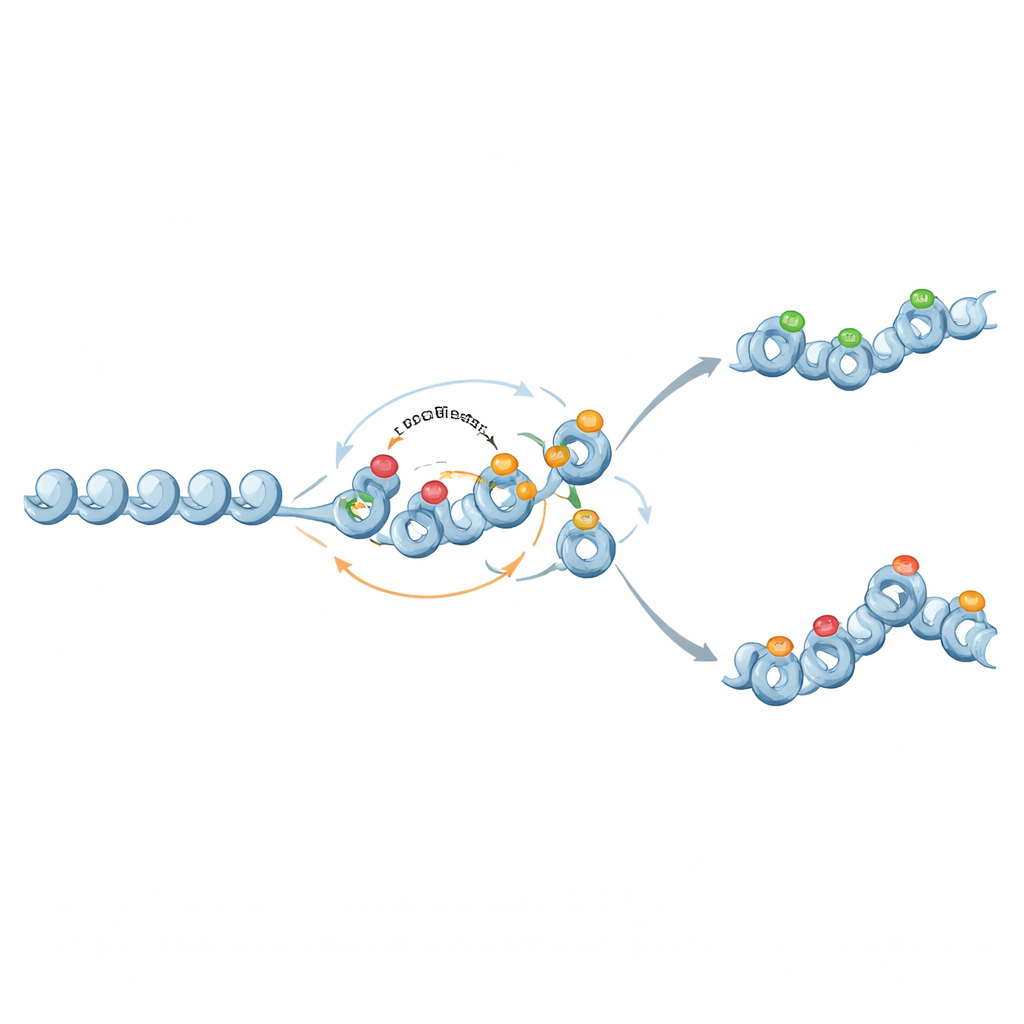
Od przełączników binarnych do stopniowanych pamięci
Ciekawie, ci sami gracze molekularni mogą także wspierać bardziej zniuansowaną, analogową pamięć. Gdy sprzężenie zwrotne z represyjnych znaków histonowych do metylacji DNA jest osłabione, a metylacja staje się niemal trwała, ale nie samo-wzmacniająca, metylacja działa jako stałe tło ustawiające średni poziom ekspresji genu. Znaki histonowe wtedy fluktuują na tym tle, czasem tworząc dwa stabilne stany chromatyny i szerokie rozkłady ekspresji przy pośrednich poziomach metylacji. W ten sposób obwody chromatynowe mogą dostrajać zarówno stabilność aktywności genu, jak i zmienność jego ekspresji w populacji komórek.
Dlaczego te modele mają znaczenie dla medycyny i projektowania
Autorzy konkludują, że zrozumienie pamięci epigenetycznej wymaga jawnego modelowania molekularnego szumu i czasowania kluczowych procesów. Ich synteza wskazuje, które szybkości reakcji i pętle sprzężenia zwrotnego najsilniej kontrolują czas przebywania komórek w stanach aktywnych lub represyjnych. Ta wiedza może ukierunkować eksperymenty zmieniające tempo cyklu komórkowego, poziomy enzymów lub konkretne znaki chromatynowe, aby przetestować przewidywania modeli. W dłuższej perspektywie takie modele mogą pomóc projektować komórki, które można niezawodnie przeprogramować, utrzymać pożądaną losowość lub przechowywać informację w kontrolowalny sposób — otwierając możliwości dla medycyny regeneracyjnej, terapii przeciwnowotworowej i programowalnych odpowiedzi odpornościowych.
Cytowanie: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Słowa kluczowe: pamięć epigenetyczna, modyfikacje chromatyny, metylacja DNA, modelowanie stochastyczne, regulacja genów