Clear Sky Science · es
Modelado estocástico de la memoria epigenética
Cómo las células recuerdan quiénes son
Cada célula de tu cuerpo contiene esencialmente el mismo ADN, sin embargo una neurona se comporta de forma muy distinta a una célula de la piel o del sistema inmunitario. Este perdurable “sentido de identidad” debe copiarse cada vez que las células se dividen, y cuando falla pueden surgir enfermedades como el cáncer. Este artículo explica cómo los investigadores usan herramientas matemáticas para comprender la memoria epigenética: las marcas bioquímicas sobre el ADN y su empaquetamiento que permiten a las células recordar a largo plazo si genes concretos deben permanecer activos o silenciados.
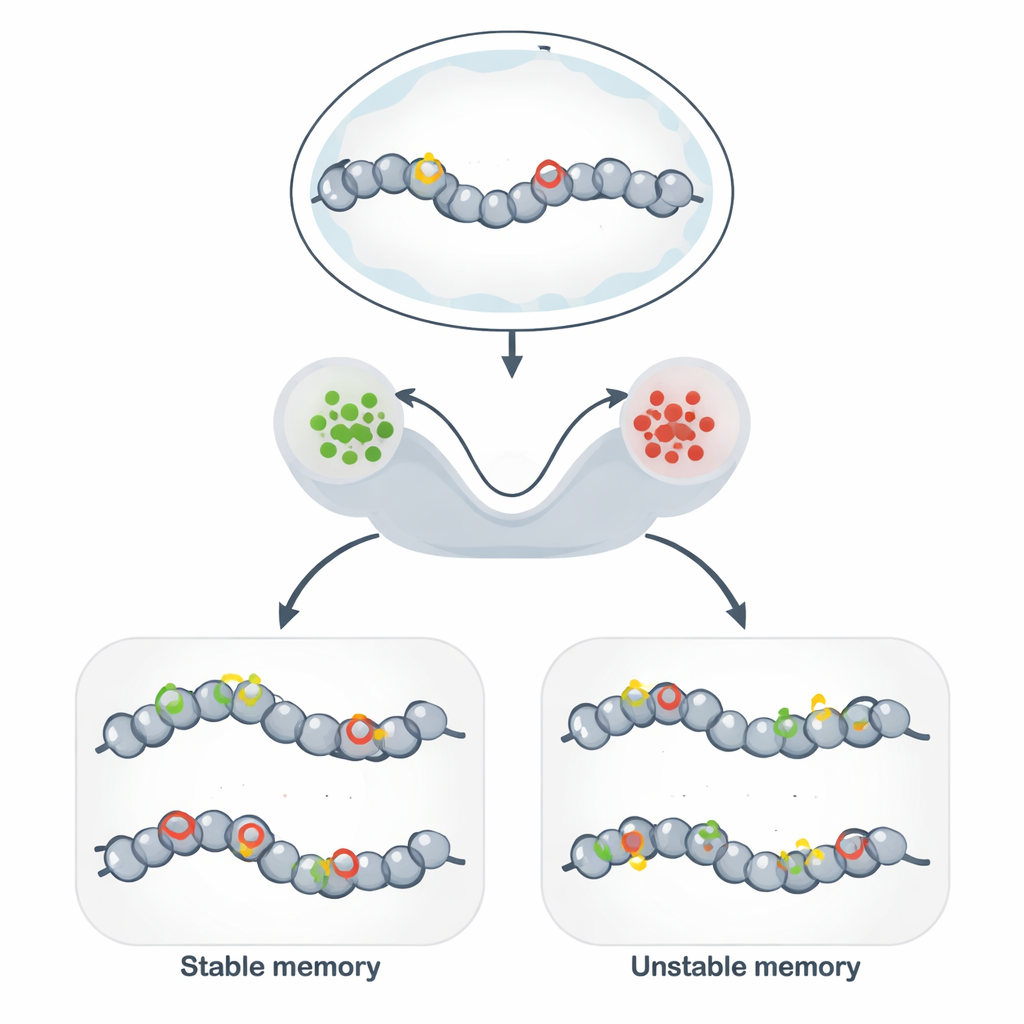
Más allá del ADN: marcas estables en el genoma
La memoria epigenética permite que células genéticamente idénticas mantengan comportamientos distintos y estables a lo largo de muchas divisiones celulares. En lugar de cambiar la secuencia de ADN, las células decoran el ADN y las proteínas que lo rodean con etiquetas químicas que aflojan o compactan la estructura local. Cuando las marcas favorecen una estructura abierta, los genes cercanos tienden a estar activos; cuando favorecen una estructura compacta, los genes se silencian. Este mecanismo subyace a la identidad de tipo celular, la persistencia de respuestas inmunitarias, algunas formas de memoria cerebral y a herramientas prometedoras de la biología sintética que buscan “programar” estados celulares estables.
Por qué no se puede ignorar la aleatoriedad
A escala molecular, la célula es un lugar ruidoso: las moléculas clave suelen existir en números reducidos y chocan entre sí al azar. Los modelos tradicionales que usan curvas suaves para describir cómo cambia la actividad génica con el tiempo pueden predecir múltiples estados estables, como dos valles separados por una colina. En tales modelos, una vez que el sistema cae en un valle debería permanecer allí para siempre. Pero en la realidad, eventos moleculares aleatorios pueden ocasionalmente empujar el sistema por encima de la colina hacia otro valle. El artículo presenta marcos estocásticos (probabilísticos) que tratan las reacciones como sucesos aleatorios y cuantifican con qué frecuencia ocurren esos cambios, por ejemplo mediante tiempos medios de primer paso que miden cuánto dura típicamente un estado antes de que el ruido provoque una transición.
Lentes matemáticas sobre el caos molecular
La revisión describe dos maneras principales de modelar esta aleatoriedad. Las redes estocásticas de reacciones químicas rastrean recuentos exactos de moléculas y tratan el sistema como un proceso de Markov, donde cada reacción se dispara con una probabilidad que depende del estado presente. Este enfoque puede capturar con fidelidad los cambios raros entre estados estables de expresión génica pero es computacionalmente costoso. Una segunda clase de modelos usa ecuaciones diferenciales estocásticas, que aproximan los recuentos moleculares como cantidades continuas sacudidas por ruido gaussiano. Variantes como la ecuación de Langevin química y la aproximación de ruido lineal sacrifican algo de precisión a cambio de claridad analítica, permitiendo a los investigadores derivar cómo los parámetros del sistema moldean las fluctuaciones alrededor de un estado estable y qué probabilidad tienen las transiciones entre estados.
Los circuitos de cromatina como hardware de memoria
Para conectar estos modelos abstractos con la biología, los autores se centran en circuitos de modificación de la cromatina: redes de marcas químicas en histonas y en el ADN que se refuerzan mutuamente. Las marcas de histonas que promueven cromatina activa y las que promueven cromatina reprimida pueden reclutar enzimas que extienden la misma marca a sitios vecinos, creando una fuerte retroalimentación positiva. Los modelos estocásticos muestran que cuando este auto-refuerzo es rápido en comparación con el borrado, el sistema desarrolla dos estados de larga vida—en términos generales “ENCENDIDO” y “APAGADO”—que funcionan como memoria binaria. Añadir la metilación del ADN, una marca muy estable copiada durante la replicación, sesga aún más el sistema hacia la represión duradera y puede prolongar drásticamente cuánto persiste un estado silenciado.
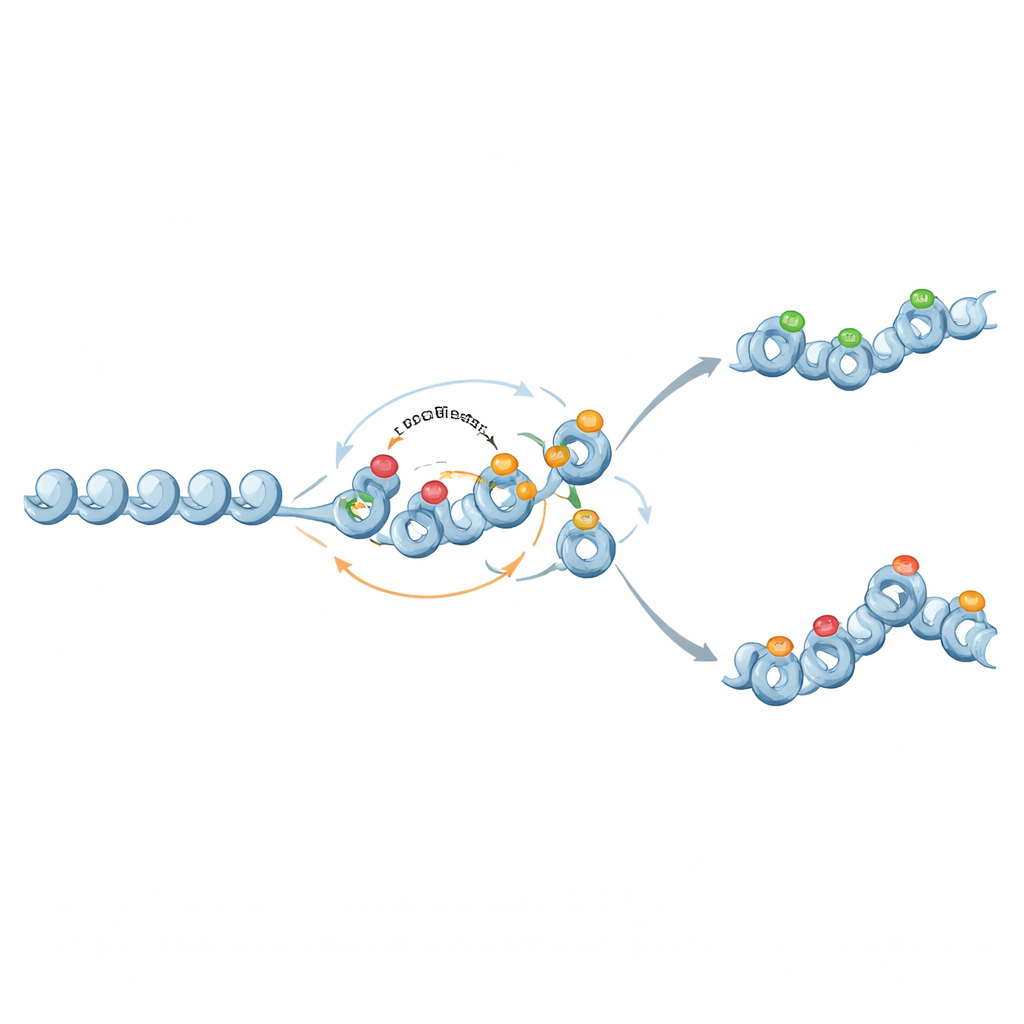
De interruptores binarios a memorias graduadas
Curiosamente, los mismos actores moleculares también pueden sustentar una memoria más matizada y análoga. Cuando la retroalimentación de marcas histónicas represivas hacia la metilación del ADN se debilita y la metilación se vuelve casi permanente pero no autoamplificadora, la metilación actúa como un telón de fondo fijo que fija un nivel medio de expresión génica. Las marcas de histonas fluctúan sobre ese fondo, a veces produciendo dos estados cromatínicos estables y distribuciones amplias de expresión en niveles intermedios de metilación. De este modo, los circuitos de cromatina pueden ajustar tanto cuán estable es la actividad de un gen como cuánta variabilidad de expresión hay entre células.
Por qué estos modelos importan para la medicina y el diseño
Los autores concluyen que entender la memoria epigenética requiere modelar explícitamente el ruido molecular y la sincronización de procesos clave. Su síntesis destaca qué tasas de reacción y bucles de retroalimentación controlan con mayor fuerza el tiempo de residencia de las células en estados activos o reprimidos. Esta perspectiva puede guiar experimentos que alteren la velocidad del ciclo celular, los niveles enzimáticos o marcas cromatínicas específicas para probar predicciones del modelo. A largo plazo, tales modelos pueden ayudar a diseñar células que puedan reprogramarse de forma fiable, mantener un destino deseado o almacenar información de forma controlable—abriendo posibilidades para la medicina regenerativa, terapias contra el cáncer y respuestas inmunitarias programables.
Cita: Bruno, S., Del Vecchio, D. Stochastic modeling of epigenetic memory. npj Syst Biol Appl 12, 58 (2026). https://doi.org/10.1038/s41540-026-00664-9
Palabras clave: memoria epigenética, modificaciones de la cromatina, metilación del ADN, modelado estocástico, regulación génica