Clear Sky Science · tr
PARK19 kırpma mutantı Dnajc6, lizozomal yetmezlik kaynaklı patolojik α-sinüklein artışına ve PARK19 knockin farelerinde substantia nigra dopaminerjik hücrelerin nörodejenerasyonuna neden olur
Bu fare çalışması neden Parkinson hastalığı için önemli
Parkinson hastalığı, beyindeki az sayıdaki dopamin üreten hücreyi yavaşça yok ederek insanların hareket yeteneğini çalar. Olguların çoğu yaş ve çevresel etkenlerin karışımıyla ortaya çıkarken, azınlık tek-gene bağlı bozukluklar hastalık sürecine ilişkin güçlü ipuçları sağlar. Bu çalışma, DNAJC6 adlı tek bir geni inceleyerek, özel olarak tasarlanmış bir fare modelinde hücre içine kadar uzanan küçük bir değişikliğin atık giderme sistemlerini nasıl aksatabileceğini, yapışkan bir protein olan alfa‑sinükleini nasıl biriktirdiğini ve nihayetinde nöron kaybı ile Parkinson benzeri belirtilere nasıl yol açtığını ortaya koyuyor. 
Hücrelerdeki hatalı yardımcı protein
DNAJC6 geni neredeyse yalnızca nöronlarda bulunan bir protein üretir; bu protein, hücre zarlarını şekillendiren ve yeniden kullanan örtü benzeri bir molekül olan klatrini yönetmeye yardımcı olur. PARK19 olarak bilinen erken başlangıçlı bir Parkinson ailesinde, DNAJC6'nın her iki kopyasında da proteinin kritik bir ucunu kesen hasarlı değişiklikler bulunur. Araştırmacılar, bu durumu taklit etmek için CRISPR gen düzenleme kullanarak farelerdeki Dnajc6 geninin eşdeğer bir konumda erken sonlanmasını sağlayan bir model oluşturdular. Bu homozigot “Q787X” fareleri yalnızca kısalmış protein formunu üretirken, heterozigot fareler insan ailelerindeki sağlıklı taşıyıcılara benzer şekilde bir normal bir mutant kopya taşır.
Gen kusurundan hareket sorunlarına
Ekip fareleri yaşlandıkça izledi ve hareket yeteneklerini test etti. Beş aylıkken tüm gruplar normal davrandı. Ancak dokuz aylıkta iki mutant kopyaya sahip fareler klasik Parkinson benzeri motor sorunlar geliştirdi: daha yavaş hareket ettiler, daha kısa mesafe kat ettiler ve bir test direğinden inmek için daha fazla süreye ihtiyaç duydular; bu hastalardaki hipokinezi ve bradikineziyi yansıtıyor. Bilimleri beyinlerini incelediklerinde, substantia nigrada dopamin üreten nöronlarda belirgin bir kayıp ve striatumdaki sinir uçlarında incelme gördüler. Bu hassas nöronlar ayrıca insan Parkinson hastalığında görülen Lewy cisimciği patolojisine benzer şekilde fosforile alfa‑sinüklein kümeleri içeriyordu. Tek mutant kopyaya sahip heterozigot farelerde bu değişikliklerin hiçbiri görülmedi.
Hücresel geri dönüşüm bozulduğunda
Olay zincirini anlamak için yazarlar hücrenin geri dönüşüm merkezlerine: lizozomlara baktı. Mutant farelerin dopamin nöronlarında klatrin ağır zinciri seviyeleri azalmıştı; bu, hücrelerin lizozom havuzunu yenileme biçimi olan otofajik lizozom yeniden oluşum sürecini bozması beklenen bir durumdu. Gerçekten de, lizozom sayısı düştü ve bozulmuş hücresel “kendini yeme” (otofaji) belirteçleri arttı. Hayati önemde bir lizozomal enzim olan katepsin D kritik ölçüde azaldı; buna karşılık alfa‑sinüklein ile onun daha toksik fosforile ve oligomerik formları birikerek sindirime dirençli hale geldi. Bu lizozomal başarısızlık seçiciydi: komşu inhibitör nöronlar aynı bozunmayı göstermedi ve bu da substantia nigra dopamin hücrelerinin özgül savunmasızlığını vurguladı. 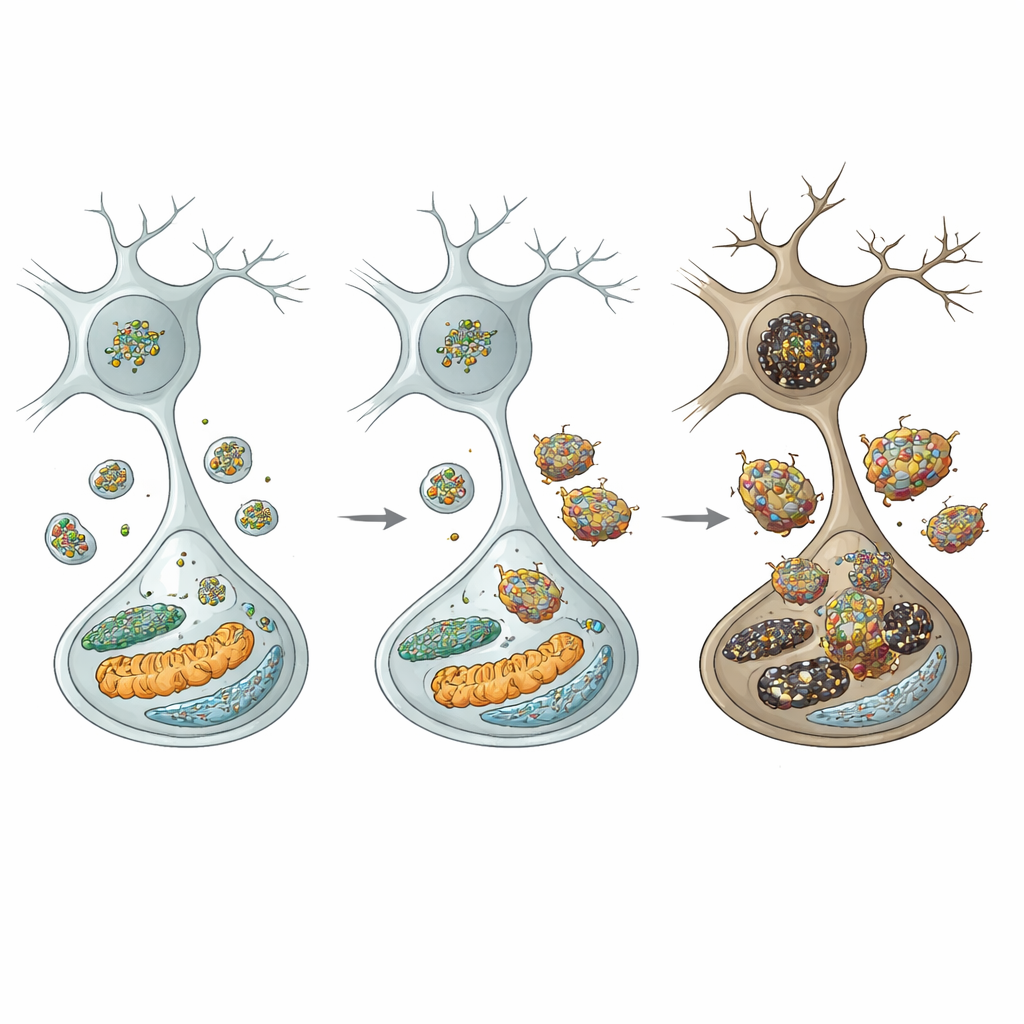
Nöron içinde ve dışında yayılan hasar
Aşırı alfa‑sinüklein yerinde kalmadı. Endoplazmik retikulum ve mitokondri gibi iki hayati iç yapıda birikerek stres ve hasar tetikledi. Endoplazmik retikulumda katlanmamış protein stres yanıtlarını ve hücre ölümünü teşvik eden yolları etkinleştirdi. Mitokondrilerde ise kompleks I aktivitesini azalttı, reaktif oksijen türlerini artırdı ve sitokrom c salınımını teşvik ederek kaspazlar olarak bilinen intihar enzimlerini aktive etti. Aynı zamanda oligomerik alfa‑sinükleinin nöronlardan dışarı sızmış olması muhtemeldi ve yakındaki mikrogliaları, beynin bağışıklık bekçilerini, tahrik etti. Bu mikroglialar pro‑inflamatuar bir duruma geçti, NLRP3 inflammasom kompleksini açtı ve IL‑1β, IL‑18 ve TNF‑α gibi inflamatuar moleküller saldı. Bu sinyaller de sırasıyla dopamin nöronları içinde JNK kaynaklı ve nekroptotik yollar dahil ek ölüm yollarını etkinleştirerek zarar döngüsünü körükledi.
Hücresel temizliği geri getiren bir ilaç
Araştırmacılar, lizozom üretimini artırmanın bu kaskadı kesip kesemeyeceğini sordular. Genin temizleyici anahtarını dolaylı olarak serbest bırakarak TFEB'in çekirdeğe girip lizozom oluşturan genleri açmasını sağlayan ve aynı zamanda otofajiyi uyaran rapamisinle genç mutant fareleri tedavi ettiler. Dört ay sonra rapamisin verilen mutant farelerde substantia nigrada lizozomal belirteçler ve katepsin D seviyeleri düzeldi ve alfa‑sinüklein birikimi çok azaldı. İlginç şekilde, bu fareler substantia nigrada ve yakın ventral tegmental alanda dopamin nöronlarının kaybından büyük ölçüde korundu ve motor performansları normale doğru iyileşti. Hücrenin atık yönetimi ağını yukarıdan hedefleyerek rapamisin, protein birikimi, organel stresi, inflamasyon ve hücre ölümü gibi aşağı doğru ilerleyen kaskadı etkili bir şekilde zayıflattı.
Parkinson’u anlamak ve tedavi etmek için bunun anlamı
Basitçe, bu çalışma nöronlara özgü bir yardımcı proteindeki tek bir kalıtsal kusurun nasıl bir zincirleme reaksiyon başlattığını gösteriyor: daha az lizozom, zayıflamış katepsin D aktivitesi, toksik alfa‑sinüklein seviyelerinde artış, önemli hücresel bölümlerde hasar, aşırı inflamatuar tepki ve nihayetinde Parkinson belirtilerinin temelini oluşturan dopamin nöronlarının kaybı. Bu özel mutasyon nadir olsa da aynı temalar—lizozomal yetmezlik, yetersiz protein temizliği ve alfa‑sinüklein yüklenmesi—daha yaygın, ailesel olmayan Parkinson hastalığında da ortaya çıkıyor. Bu çalışma bu nedenle beynin temizlik sistemlerinin, örneğin TFEB’i aktive eden veya otofajiyi artıran ilaçlar (rapamisin veya daha güvenli türevleri gibi), Parkinson ilişkili nörodejenerasyonu yavaşlatmak veya önlemek için umut verici bir strateji olabileceği fikrini güçlendiriyor.
Atıf: Wang, HL., Chen, YL., Chiu, TJ. et al. PARK19 truncation mutant Dnajc6 causes lysosomal deficiency-induced upregulation of pathologic α-synuclein and neurodegeneration of substantia nigra dopaminergic cells in PARK19 knockin mice. npj Parkinsons Dis. 12, 102 (2026). https://doi.org/10.1038/s41531-026-01317-8
Anahtar kelimeler: Parkinson hastalığı, lizozomlar, alfa-sinüklein, dopaminerjik nöronlar, rapamisin