Clear Sky Science · sv
PARK19-trunkeringsmutanten Dnajc6 orsakar lysosomal brist‑inducerad uppreglering av patologisk α‑synuklein och neurodegeneration i dopaminerga celler i substantia nigra hos PARK19 knockin‑möss
Varför denna muse‑studie är viktig för Parkinsons sjukdom
Parkinsons sjukdom berövar människor rörlighet genom att långsamt döda en liten grupp hjärnceller som tillverkar budbäraren dopamin. De flesta fall uppstår ur en blandning av ålder och miljö, men en minoritet orsakas av enkla genfel som fungerar som kraftfulla ledtrådar till sjukdomsprocessen. Denna studie undersöker en sådan gen, DNAJC6, med hjälp av en specialkonstruerad mus för att visa hur en liten förändring djupt inne i hjärnceller kan försvaga deras avfallshanteringssystem, överbelasta dem med ett klibbigt protein kallat alfa‑synuklein och slutligen leda till neuronförlust och Parkinson‑liknande symtom. 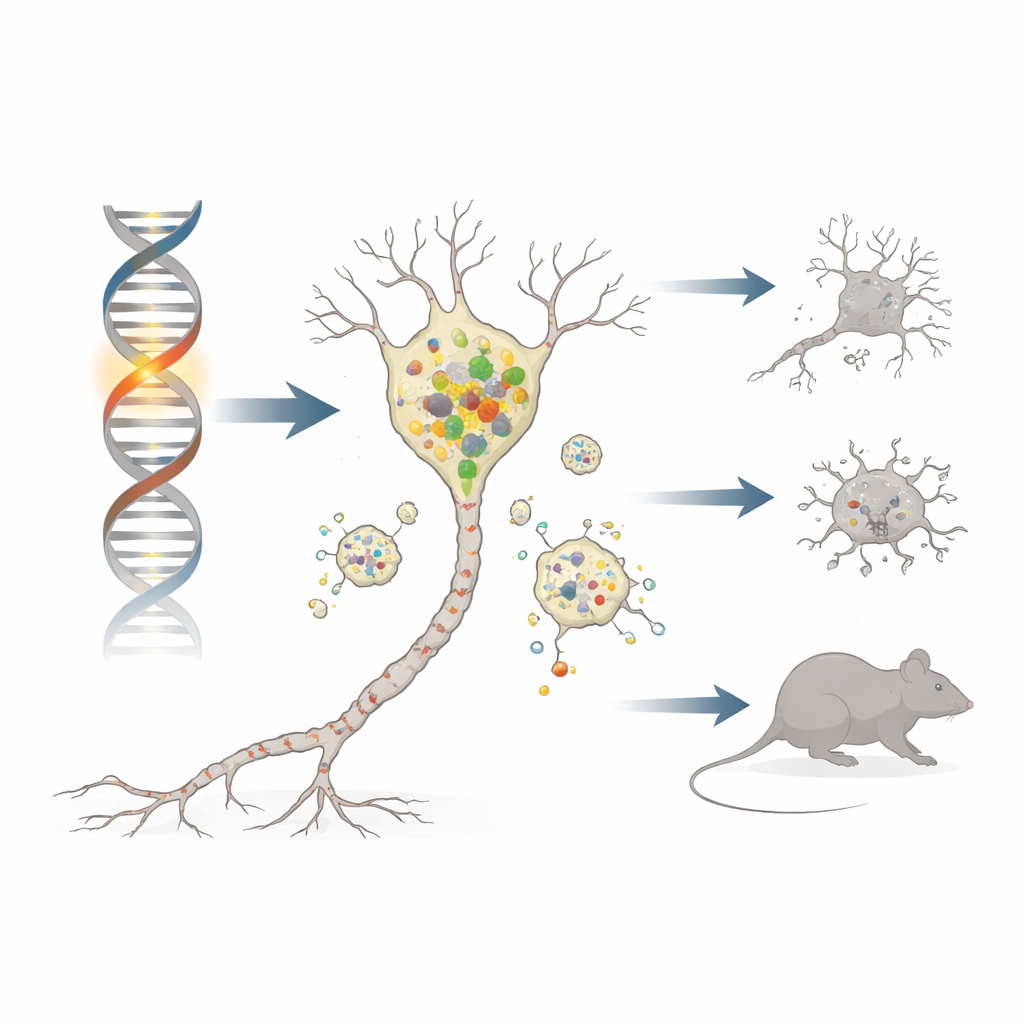
En defekt hjälparprotein i hjärnceller
Genen DNAJC6 kodar för ett protein som finns nästan uteslutande i neuroner, där det hjälper till att hantera klatrin, ett beläggsliknande molekylkomplex som formar och återvinner cellmembran. I flera familjer med en tidigt debuterande form av Parkinsons sjukdom, kallad PARK19, har båda kopiorna av DNAJC6 skadliga förändringar som kapar av en kritisk ände av proteinet. För att efterlikna detta skapade forskarna med CRISPR genredigering möss vars genvariant (kallad Dnajc6 hos möss) slutar tidigt på en motsvarande position. Dessa homozygota ”Q787X”‑möss producerar endast den förkortade formen av proteinet, medan heterozygota möss bär en normal och en muterad kopia, liknande friska bärare i mänskliga familjer.
Från gendefekt till rörelsestörningar
Teamet följde mössen medan de åldrades och testade deras rörelseförmåga. Vid fem månader uppträdde alla grupper normalt. Vid nio månader utvecklade dock möss med två mutanta kopior klassiska Parkinson‑lika motoriska problem: de rörde sig långsammare, täckte kortare avstånd och behövde mer tid för att gå nedför en testpinne, vilket speglar hypokinesi och bradykinesi hos patienter. När forskarna undersökte deras hjärnor såg de en påtaglig förlust av dopaminproducerande neuroner i substantia nigra och förtunning av deras nervändar i striatum. Dessa sårbara neuroner innehöll också klumpar av fosforylerad alfa‑synuklein, liknande Lewy‑kropps‑patologin som ses vid mänsklig Parkinsons sjukdom. Heterozygota möss, med endast en muterad kopia, visade inga av dessa förändringar.
När cellernas återvinningssystem bryter ihop
För att förstå händelsekedjan undersökte författarna cellernas återvinningscentraler: lysosomerna. I dopaminneuroner från mutanta möss var nivåerna av klatrin tung kedja minskade, vilket förväntas störa en process kallad autophagic lysosome reformation—sättet celler fyller på sin lysosompool. Antalet lysosomer föll, och markörer för nedsatt cellulär ”självätning” (autofagi) ökade. Avgörande sjönk ett viktigt lysosomalt enzym, katepsin D, medan alfa‑synuklein och dess mer toxiska fosforylerade och oligomeriska former byggdes upp och till och med blev motståndskraftiga mot nedbrytning. Denna lysosomala svikt var selektiv: närliggande hämmande neuroner i andra regioner visade inte samma underskott, vilket lyfter fram substantia nigras dopaminerga cellers särskilda sårbarhet. 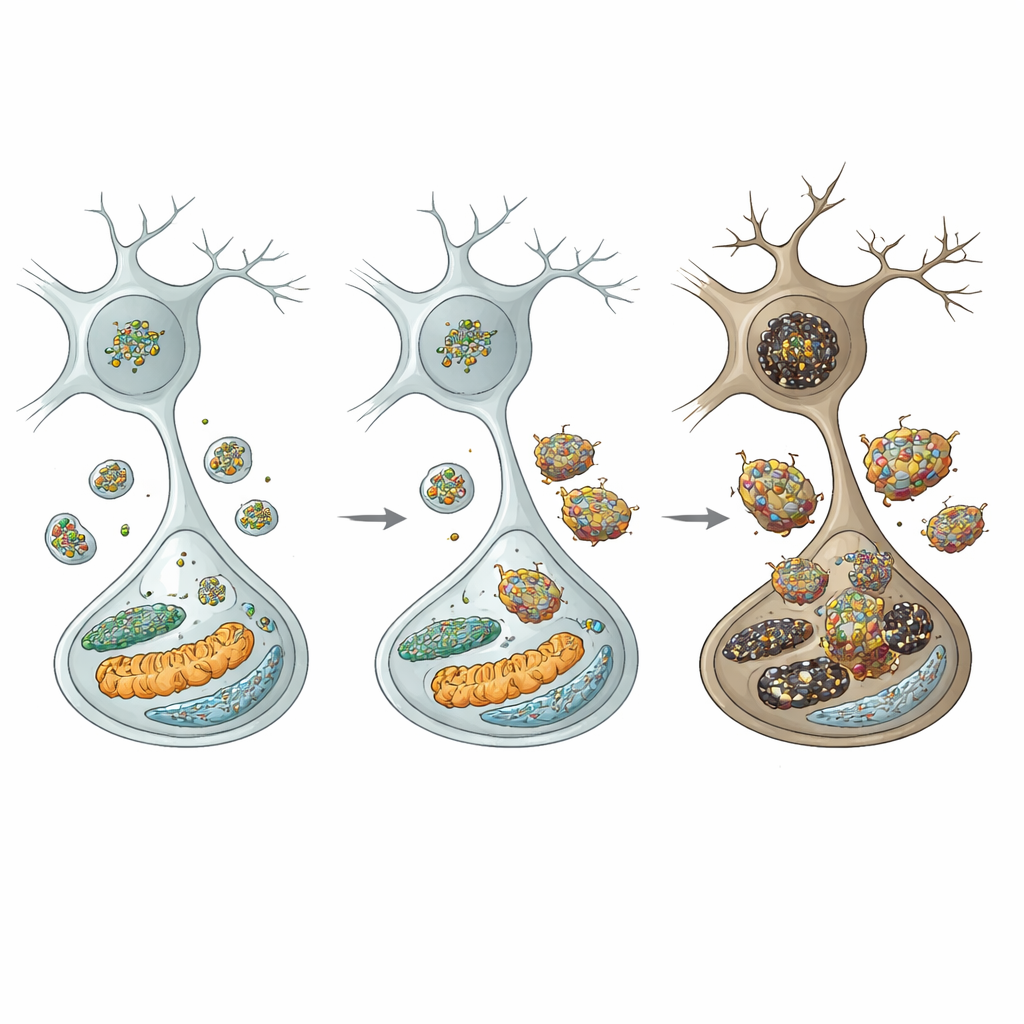
Spridande skada inne i och utanför neuronen
Det överskjutande alfa‑synukleinet stannade inte kvar på sin plats. Det ackumulerades på två viktiga interna strukturer—endoplasmatiska retikulumet och mitokondrierna—där det utlöste stress och skada. I det endoplasmatiska retikulumet aktiverade det svar på ofalt veckade proteiner och pro‑dödsignalering. I mitokondrierna minskade det aktiviteten i komplex I som producerar energi, ökade reaktiva syreföreningar och främjade frisättning av cytokrom c, vilket aktiverar självmordsenzym kända som kaspaser. Samtidigt läckte sannolikt oligomeriskt alfa‑synuklein ut ur neuroner och väckte närliggande mikroglia, hjärnans immunsentineller. Dessa mikroglia övergick till ett proinflammatoriskt tillstånd, aktiverade ett NLRP3‑inflammasomkomplex och frisatte inflammatoriska molekyler såsom IL‑1β, IL‑18 och TNF‑α. Dessa signaler aktiverade i sin tur ytterligare dödsvägar i dopaminneuroner, inklusive JNK‑drivna och nekroptotiska vägar, och skapade en ond cirkel av skada.
En drog som återställer cellens städbesättning
Forskarna frågade sedan om ökad lysomproduktion kunde avbryta denna kaskad. De behandlade unga mutanta möss med rapamycin, en drog som indirekt frigör en huvudomkopplare kallad TFEB så att den kan gå in i kärnan och slå på gener som bygger lysosomer, samtidigt som autofagi stimuleras. Efter fyra månader visade rapamycin‑behandlade mutanta möss återställda nivåer av lysosomala markörer och katepsin D i substantia nigra och mycket lägre uppbyggnad av alfa‑synuklein. Anmärkningsvärt nog skyddades dessa möss i stor utsträckning från förlusten av dopaminneuroner både i substantia nigra och i närliggande ventral tegmental area, och deras motoriska prestation förbättrades mot normal nivå. Genom att verka uppströms på cellens avfallshanteringsnätverk dämpade rapamycin effektivt den efterföljande kaskaden av proteinansamling, organelstres, inflammation och celldöd.
Vad detta betyder för förståelsen och behandlingen av Parkinsons
Enkelt uttryckt visar denna studie hur ett enstaka ärftligt fel i ett neuronspecifikt hjälparprotein kan utlösa en kedjereaktion: färre lysosomer, svagare katepsin D‑aktivitet, stigande nivåer av toxiskt alfa‑synuklein, skador på viktiga cellulära compartment, överdriven inflammatorisk reaktion och slutligen förlusten av dopaminneuroner som ligger bakom Parkinsonsymtomen. Även om denna specifika mutation är sällsynt, återfinns samma teman—lysosomal brist, dålig proteinrensning och alfa‑synukleinöverbelastning—även i vanligare, icke‑familjära former av Parkinsons sjukdom. Arbetet stärker därför idén att återställa hjärnans städsystem, till exempel genom TFEB‑aktiverande eller autofagi‑ökande läkemedel som rapamycin eller säkrare efterträdare, kan vara en lovande strategi för att sakta eller förebygga Parkinson‑relaterad neurodegeneration.
Citering: Wang, HL., Chen, YL., Chiu, TJ. et al. PARK19 truncation mutant Dnajc6 causes lysosomal deficiency-induced upregulation of pathologic α-synuclein and neurodegeneration of substantia nigra dopaminergic cells in PARK19 knockin mice. npj Parkinsons Dis. 12, 102 (2026). https://doi.org/10.1038/s41531-026-01317-8
Nyckelord: Parkinsons sjukdom, lysosomer, alfa‑synuklein, dopaminerga neuroner, rapamycin