Clear Sky Science · he
מוטציית חיתוך PARK19 ב-Dnajc6 גורמת לחוסר חומצונים־ליזוזומליים, לעלייה פתולוגית של α‑synuclein ולניוון של תאי דופמינרגיים בסובסטנסיה ניגרה בעכברי PARK19 knockin
מדוע מחקר בעכברים זה חשוב עבור מחלת פרקינסון
מחלת פרקינסון גוזלת מאנשים את היכולת לנוע על‑ידי הרג איטי של קבוצת תאים קטנה במוח שמייצרת את המוליך הכימי דופמין. ברוב המקרים הגורמים הם תערובת של גיל וסביבה, אך במיעוט המקרים שגיאות גנטיות חד‑גניות מספקות רמזים חזקים לתהליך המחלה. מחקר זה בוחן גן כזה, DNAJC6, באמצעות עכבר מהונדס במיוחד כדי לחשוף כיצד שינוי זעיר בתוך תאי המוח עלול לשתק את מערכות הטיפול בפסולת התאית, להציף אותן בחלבון דביק בשם אלפא‑סינוקלאין ולבסוף להוביל לאובדן נוירונים ותסמינים הדומים לפרקינסון. 
חלבון מסייע פגום בתאי המוח
הגן DNAJC6 מקודד חלבון שמצוי כמעט אך ורק בנוירונים, שם הוא עוזר לנהל את הקלתרין, מולקולה דמויית מעיל שמעצבת וממחזרת ממברנות תאיות. בכמה משפחות עם צורה של מחלת פרקינסון בעלת התחלה מוקדמת הידועה כ‑PARK19, שתי העותקים של DNAJC6 נושאים שינויים מזיקים החותכים קצה חיוני של החלבון. כדי לחקות מצב זה השתמשו החוקרים בעריכת גנים CRISPR כדי ליצור עכברים שבהם גרסת הגן (Dnajc6 בעכברים) נפסקת מוקדם במיקום שקול. עכרים הומוזיגוטיים אלה, הקרויים “Q787X”, מייצרים רק את הצורה המקוצרת של החלבון, בעוד עכברים הטרוזיגוטיים נושאים עותק תקין ועותק מוטנטי, בדומה לנשאים בריאים במשפחות אנושיות.
מפגם גנטי לבעיות התנועה
הצוות עקב אחרי העכברים ככל שהתבגרו ובחן את תנועתם. בגיל חמש חודשים כל הקבוצות התנהגו כרגיל. עם זאת, בגיל תשעה חודשים עכברים עם שני עותקים מוטנטיים פיתחו בעיות תנועה קלאסיות הדומות לפרקינסון: הם נעו לאט יותר, כיסו מרחקים קצרים יותר והזדקקו לזמן נוסף לרדת מעמודת מבחן—מה שמשקף היפוקינזיה וברדיקינזיה בחולים. כאשר המדענים בדקו את מוחם ראו אובדן משמעותי של נוירונים מייצרי דופמין בסובסטנסיה ניגרה ודילול של סיומות העצב שלהם בסטראטום. נוירונים פגיעים אלה גם הכילו גושים של אלפא‑סינוקלאין מזורחן, בדומה לפתולוגיית גופיפי לווי הנראית בפרקינסון אנושי. עכברים הטרוזיגוטיים, עם עותק מוטנטי יחיד, לא הראו את השינויים הללו.
כאשר המיחזור התאי מתפרק
כדי להבין את שרשרת האירועים, המחברים בחנו את מרכזי המיחזור של התא: הליזוזומים. בתאי דופמין של עכברים מוטנטים רמות של שרשרת כבדה של קלתרין ירדו, דבר הצפוי להפריע לתהליך שנקרא יצירת ליזוזום מחדש באוטופאגיה—the autophagic lysosome reformation—אופן שבו תאים ממלאים מחדש את מאגר הליזוזומים שלהם. אכן, מספר הליזוזומים ירד וסמנים של אוטופאגיה פגועה עלו. באופן קריטי, אנזים ליזוזומלי מרכזי, קטפטסין D, ירד, בעוד אלפא‑סינוקלאין וצורותיו הרעילות המזורחנות והאוליגומריות הצטברו ואפילו הפכו עמידות לעיכול. כשלון ליזוזומלי זה היה סלקטיבי: תאים מעכבים סמוכים באזורים אחרים לא הראו את אותם חסרים, מה שמדגיש את הרגישות המיוחדת של תאי הדופמין בסובסטנסיה ניגרה. 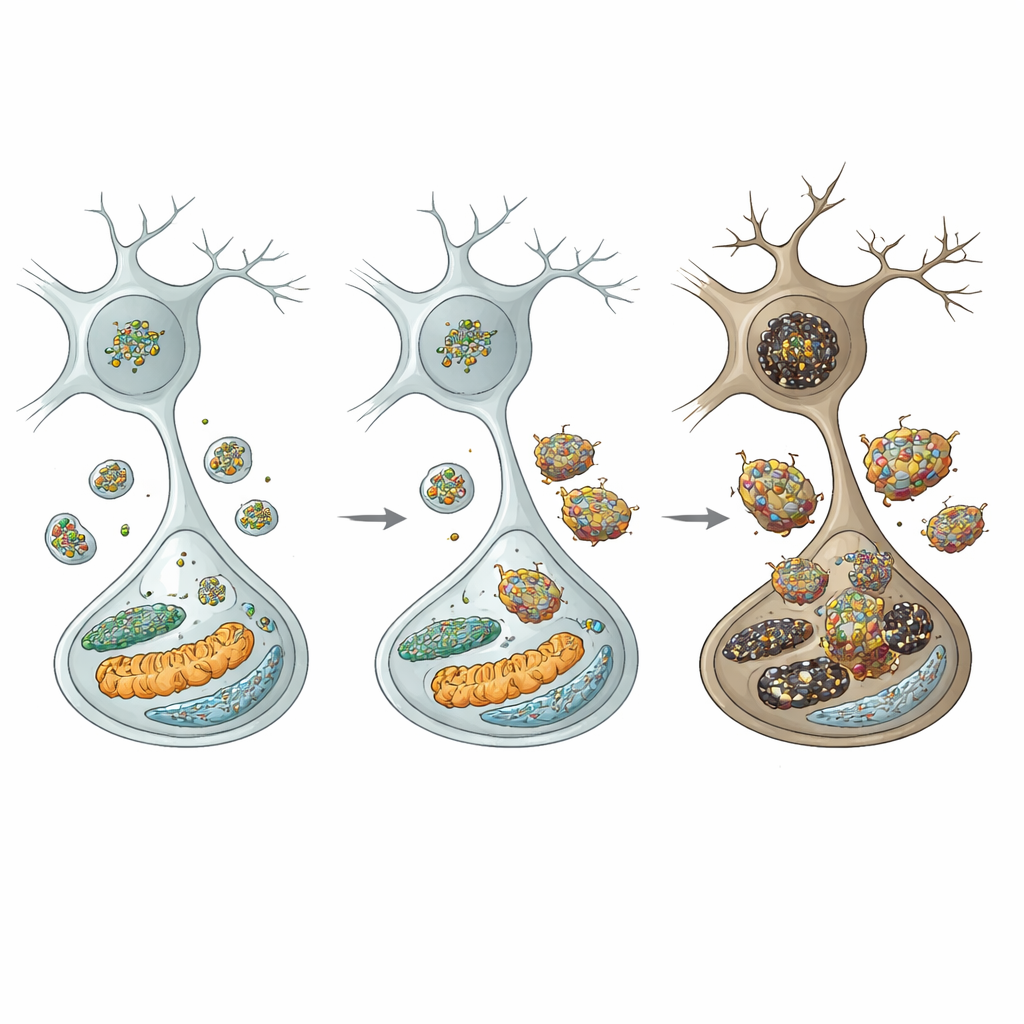
נזק שמשתלט בתוך ומחוץ לנוירון
אלפא‑סינוקלאין העודף לא נשאר במקום. הוא הצטבר על שני מבנים פנימיים חיוניים—הרשת האנדופלסמטית והמיטוכונדריה—שם הוא עורר מתחים ונזק. ברשת האנדופלסמטית הוא הפעיל תגובות למתח עקב חלבונים לא מקופלים ואיתותי מוות. במיטוכונדריה הוא הפחית את פעילות הקומפלקס I המייצר אנרגיה, הגדיל יצור של סוגי חמצון ריאקטיביים וקידם שחרור של ציטוכרום c, שמפעיל אנזימי התאבדות הנקראים קאספאזות. במקביל, אלפא‑סינוקלאין אוליגומרי ככל הנראה דלף החוצה מהנוירונים והעיר מיקרוגליה סמוכה, השומרים החיסוניים של המוח. מיקרוגליה אלה התדרגה למצב פרו‑דלקתי, הפעילה קומפלקס אינפלממסום NLRP3 ושיחרה מולקולות דלקתיות כמו IL‑1β, IL‑18 ו‑TNF‑α. אותות אלה, בתורם, הפעילו נתיבי מוות נוספים בתוך תאי הדופמין, כולל נתיבי JNK ונתיבי נקרופטוזיס, ויצרו מעגל קסמים של פגיעה.
תרופה שמשיבה את צוות הניקיון התאי
החוקרים בדקו האם חיזוק ייצור הליזוזומים יכול לקטוע את קסקדת האירועים הזו. הם טיפלו בעכברים מוטנטיים צעירים ברפאמיצין, תרופה שמשחררת בצורה עקיפה מתג‑על מרכזי בשם TFEB לחדור לגרעין ולהפעיל גנים לבניית ליזוזומים, ובו‑זמנית מגרה אוטופאגיה. לאחר ארבעה חודשים, עכברים מוטנטים שטופלו ברפאמיצין הראו שחזור של רמות סמני ליזוזום וקטפטסין D בסובסטנסיה ניגרה והצטברות נמוכה בהרבה של אלפא‑סינוקלאין. באופן מרשים, עכברים אלה הוגנו ברובם מאובדן תאי דופמין הן בסובסטנסיה ניגרה והן באזור הוונטראלי טגמנטלי הקרוב, וביצועיהם המוטוריים השתפרו לכיוון הנורמה. על‑ידי פעולה בחלק העליון של רשת הטיפול בפסולת התאית, רפאמיצין החזיק אפקטיבית את קסקדת ההצטברות של חלבונים, מתחים בארגונלות, דלקת ומוות תאי.
מה משמעות זה להבנה וטיפול בפרקינסון
לסיכום, מחקר זה מראה כיצד פגם תורשתי יחיד בחלבון מסייע הספציפי לנוירונים יכול להצית תגובת שרשרת: פחות ליזוזומים, פעילות קטפטסין D מוחלשת, עלייה ברמות אלפא‑סינוקלאין הרעיל, נזק לאברונים מרכזיים, תגובתיות דלקתית וכתוצאה מכך אובדן נוירונים דופמינרגיים שמפרט את התסמינים של פרקינסון. על אף שמוטציה מסוימת זו נדירה, אותם נושאים—חוסר ליזוזומלי, ניקוי חלבונים לקוי והצפת אלפא‑סינוקלאין—נראים גם בצורות השכיחות יותר של פרקינסון שאינן משפחתיות. עבודה זו מחזקת את הרעיון ששיקום מערכות הניקיון של המוח, למשל באמצעות הפעלת TFEB או על‑ידי תרופות שמגבירות אוטופאגיה כמו רפאמיצין או יורשיו הבטוחים יותר, עלול להיות אסטרטגיה מבטיחה להאטה או מניעה של ניוון עצבי הקשור לפרקינסון.
ציטוט: Wang, HL., Chen, YL., Chiu, TJ. et al. PARK19 truncation mutant Dnajc6 causes lysosomal deficiency-induced upregulation of pathologic α-synuclein and neurodegeneration of substantia nigra dopaminergic cells in PARK19 knockin mice. npj Parkinsons Dis. 12, 102 (2026). https://doi.org/10.1038/s41531-026-01317-8
מילות מפתח: מחלת פרקינסון, ליזוזומים, אלפא‑סינוקלאין, תאים דופמינרגיים, רפאמיצין