Clear Sky Science · ja
PARK19の切断変異体Dnajc6はリソソーム欠損を引き起こし病的なα‑シヌクレインの上昇と黒質ドーパミン作動性細胞の神経変性をPARK19ノックインマウスで誘導する
このマウス研究がパーキンソン病にとって重要な理由
パーキンソン病は、化学メッセンジャーであるドーパミンを作る少数の脳細胞をゆっくりと失うことで運動機能を奪います。多くの症例は加齢と環境要因の組み合わせによりますが、一部は単一遺伝子の異常によって起こり、病態解明の強力な手がかりになります。本研究はそのような遺伝子の一つであるDNAJC6を、特別に作られたマウスを用いて調べています。細胞内部の小さな変化が廃棄物処理システムを損ない、粘着性のあるタンパク質であるα‑シヌクレインを蓄積させ、最終的にニューロンの喪失とパーキンソン様の症状に至る仕組みを明らかにしています。 
脳細胞の不具合な補助タンパク質
DNAJC6遺伝子はほぼニューロンに限定して発現するタンパク質を作り、クラシンという被膜様分子の取り扱いを助けて細胞膜の形作りや再利用を支えます。PARK19として知られる若年発症型パーキンソン病のいくつかの家系では、DNAJC6の両コピーにタンパク質の重要な末端を切り落とす致命的な変化が入っています。この状況を模倣するために、研究者らはCRISPR遺伝子編集を使い、マウスの遺伝子(マウスではDnajc6と呼ばれる)が同等の位置で早期停止する個体を作成しました。これらのホモ接合「Q787X」マウスは短縮型タンパク質のみを産生し、ヘテロ接合のマウスはヒトの家系に見られる健常保因者と同様に一つは正常コピー、一つは変異コピーを持ちます。
遺伝子欠陥から運動障害へ
研究チームはマウスを加齢とともに追跡し、運動機能を評価しました。5か月時点では全グループに異常は見られませんでした。しかし9か月になると、両方が変異コピーのマウスは古典的なパーキンソン様の運動障害を示しました:移動が遅く、移動距離が短く、試験用のポールを降りるのに時間がかかるなどで、患者の低運動症や徐動に相当します。脳を調べると、黒質にあるドーパミン産生ニューロンの著しい喪失と線条体における神経終末の希薄化が確認されました。これらの脆弱なニューロンは、ヒトのパーキンソン病で見られるレビー小体病理に似たリン酸化α‑シヌクレインの凝集も含んでいました。ヘテロ接合のマウス(変異を1コピー持つ)はこれらの変化を示しませんでした。
細胞のリサイクルが破綻したとき
一連の出来事を理解するために、著者らは細胞のリサイクル拠点であるリソソームを調べました。変異マウスのドーパミンニューロンではクラシン重鎖のレベルが低下しており、これは細胞がリソソーム貯蔵を補充する過程であるオートファジックリソソーム再形成の障害を引き起こすと考えられます。実際にリソソーム数は減少し、細胞の「自食(オートファジー)」の障害を示すマーカーは増加していました。重要なリソソーム酵素であるカテプシンDが低下し、α‑シヌクレインとそのより毒性の高いリン酸化型やオリゴマー型が蓄積して分解に抵抗性を示すようになりました。このリソソーム障害は選択的で、近傍の抑制性ニューロンでは同じ欠損が見られず、黒質ドーパミン細胞の特異的脆弱性が浮き彫りになりました。 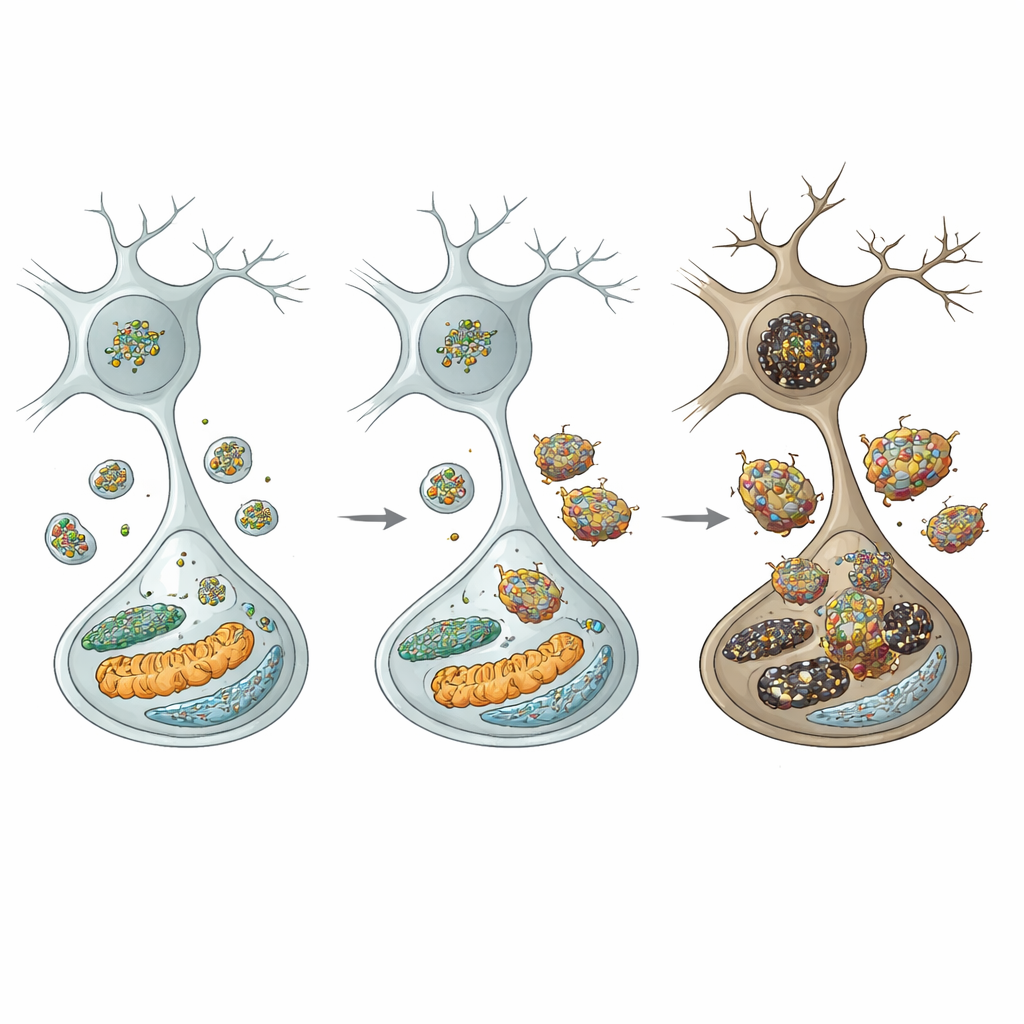
ニューロン内外へ広がる損傷
過剰なα‑シヌクレインは局所に留まりませんでした。小胞体とミトコンドリアという二つの重要な内部構造に蓄積してストレスと損傷を引き起こしました。小胞体では、未折りたたみタンパク質反応が活性化され、細胞死を促すシグナルが作動しました。ミトコンドリアでは、エネルギー産生の複合体I活性が低下し、活性酸素種が増加し、シトクロムcが放出されてカスパーゼと呼ばれる自殺系酵素が活性化されました。同時にオリゴマー化したα‑シヌクレインはニューロン外へ漏れ出し、近傍のミクログリア(脳の免疫見張り役)を刺激した可能性があります。これらのミクログリアは炎症誘導的な状態へと変化し、NLRP3インフラマソームを活性化し、IL‑1β、IL‑18、TNF‑αなどの炎症性分子を放出しました。これらの信号はさらにドーパミンニューロン内の死の経路(JNK駆動やネクロプトーシス経路など)を活性化し、損傷の悪循環を作り出しました。
細胞の清掃部隊を回復させる薬
研究者らは次に、リソソームの産生を高めることでこの連鎖を遮断できるかを検討しました。若い変異マウスをラパマイシンで治療しました。ラパマイシンは間接的にTFEBというマスタースイッチを核へ入らせ、リソソーム構築遺伝子をオンにし、オートファジーも刺激します。4か月後、ラパマイシン投与を受けた変異マウスでは黒質のリソソームマーカーとカテプシンDのレベルが回復し、α‑シヌクレインの蓄積は大幅に低下しました。驚くべきことに、これらのマウスは黒質および近接する腹側被蓋野のドーパミンニューロン喪失から大部分保護され、運動機能も正常に近づきました。細胞の廃棄処理ネットワークの上流を修復することで、ラパマイシンはタンパク質蓄積、オルガネラストレス、炎症、細胞死という下流の連鎖を効果的に鈍化させました。
パーキンソン病の理解と治療にとっての意義
簡潔に言えば、本研究はニューロン特異的な補助タンパク質の単一の遺伝的欠陥がどのように一連の反応を引き起こすかを示しています:リソソーム減少、カテプシンD活性の低下、有害なα‑シヌクレインの増加、主要な細胞区画の損傷、過剰な炎症反応、そして最終的にパーキンソン症状の基盤となるドーパミンニューロンの喪失です。この特定の変異は稀ですが、リソソーム欠損、タンパク質除去不良、α‑シヌクレインの過負荷といったテーマは、より一般的な非家族性パーキンソン病にも共通して現れます。したがって本研究は、TFEBを活性化する薬剤やラパマイシンのようなオートファジー促進薬、あるいはより安全な後継薬を用いて脳の“清掃システム”を回復させることが、パーキンソン病に伴う神経変性を遅らせたり予防したりする有望な戦略になり得るという考えを強化します。
引用: Wang, HL., Chen, YL., Chiu, TJ. et al. PARK19 truncation mutant Dnajc6 causes lysosomal deficiency-induced upregulation of pathologic α-synuclein and neurodegeneration of substantia nigra dopaminergic cells in PARK19 knockin mice. npj Parkinsons Dis. 12, 102 (2026). https://doi.org/10.1038/s41531-026-01317-8
キーワード: パーキンソン病, リソソーム, アルファシヌクレイン, ドーパミン作動性ニューロン, ラパマイシン