Clear Sky Science · ar
طفرة قطع PARK19 في Dnajc6 تسبب عجزًا نِزليًا يؤدي إلى ارتفاع مضر في α‑سينوكلين وتحلل عصبي لخلايا الدوبامين في المادة السوداء لدى فئران PARK19 المعادلة جينيًا
لماذا تهم هذه الدراسة على الفئران مرض باركنسون
يسلب مرض باركنسون قدرة الأشخاص على الحركة عن طريق قتل مجموعة صغيرة من خلايا الدماغ التي تُنتج الناقل الكيميائي الدوبامين بشكل بطيء. تنشأ معظم الحالات من تداخل العمر والبيئة، لكن قلة منها ناتجة عن أخطاء في جين واحد توفر دلائل قوية على آلية المرض. تفحص هذه الدراسة أحد هذه الجينات، DNAJC6، باستخدام فأر مُهندس خصيصًا لتوضيح كيف يمكن لتغير صغير داخل الخلايا العصبية أن يعطِّل أنظمة التخلص من النفايات، ويُثقلها ببروتين لزج يُدعى ألفا‑سينوكلين، ويؤدي في النهاية إلى فقدان الخلايا العصبية وظهور أعراض شبيهة بمرض باركنسون. 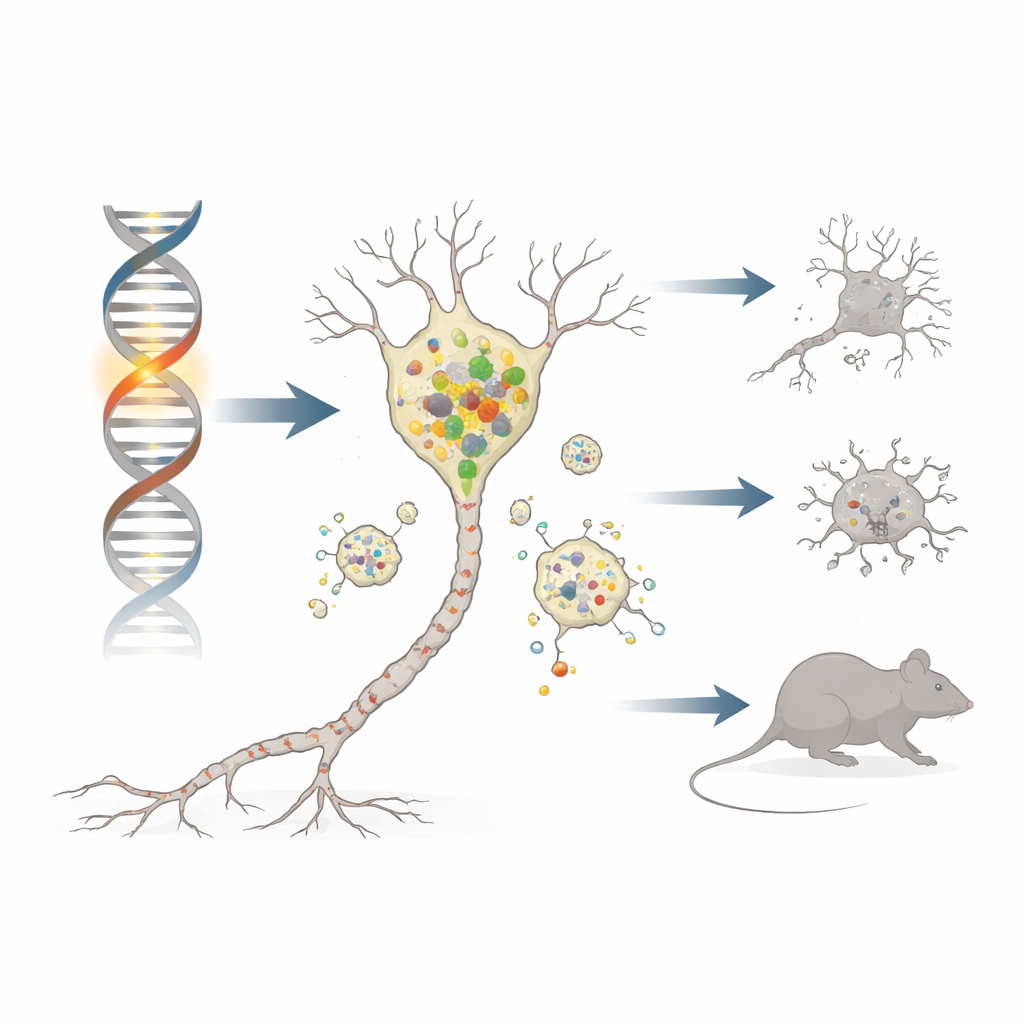
بروتين مساعد معطل في الخلايا العصبية
يصنع جين DNAJC6 بروتينًا يوجد تقريبًا حصريًا في الخلايا العصبية، حيث يساعد على تنظيم الكلاترين، وهي جزيئات تغطي وتشكّل أغشية الخلايا وتعيد تدويرها. في عدة عائلات تعاني شكلًا مبكرًا من باركنسون المعروف باسم PARK19، يحمل كلتا نسختي DNAJC6 تغييرات ضارة تقصُّ نهاية حرجة من البروتين. لمحاكاة هذا الوضع، استخدم الباحثون تحرير الجينات CRISPR لإنشاء فئران تتوقف نسخة الجين لديها (المسمى Dnajc6 في الفئران) مبكرًا عند موضع معادل. تنتج هذه الفئران المتناظرة «Q787X» الشكل المختصر فقط من البروتين، بينما تحمل الفئران المتغايرة نسخة عادية ونسخة طفرة، شبيهة بحاملي الطفرة الأصحاء في العائلات البشرية.
من عيب جيني إلى مشاكل حركية
عندما يتعطل إعادة تدوير الخلايا
لفهم سلسلة الأحداث، نظر المؤلفون إلى مراكز إعادة التدوير داخل الخلية: الجسيمات الليزوزومية. في خلايا الدوبامين من الفئران الطافرة، انخفضت مستويات السلسلة الثقيلة للكلاترين، وهو ما يُتوقع أن يُعطل عملية تُسمى إعادة تكوين الجسيمات الليزوزومية عبر الالتهام الذاتي—الطريقة التي تجدد بها الخلايا مخزون الليزوزومات. فعلاً، انخفض عدد الليزوزومات وارتفعت مؤشرات ضعف الالتهام الذاتي الخلوي. والأهم أن إنزيمًا لِيزوزوميًا رئيسيًا، كاتيبسين D، انخفض، في حين تراكمت أشكال ألفا‑سينوكلين ونسخها المفسفَرة والمتعددة (أوليغومرات) وأصبحت مقاومة للهضم. كان هذا الفشل الليزوزومي انتقائيًا: لم تُظهر الخلايا العصبية المثبطة المجاورة في مناطق أخرى نفس العجز، مما يبرز هشاشة خلايا الدوبامين في المادة السوداء بشكل خاص. 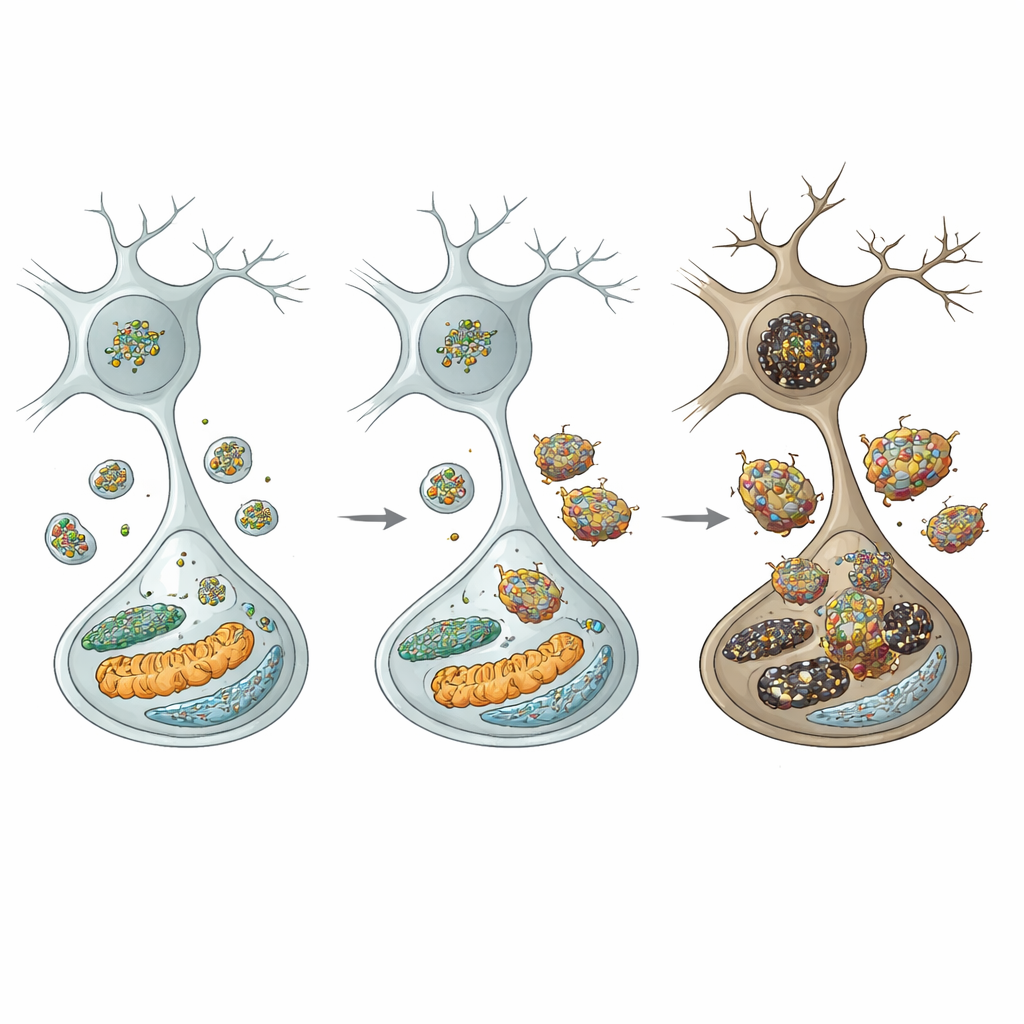
انتشار الضرر داخل الخلية وخارجها
لم تَحْبِس ألفا‑سينوكلين الزائدة نفسها في مكان واحد. تراكمت على بنيتين داخليتين حيويتين—الشبكة الإندوبلازمية والميتوكندريا—حيث أثارت الإجهاد والضرر. في الشبكة الإندوبلازمية، أطلقت استجابات الإجهاد الخاصة بالبروتينات غير المطوية وإشارات دفع نحو الموت الخلوي. في الميتوكندريا، قلّلت نشاط المعقد I المنتج للطاقة، زادت الجذور الحرة التفاعلية، وعززت إطلاق السيتوكروم c، الذي ينشط إنزيمات الموت المعروفة بالكاسبازات. في الوقت نفسه، من المحتمل أن الأشكال الأوليغومرية لألفا‑سينوكلين تسربت خارج الخلايا العصبية وأثارت الخلايا الدبقية الصغيرة المجاورة، الحراس المناعيين للدماغ. تحولت هذه الخلايا الدبقية إلى حالة مؤيدة للالتهاب، فعّلت مركبًا يسمى إنفلاماسوم NLRP3، وأطلقت جزيئات التهابية مثل IL‑1β وIL‑18 وTNF‑α. تلك الإشارات بدورها نشّطت مسارات موت إضافية داخل خلايا الدوبامين، بما في ذلك مسارات تقودها JNK ومسارات نيكرُبتوزت، مكونة دائرة مؤذية متواصلة.
دواء يعيد طواقم تنظيف الخلايا
سأل الباحثون بعد ذلك ما إذا كان تعزيز إنتاج الليزوزومات يمكن أن يقطع هذه السلسلة الضارة. عالجوا فئرانًا طافرة صغيرة برابامايسين، دواء يحرر بشكل غير مباشر مفتاحًا رئيسيًا يُدعى TFEB ليدخل النواة ويشغّل جينات بناء الليزوزومات، بينما يحفز أيضًا الالتهام الذاتي. بعد أربعة أشهر، أظهرت الفئران الطافرة المعالجة بالرابامايسين استعادة مستويات مؤشرات الليزوزوم وكاتيبسين D في المادة السوداء وتراجعًا كبيرًا في تراكم ألفا‑سينوكلين. بشكل ملحوظ، كانت هذه الفئران محمية إلى حد كبير من فقدان خلايا الدوبامين في كل من المادة السوداء والمنطقة الجيبية البطنية المجاورة، وتحسّن أداؤها الحركي نحو الطبيعي. عن طريق العمل أعلى سلسلة معالجة النفايات الخلوية، خفف الرابامايسين بفعالية من سلسلة التتابعات اللاحقة لتراكم البروتين، وإجهاد العُضَيَّات، والالتهاب، والموت الخلوي.
ماذا يعني هذا لفهم وعلاج باركنسون
بعبارة بسيطة، تُظهر هذه الدراسة كيف يمكن لخلل وراثي وحيد في بروتين مساعد خاص بالخلايا العصبية أن يُطلق سلسلة من ردود الفعل: عدد أقل من الليزوزومات، ضعف نشاط كاتيبسين D، ارتفاع مستويات ألفا‑سينوكلين السام، ضرر للأقسام الخلوية الحيوية، فرط استجابة التهابية، وفي النهاية فقدان خلايا الدوبامين التي تقوم عليها أعراض باركنسون. رغم ندرة هذه الطفرة بالذات، تظهر نفس المواضيع—نقص ليزوزومي، ضعف إزالة البروتين، وتراكم ألفا‑سينوكلين—أيضًا في حالات باركنسون الشائعة غير العائلية. لذا تعزز هذه النتائج فكرة أن استعادة أنظمة تنظيف الدماغ، مثلاً عبر منشطّات TFEB أو أدوية تعزز الالتهام الذاتي مثل الرابامايسين أو نظائرها الآمنة أكثر، قد تكون استراتيجية واعدة لإبطاء أو منع التحلل العصبي المرتبط بباركنسون.
الاستشهاد: Wang, HL., Chen, YL., Chiu, TJ. et al. PARK19 truncation mutant Dnajc6 causes lysosomal deficiency-induced upregulation of pathologic α-synuclein and neurodegeneration of substantia nigra dopaminergic cells in PARK19 knockin mice. npj Parkinsons Dis. 12, 102 (2026). https://doi.org/10.1038/s41531-026-01317-8
الكلمات المفتاحية: مرض باركنسون, الجسيمات الليزوزومية, ألفا‑سينوكلين, الخلايا العصبية الدوبامينية, رابامايسين