Clear Sky Science · nl
PARK19-truncatiemutant Dnajc6 veroorzaakt door lysosomale tekortkoming geactiveerde pathologische α-synucleïne en neurodegeneratie van dopaminerge cellen in de substantia nigra bij PARK19 knockin-muizen
Waarom deze muizenstudie belangrijk is voor de ziekte van Parkinson
De ziekte van Parkinson berooft mensen van beweging door geleidelijk een kleine groep hersencellen die de boodschapper dopamine aanmaken te doden. De meeste gevallen ontstaan door een mix van leeftijd en omgeving, maar een minderheid wordt veroorzaakt door fouten in een enkel gen die krachtige aanwijzingen geven voor het ziekteproces. Deze studie onderzoekt een van die genen, DNAJC6, met behulp van speciaal gefabriceerde muizen om te laten zien hoe een kleine verandering diep in hersencellen hun afvalverwerkende systemen kan verzwakken, ze kan overladen met een kleverig eiwit genaamd alfa‑synucleïne, en uiteindelijk kan leiden tot verlies van neuronen en Parkinson‑achtige symptomen. 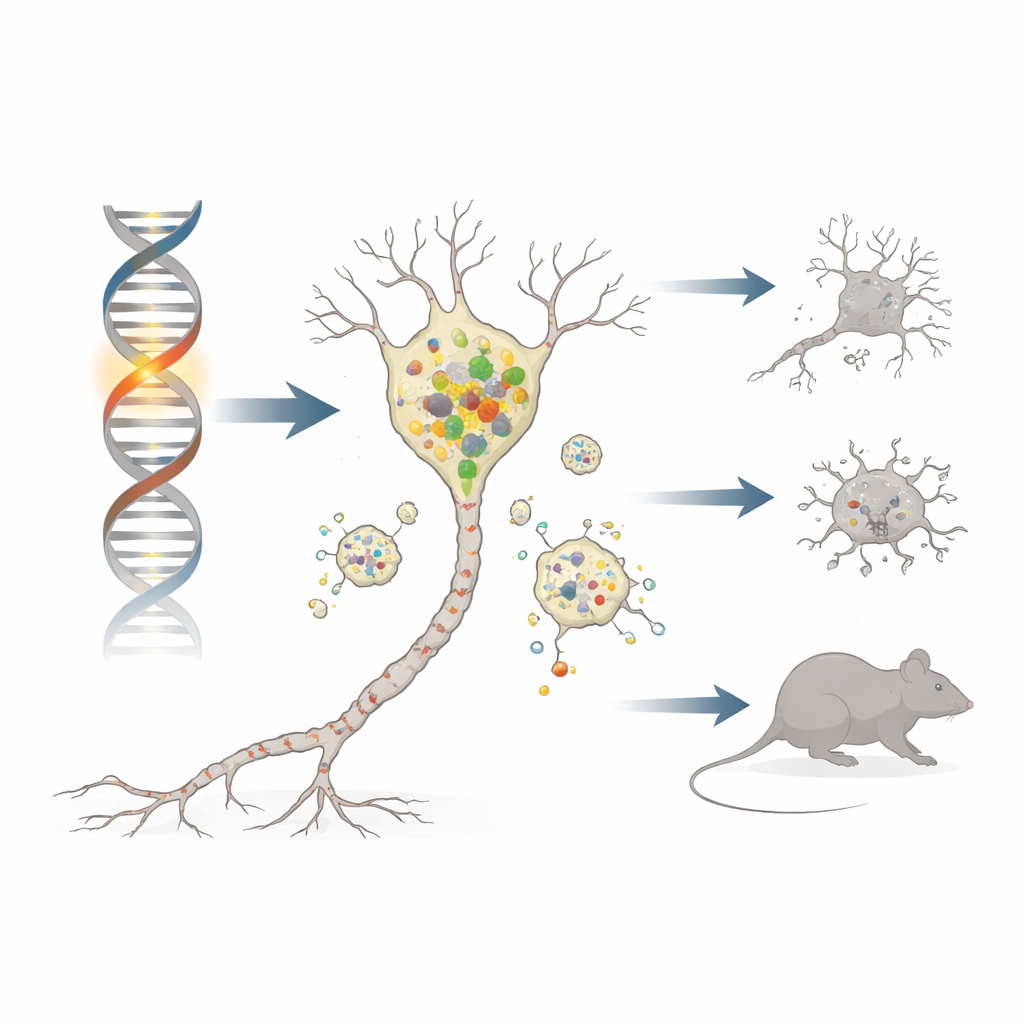
Een defect hulp-eiwit in hersencellen
Het gen DNAJC6 maakt een eiwit dat vrijwel uitsluitend in neuronen voorkomt en dat helpt bij het beheren van clathrine, een mantelachtig molecuul dat celmembranen vormt en recyclet. In meerdere families met een vroeg‑beginnende vorm van de ziekte van Parkinson, bekend als PARK19, dragen beide kopieën van DNAJC6 schadelijke veranderingen die een cruciaal uiteinde van het eiwit afknippen. Om deze situatie na te bootsen gebruikten de onderzoekers CRISPR-genbewerking om muizen te maken waarvan de versie van het gen (Dnajc6 bij muizen) vroegtijdig stopt op een equivalente plaats. Deze homozygote “Q787X”-muizen produceren alleen de verkorte vorm van het eiwit, terwijl heterozygote muizen één normale en één gemuteerde kopie dragen, vergelijkbaar met gezonde dragers in menselijke families.
Van gendefect naar bewegingsproblemen
Het team volgde de muizen tijdens het ouder worden en testte hun beweging. Op vijf maanden gedroegen alle groepen zich normaal. Tegen negen maanden ontwikkelden muizen met twee gemuteerde kopieën echter klassieke Parkinson‑achtige motorische problemen: ze bewogen trager, legden kortere afstanden af en hadden meer tijd nodig om een testpaal af te dalen, wat overeenkomt met hypokinesie en bradykinesie bij patiënten. Bij onderzoek van hun hersenen zagen de onderzoekers een duidelijke afname van dopamineproducerende neuronen in de substantia nigra en verdunning van hun zenuweinden in het striatum. Deze kwetsbare neuronen bevatten ook ophopingen van gefosforyleerd alfa‑synucleïne, vergelijkbaar met de Lewy‑lichaampjespathologie die bij menselijke ziekte‑van‑Parkinson‑patiënten wordt gezien. Heterozygote muizen, met slechts één gemuteerde kopie, toonden geen van deze veranderingen.
Wanneer cellulair recyclen faalt
Om de keten van gebeurtenissen te begrijpen, bekeken de auteurs de recyclagecentra van de cel: lysosomen. In dopaminerge neuronen van gemuteerde muizen waren de niveaus van clathrine heavy chain verlaagd, wat naar verwachting een proces verstoort dat autophagic lysosome reformation wordt genoemd—de manier waarop cellen hun lysosoomvoorraad aanvullen. Inderdaad daalde het aantal lysosomen en namen markers van verstoorde cellulaire "zelf‑eter"‑processen (autofagie) toe. Cruciaal was dat een belangrijke lysosomale enzym, cathepsine D, afnam, terwijl alfa‑synucleïne en diens toxischere gefosforyleerde en oligomere vormen zich ophoopten en zelfs resistent werden tegen afbraak. Deze lysosomale falen was selectief: naburige remmende neuronen in andere regio’s toonden niet dezelfde tekorten, wat de bijzondere kwetsbaarheid van dopaminerge cellen in de substantia nigra benadrukt. 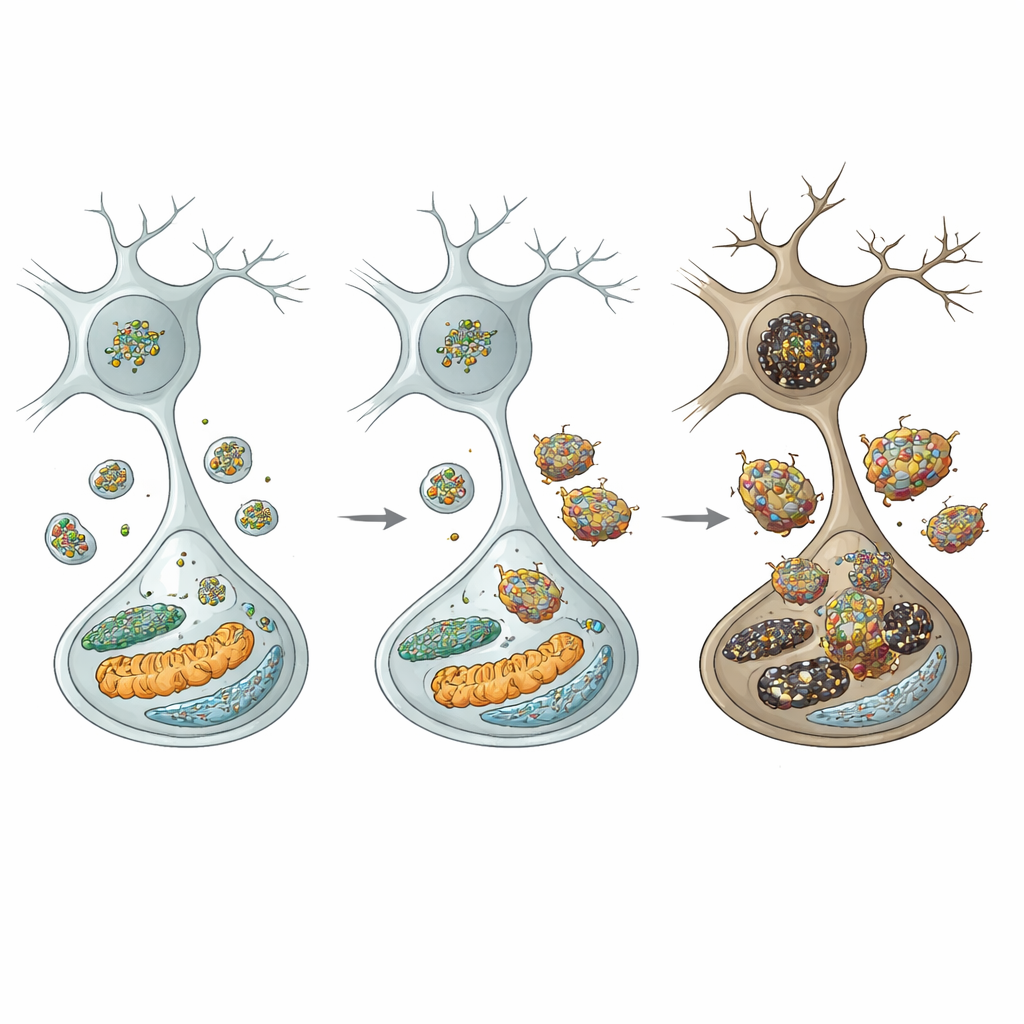
Verspreidende schade binnen en buiten de neuron
Het overtollige alfa‑synucleïne bleef niet op zijn plaats. Het stapelde zich op twee vitale interne structuren—het endoplasmatisch reticulum en mitochondriën—waar het stress en schade veroorzaakte. In het endoplasmatisch reticulum schakelde het reacties op ongevouwen eiwitten en pro‑deathsignalen aan. In mitochondriën verminderde het de activiteit van energieproducerend complex I, nam de productie van reactieve zuurstofsoorten toe en bevorderde het de vrijgave van cytochroom c, wat suïcide‑enzymen genaamd caspases activeert. Tegelijkertijd lekte oligomere alfa‑synucleïne waarschijnlijk uit neuronen en wekte naburige microglia, de immuurbewakers van de hersenen, tot activiteit. Deze microglia schakelden over naar een pro‑inflammatoire toestand, activeerden een NLRP3‑inflammasoomcomplex en gaven ontstekingsmoleculen vrij zoals IL‑1β, IL‑18 en TNF‑α. Die signalen activeerden op hun beurt bijkomende doodspaden in dopaminerge neuronen, waaronder JNK‑gedreven en necroptotische routes, wat een vicieuze cirkel van schade creëerde.
Een medicijn dat het opruimteam van de cel herstelt
De onderzoekers vroegen zich vervolgens af of het stimuleren van lysosoomproductie deze cascade kon onderbreken. Ze behandelden jonge gemuteerde muizen met rapamycine, een medicijn dat indirect een hoofdschakelaar genaamd TFEB vrijmaakt om de kern binnen te gaan en lysosoombouwende genen aan te zetten, terwijl het ook autofagie stimuleert. Na vier maanden toonden rapamycine‑behandelde gemuteerde muizen herstelde niveaus van lysosomale markers en cathepsine D in de substantia nigra en veel minder ophoping van alfa‑synucleïne. Opmerkelijk genoeg waren deze muizen grotendeels beschermd tegen het verlies van dopaminerge neuronen in zowel de substantia nigra als het nabijgelegen ventrale tegmentale gebied, en verbeterde hun motorische prestaties richting normaal. Door upstream in te grijpen in het vuilverwerkingssysteem van de cel, dempte rapamycine effectief de downstream cascade van eiwitophoping, organelstress, ontsteking en celdood.
Wat dit betekent voor begrip en behandeling van Parkinson
Kort gezegd toont deze studie aan hoe een enkele erfelijke fout in een neuron‑specifiek hulp‑eiwit een kettingreactie kan veroorzaken: minder lysosomen, zwakkere cathepsine D‑activiteit, stijgende niveaus van toxisch alfa‑synucleïne, schade aan sleutelcompartimenten van de cel, een overreactieve ontstekingsreactie en tenslotte het verlies van dopaminerge neuronen dat de symptomen van Parkinson onderbouwt. Hoewel deze specifieke mutatie zeldzaam is, verschijnen dezelfde thema’s—lysosomale tekortkoming, gebrekkige eiwitopruiming en alfa‑synucleïne‑overbelasting—ook bij meer voorkomende, niet‑familiaire vormen van de ziekte van Parkinson. Het werk versterkt daarom het idee dat het herstellen van de opruimsystemen van de hersenen, bijvoorbeeld met TFEB‑activerende of autofagie‑stimulerende middelen zoals rapamycine of veiligere opvolgers, een veelbelovende strategie kan zijn om Parkinson‑gerelateerde neurodegeneratie te vertragen of te voorkomen.
Bronvermelding: Wang, HL., Chen, YL., Chiu, TJ. et al. PARK19 truncation mutant Dnajc6 causes lysosomal deficiency-induced upregulation of pathologic α-synuclein and neurodegeneration of substantia nigra dopaminergic cells in PARK19 knockin mice. npj Parkinsons Dis. 12, 102 (2026). https://doi.org/10.1038/s41531-026-01317-8
Trefwoorden: Ziekte van Parkinson, lysosomen, alfa-synucleïne, dopaminerge neuronen, rapamycine