Clear Sky Science · tr
AMR-GNN: genomik antimikrobiyal direnç tahminini mümkün kılmak için çoklu temsilli bir grafik sinir ağı çerçevesi
İlaç direncini tahmin etmenin önemi
Antibiyotiklere dirençli enfeksiyonlar, her yıl bir milyondan fazla insanın ölümüne yol açarak zamanımızın en önemli tıbbi tehditlerinden biridir. Hekimlerin, belirli bir enfeksiyon için hangi antibiyotiklerin etkili olacağını daha hızlı söylemelerine acil ihtiyaç var; ancak geleneksel laboratuvar testleri birkaç gün sürebilir. Bu çalışma, bakterilerin tam DNA dizilimini okuyup çeşitli antibiyotiklere karşı dirençli mi yoksa duyarlı mı olacaklarını tahmin eden AMR-GNN adında yeni bir yapay zeka çerçevesi tanıtıyor; bu da potansiyel olarak yatağın başında aynı gün rehberlik sağlamanın yolunu açabilir.
Yavaş kültürlerden dijital DNA testlerine
Günümüzde çoğu hastane hâlâ kültür tabanlı testlere güveniyor: bakteriler laboratuvarda yetiştirilir ve büyümelerini durduran ilaçlar tespit edilir. Güvenilir olmakla birlikte bu yaklaşım yavaş ve emek yoğundur. Aynı zamanda, bakteriyel genomların tamamının dizilenmesi daha ucuz ve kolay hale gelerek ayrıntılı büyük veri kümeleri üretiliyor. Zorluk şudur: bakteriyel DNA son derece yüksek boyutludur, milyonlarca yapı taşı içerir ve bu genetik kodu bilgisayarların ilaç direncini tahmin edebileceği bir formata dönüştürmenin tek, üzerinde uzlaşılan bir yolu yoktur. Önceki araçlar genellikle birkaç bilinen direnç genine veya basit kalıplara odaklandı; bu, direnç tek bir mutasyona bağlı olduğunda işe yarar ama birçok ince değişiklik etkileştiğinde başarısız olur.
Farklı genomik bakışları tek bir resimde birleştirmek
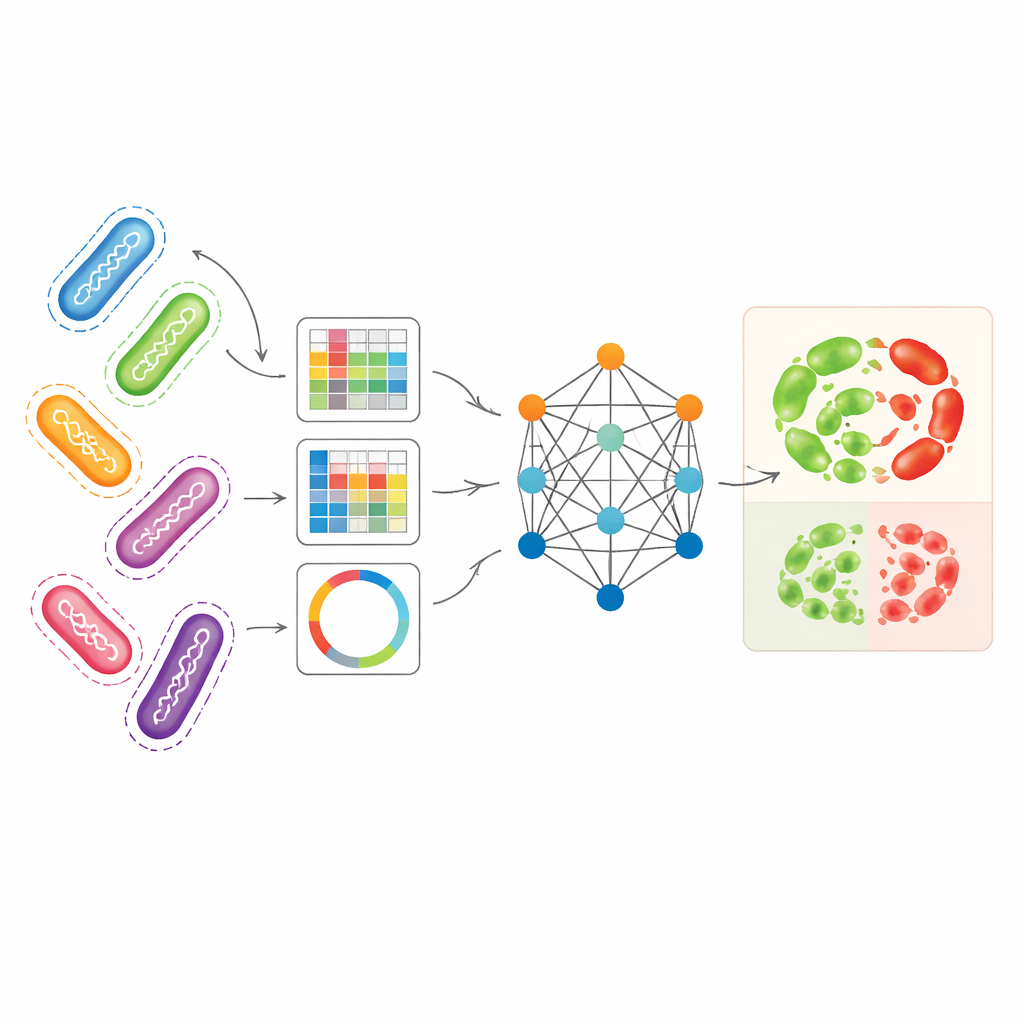
Araştırmacılar, bakteriyel genomları aynı anda temsil etmenin birbirini tamamlayan birkaç yolunu kullanmayı amaçladılar. Başlıca test vakası olarak özellikle karmaşık direnç desenlerine sahip hastane kaynaklı bir patojen olan Pseudomonas aeruginosa’yı kullandılar. Bir temsil biçimi olan unitigler, referans bir genom kullanmadan tekrarlayan DNA parçalarını yakalar. Diğer bir temsil belirli pozisyonlardaki küçük DNA değişikliklerini izlerken, üçüncüsü seçilmiş dirençle ilişkili genleri kısa DNA dizilerinin nasıl düzenlendiğini özetleyen görüntü-benzeri desenlere çevirir. Bu temsil biçimleri tek başlarına, özellikle bazı antibiyotikler için unitigler, standart makine öğrenimi modellerinin makul doğrulukla direnç tahmini yapmasına zaten izin verdi. Ancak her bakış açısı biyolojik hikâyenin bir parçasını kaçırır ve bunları ayrı ayrı kullanmak alttaki genom verilerinin zenginliğini yeterince değerlendirmez.
Grafik tabanlı model benzer suşlardan nasıl öğreniyor
AMR-GNN, her bir bakteri izolatını bir nokta (düğüm) olarak ele alan ve genetik olarak benzer izolatları bağlantılar (kenarlar) ile bağlayan grafik sinir ağı olarak bilinen bir derin öğrenme biçimi kullanır. Bu düzenekte, her izolatın ayrıntılı unitig profili ana özellik vektörünü oluştururken diğer genomik görünümler izolatların grafikte nasıl bağlanacağını tanımlar. Model daha sonra bu bağlantılar boyunca bilgi geçirir ve ilişkili genomlar arasında paylaşılan kalıplardan öğrenmesine olanak sağlar. Yazarlar, klonal ilişkilerin—bakterilerin yakın akraba olduğu ancak modelin keşfetmesi gereken nedenlerle direnç açısından farklılık gösterebildiği durumların—modeli yanıltmasını önlemek için aynı genetik soya ait izolatları birbirine bağlayan kenarları kasıtlı olarak kaldırdılar. Bu “ayırma” adımı, ağın geniş soy etiketlerine kestirme çözümler olarak değil, dirence özgü DNA özelliklerine daha fazla dikkat etmesini zorunlu kılar.
Bakteri ve ilaçlar arasında daha güçlü tahminler
Ekip AMR-GNN’yi tekil genomik görünümlere dayanan daha basit modellerle karşılaştırdığında, grafik tabanlı yaklaşım P. aeruginosa’da test edilen 12 antibiyotiğin neredeyse tamamı için performansı iyileştirdi; en büyük kazançlar önceden tahmin edilmesi en zor olan ilaçlar için görüldü. Model ayrıca bağımsız test veri kümelerine daha iyi genelleşti, ancak eğitim verisi dışına çıkıldığında performans hâlâ bir ölçüde düştü; bu da daha büyük ve daha çeşitli genom koleksiyonlarına olan ihtiyacı vurguluyor. P. aeruginosa’nın ötesinde araştırmacılar, AMR-GNN’yi Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus ve Enterococcus faecium da dahil olmak üzere diğer önemli patojenlerden 23.000’in üzerinde genom üzerinde, birçok klinik açıdan önemli antibiyotik için uyguladılar. Çoğu tür–ilaç kombinasyonunda çerçeve çok yüksek doğruluğa ulaştı ve bilinen direnç genlerinin küratörlüğüne dayanan yaygın olarak kullanılan kural tabanlı araçlardan daha iyi performans gösterdi.
Kara kutu modellerini daha açıklanabilir kılmak
Klinik kullanım için önemli bir endişe, böyle bir yapay zeka sisteminin belirli bir tahmini neden yaptığını açıklayıp açıklayamayacağıdır. Ekip, modelin kararlarına en çok hangi DNA özelliklerinin katkıda bulunduğunu takip eden yorumlanabilirlik yöntemleri uygulayarak buna yanıt verdi. Modelin en iyi performans gösterdiği ilaçlarda AMR-GNN birçok bilinen direnç geni ve mutasyonu, örneğin florokinolon antibiyotiklerinin klasik hedeflerini vurguladı. Ayrıca, bakteriyel büyümeyi durdurmak için gereken daha yüksek ilaç konsantrasyonlarıyla güçlü şekilde ilişkili olan ve laboratuvar takibi için yeni adaylar önerebilecek daha az iyi anlaşılan genlere de işaret etti. Bu hem direnci tahmin etme hem de olası biyolojik sürücüleri işaret etme yeteneği, saf tahmin ile mekanistik anlayış arasındaki boşluğu kapatmaya yardımcı olur.
Gelecekte hasta bakımına etkisi
Özetle, bu çalışma çoklu DNA “görünümlerini” bir grafik tabanlı derin öğrenme modelinde birleştirmenin, bakteriyel genomlardan antibiyotik direncinin tahminini önemli ölçüde iyileştirebileceğini gösteriyor. AMR-GNN, gen aktivite ölçümleri veya klinik bilgiler gibi diğer veri türlerine genişletilebilecek esnek, yorumlanabilir bir çerçeve olarak sunuluyor. Daha fazla çalışmaya—özellikle coğrafi olarak çeşitlendirilmiş daha büyük veri setlerine ve prospektif klinik denemelere—ihtiyaç olsa da, bu yaklaşım bir bakteri genom dizisinin hasta örneğinden doğrudan elde edilip doktorları doğru ilaca hızla yönlendirebileceği ve dirençli enfeksiyonların yayılmasını yavaşlatmaya yardımcı olabileceği bir geleceğe bizi daha da yaklaştırıyor.
Atıf: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
Anahtar kelimeler: antimikrobiyal direnç, grafik sinir ağları, bakteriyel genomik, makine öğrenimi, antibiyotik duyarlılık tahmini