Clear Sky Science · ja
AMR-GNN: ゲノム情報に基づく抗菌薬耐性予測を可能にする多表現グラフニューラルネットワークフレームワーク
薬剤耐性を予測する意義
抗生物質耐性による感染症は現代の重大な医療上の脅威の一つで、毎年100万人以上が命を落としています。臨床医は特定の感染症に対してどの抗生物質が有効かを速やかに知る必要がありますが、従来の検査は数日を要することが多いです。本研究はAMR-GNNと呼ばれる新しい人工知能フレームワークを提案します。これは細菌の全DNA配列を読み取り、各抗生物質に対して耐性か感受性かを予測するもので、臨床現場で当日中に治療指針を示す道を開く可能性があります。
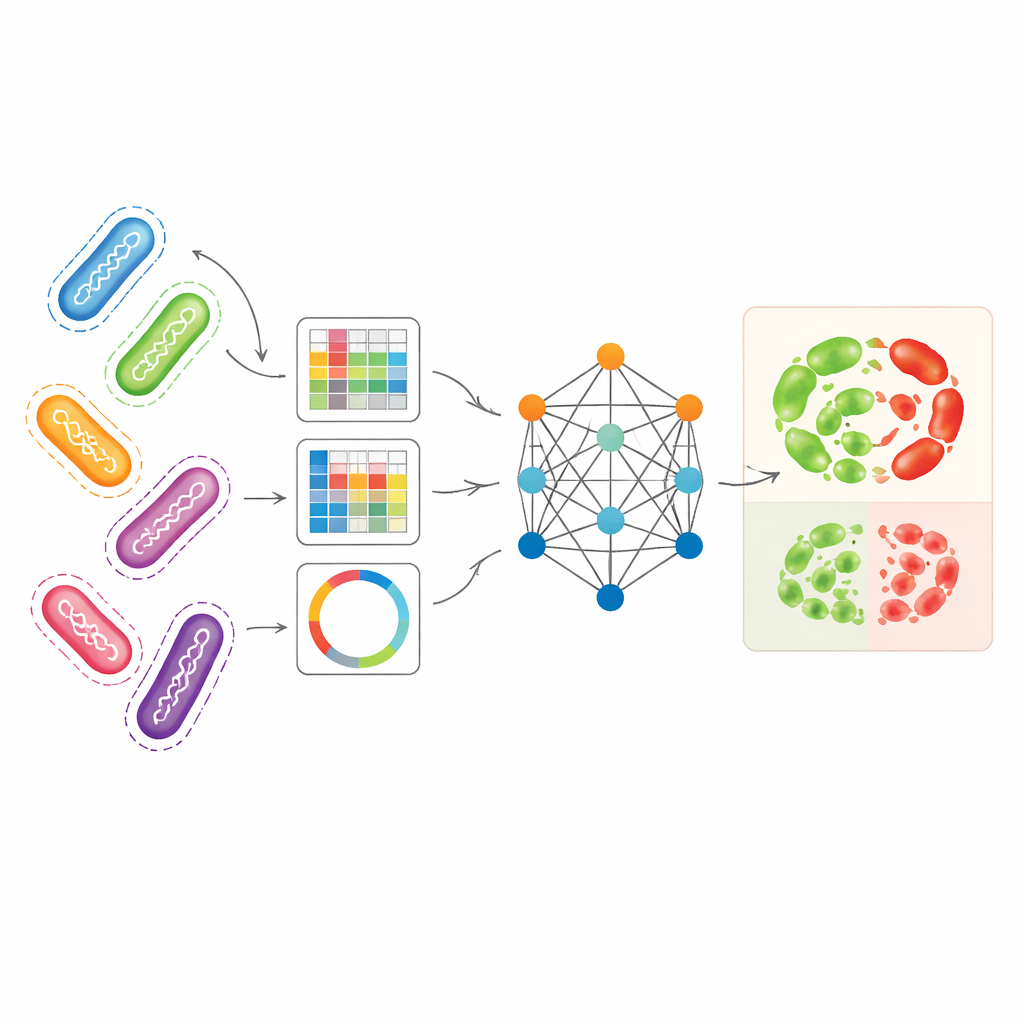
遅い培養検査からデジタルDNA検査へ
現在、多くの病院では依然として培養ベースの検査に頼っており、細菌を培養して各種薬剤に曝露し成長が阻害されるかを調べます。確実ですが時間と手間がかかります。一方で、細菌ゲノムの全配列決定は安価で容易になり、詳細な情報が大量に得られるようになりました。問題は細菌DNAが極めて高次元であり何百万もの構成要素を含むため、これをコンピュータが抗菌薬耐性を予測しやすい形式に変換する統一された方法がないことです。従来のツールは既知の耐性遺伝子や単純なパターンに注目することが多く、耐性が単一の変異に起因する場合には有効ですが、多数の微小な変化が相互作用する場合には限界があります。
異なるゲノム表現を一つに統合する
研究者たちは、細菌ゲノムを表す複数の補完的な表現を同時に活用することを目指しました。主な実験対象は院内感染で複雑な耐性パターンを示すPseudomonas aeruginosaです。ひとつの表現であるunitigは、リファレンスゲノムに依存せずに繰り返し現れるDNA断片を捉えます。別の表現は特定位置での小さなDNA変化を追跡し、さらに別の表現は耐性に関連する遺伝子を画像のようなパターンに変換して短い配列の配列状況を要約します。これら単独でも標準的な機械学習モデルで比較的良好な耐性予測が可能で、特にある抗生物質についてはunitigが有効でした。しかし各表現は生物学的な情報の一部を欠き、個別に使うとゲノムが持つ豊富な情報を十分に活用できません。
類縁株から学ぶグラフベースのモデル
AMR-GNNはグラフニューラルネットワークという深層学習の一形式を用いており、各細菌分離株を点(ノード)として扱い、遺伝的に類似した分離株同士を辺でつなぎます。この構成では、各分離株の詳細なunitigプロファイルが主要な特徴ベクトルとなり、他のゲノム表現がグラフ上でどのように分離株を結びつけるかを定義します。モデルはこれらの接続を通じて情報を伝搬させ、関連するゲノム間で共有されるパターンから学習します。単純なクローナル関係(近縁だが耐性が異なる場合)に惑わされないように、著者らは同一の遺伝的系統グループに属する分離株をつなぐ辺を意図的に除去しました。この「デカップリング」ステップにより、ネットワークは広い系統ラベルに頼るショートカットではなく、耐性に関連する具体的なDNA特徴に注目することを促されます。
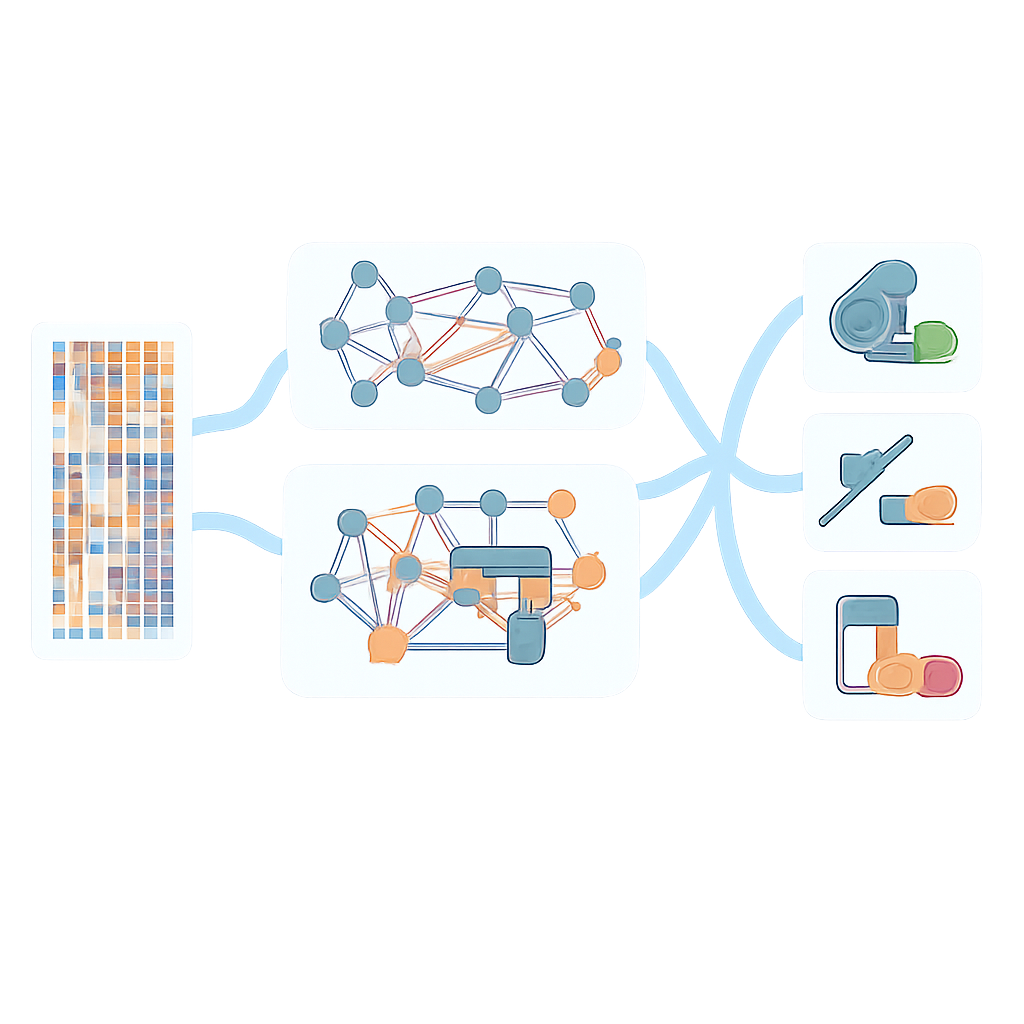
細菌種と薬剤を超えた強化された予測力
チームがAMR-GNNを単一のゲノム表現に依存する単純なモデルと比較したところ、グラフベースのアプローチはP. aeruginosaで試験した12種類の抗生物質のほぼすべてで性能を向上させ、とりわけ従来予測が難しかった薬剤で大きな改善が得られました。モデルは独立したテストデータセットにもより良く一般化しましたが、依然として訓練データ外では性能がやや低下し、より大規模で多様なゲノムコレクションの必要性を示しています。P. aeruginosaに加え、研究者たちはEscherichia coli、Klebsiella pneumoniae、Staphylococcus aureus、Enterococcus faeciumなど他の主要病原体からの23,000を超えるゲノムにAMR-GNNを適用しました。多くの臨床的に重要な抗生物質に対するほとんどの種–薬剤組み合わせで、このフレームワークは非常に高い精度に達し、既知の耐性遺伝子の精選リストに依存する広く使われるルールベースのツールを上回りました。
ブラックボックスモデルをより説明可能にする
臨床用途での重要な懸念は、なぜそのようなAIシステムが特定の予測を出すのかについて洞察を提供できるかどうかです。チームは解釈可能性手法を適用して、モデルの判断に大きく寄与するDNA特徴をたどることでこれに取り組みました。モデルの性能が最も高かった薬剤では、AMR-GNNはフルオロキノロン系抗生物質の古典的な標的変異のように、多くの既知の耐性遺伝子や変異を強調しました。また、よりよく理解されていない遺伝子であっても、細菌の増殖を抑えるために必要な薬剤濃度の上昇と強く関連する変化を示すものが見つかり、実験室での追試の新たな候補を示唆しました。耐性を予測すると同時に潜在的な生物学的駆動因子を指摘する能力は、純粋な予測と機序的理解の橋渡しに役立ちます。
将来の患者ケアへの示唆
本質的に、本研究は複数のDNA「ビュー」をグラフベースの深層学習モデル内で組み合わせることで、細菌ゲノムからの抗生物質耐性予測が大幅に改善されうることを示しています。AMR-GNNは拡張性が高く、遺伝子発現測定や臨床情報など他のデータ型にも拡張できる解釈可能なフレームワークとして提示されています。より大規模で地理的に多様なデータセットや前向き臨床試験など、さらに取り組むべき課題はありますが、このアプローチは患者試料から直接得られた細菌ゲノム配列が迅速に適切な薬剤選択を導き、耐性感染の拡大を抑える未来に近づける可能性を示しています。
引用: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
キーワード: 抗菌薬耐性, グラフニューラルネットワーク, 細菌ゲノミクス, 機械学習, 抗生物質感受性予測