Clear Sky Science · ru
AMR-GNN: многоформатная графовая нейронная сеть для предсказания геномной антимикробной резистентности
Почему важно прогнозировать устойчивость к препаратам
Инфекции, устойчивые к антибиотикам, являются одной из главных медицинских угроз нашего времени и уносят более миллиона жизней ежегодно. Врачам остро нужны более быстрые способы определить, какие антибиотики подойдут при конкретной инфекции, однако традиционные лабораторные тесты могут занимать несколько дней. В этом исследовании предложена новая система на основе искусственного интеллекта, названная AMR-GNN, которая анализирует полный ДНК-последовательность бактерий и предсказывает, будут ли они устойчивы или чувствительны к разным антибиотикам, что потенциально открывает путь к рекомендациям в тот же день у постели больного.
От медленных культур к цифровым ДНК‑тестам
Сегодня в большинстве больниц по-прежнему используют культуры: бактерии выращивают в лаборатории и подвергают воздействию различных препаратов, чтобы увидеть, какие из них останавливают рост. Хотя этот подход надежен, он медленный и трудоемок. В то же время секвенирование полных бактериальных геномов стало дешевле и проще, что порождает огромные объемы детальной информации. Проблема в том, что бактериальная ДНК чрезвычайно высокоразмерна, содержит миллионы строительных блоков, и нет единого общепринятого способа превратить этот генетический код в формат, удобный для вычислительных моделей, предсказывающих резистентность. Ранние инструменты часто фокусировались на нескольких известных генах резистентности или простых паттернах — это работает, когда устойчивость вызвана одной мутацией, но не учитывает ситуации, где взаимодействует множество тонких изменений.
Объединение разных геномных представлений в единую картину
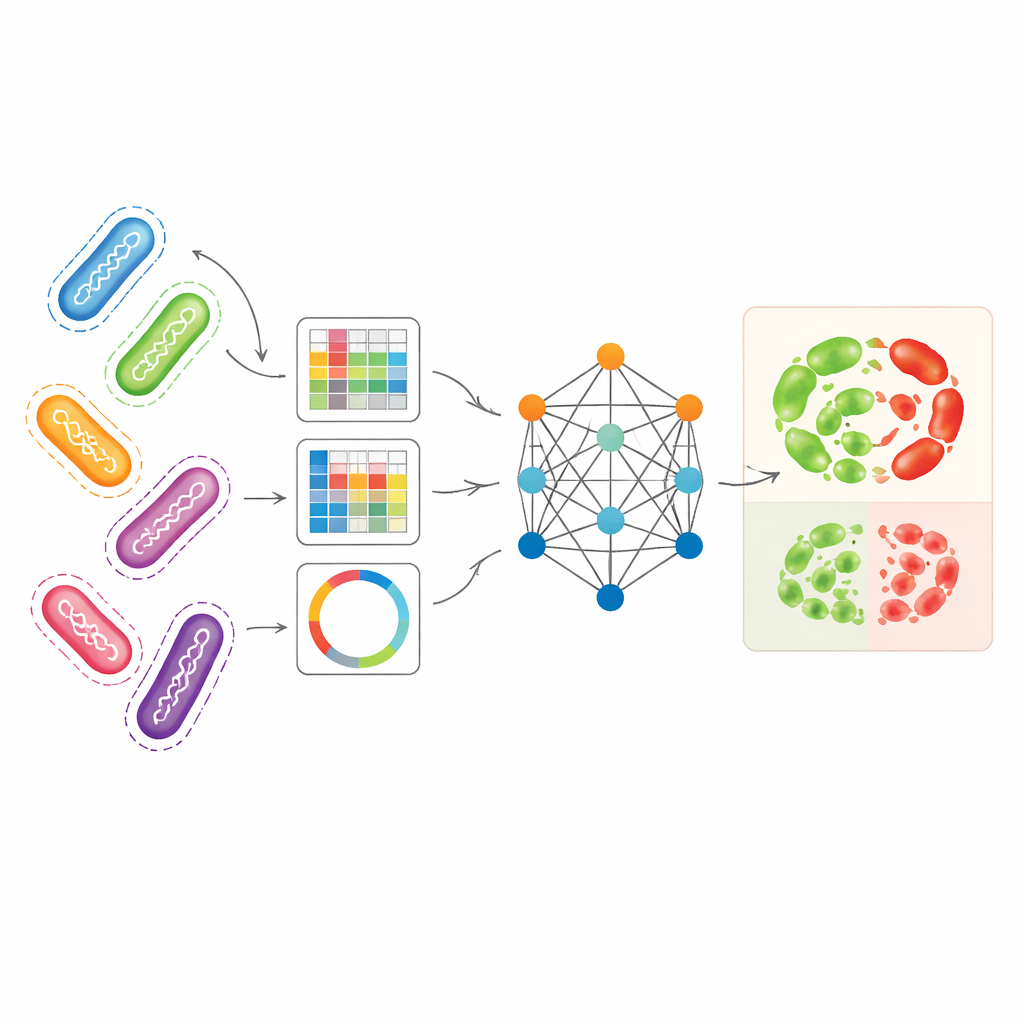
Авторы поставили цель использовать несколько взаимодополняющих способов представления бактериальных геномов одновременно. В качестве основной тестовой задачи они выбрали Pseudomonas aeruginosa — внутрибольничный патоген со особенно сложными паттернами резистентности. Одно представление, называемое unitigs, фиксирует повторяющиеся фрагменты ДНК без опоры на референтный геном. Другое отслеживает мелкие изменения ДНК в конкретных позициях, а третье преобразует выбранные гены, связанные с резистентностью, в изображения, которые суммируют расположение коротких участков ДНК. Каждое представление по отдельности уже позволяло стандартным моделям машинного обучения предсказывать резистентность с приемлемой точностью, особенно unitigs для некоторых антибиотиков. Но каждое представление отражает лишь часть биологической истории, и их раздельное использование недоиспользует богатство исходных геномных данных.
Как графовая модель учится на родственных штаммах
AMR-GNN использует разновидность глубокого обучения, известную как графовая нейронная сеть, которая рассматривает каждый бактериальный изолят как точку (узел) и соединяет генетически близкие изоляты связями (ребрами). В этой схеме детализированный профиль unitig каждого изолята формирует его главный вектор признаков, тогда как другие геномные представления определяют, как изоляты связаны в графе. Модель передает информацию по этим связям, что позволяет ей учиться на паттернах, общих для родственных геномов. Чтобы не вводить модель в заблуждение простыми клонами — когда бактерии близкородственны, но различаются по резистентности по причинам, которые модель должна выявить — авторы намеренно удаляли ребра, связывающие изоляты из одной генетической линии. Этот шаг «развязывания» заставляет сеть больше обращать внимание на конкретные ДНК‑признаки, ассоциированные с резистентностью, а не использовать широкие метки линии как быстрые подсказки.
Более сильные прогнозы для разных бактерий и препаратов
При сравнении AMR-GNN с более простыми моделями, опиравшимися на отдельные геномные представления, графовый подход улучшил результаты для почти всех 12 протестированных антибиотиков у P. aeruginosa, с наибольшими приростами для препаратов, которые раньше было труднее всего предсказать. Модель также лучше обобщалась на независимые тестовые наборы, хотя производительность всё же несколько падала вне тренирующих данных, что подчёркивает необходимость более крупных и разнообразных коллекций геномов. За пределами P. aeruginosa исследователи применили AMR-GNN к более чем 23 000 геномов других основных патогенов, включая Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus и Enterococcus faecium, по множеству клинически важных антибиотиков. В большинстве сочетаний вид/препарат фреймворк достигал очень высокой точности и превосходил широко используемые правило‑ориентированные инструменты, зависящие от куратированных списков известных генов резистентности.
Делая «черный ящик» более объяснимым
Важная проблема для клинического применения — сможет ли такая ИИ‑система объяснить, почему она делает то или иное предсказание. Команда занялась этой задачей, применив методы интерпретируемости, которые отслеживают, какие ДНК‑признаки вносят наибольший вклад в решения модели. Для препаратов, где модель показывала лучшие результаты, AMR-GNN выделяла многие известные гены и мутации, связанные с резистентностью, например классические мишени фторхинолоновых антибиотиков. Модель также указывала на менее изученные гены, изменения в которых были сильно ассоциированы с повышением концентрации препарата, необходимой для остановки роста бактерий, предлагая новые кандидаты для лабораторной проверки. Эта способность как предсказывать резистентность, так и отмечать потенциальные биологические драйверы помогает преодолеть разрыв между чистым предсказанием и механистическим пониманием.
Что это значит для будущей помощи пациентам
По сути, работа показывает, что объединение нескольких «взглядов» на ДНК внутри графовой модели глубокого обучения может существенно улучшить предсказание антибиотикорезистентности по бактериальным геномам. AMR-GNN представлен как гибкий, объяснимый фреймворк, который можно расширить на другие типы данных, такие как измерения активности генов или клиническая информация. Хотя требуется дополнительная работа — в особенности более крупные, географически разнообразные наборы данных и проспективные клинические испытания — подход приближает нас к будущему, в котором последовательность бактериального генома, полученная непосредственно из образца пациента, сможет быстро направить врача к правильному препарату и помочь замедлить распространение устойчивых инфекций.
Цитирование: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
Ключевые слова: антимикробная резистентность, графовые нейронные сети, бактериальная геномика, машинное обучение, предсказание чувствительности к антибиотикам