Clear Sky Science · nl
AMR-GNN: een multi-representatie graf-neuraal-netwerkframework om genomische voorspellingen van antimicrobiële resistentie mogelijk te maken
Waarom het voorspellen van medicijnresistentie ertoe doet
Infecties die resistent zijn tegen antibiotica behoren tot de grootste medische bedreigingen van onze tijd en eisen jaarlijks meer dan een miljoen levens. Artsen hebben dringend snellere methoden nodig om te bepalen welke antibiotica geschikt zijn voor een specifieke infectie, maar traditionele laboratoriumtesten kunnen enkele dagen duren. Deze studie introduceert een nieuw kunstmatig-intelligentieraamwerk, AMR-GNN, dat de volledige DNA-sequentie van bacteriën leest en voorspelt of ze resistent of gevoelig zijn voor verschillende antibiotica — een stap die kan bijdragen aan richtlijnen voor dezelfde dag bij het bed van de patiënt.
Van trage kweektesten naar digitale DNA-tests
Tegenwoordig vertrouwen veel ziekenhuizen nog op kweekgebaseerde testen: bacteriën worden in het laboratorium gekweekt en aan verschillende middelen blootgesteld om te zien welke hun groei stoppen. Hoewel betrouwbaar, is deze aanpak traag en arbeidsintensief. Tegelijkertijd is het sequentiëren van volledige bacteriële genomen goedkoper en eenvoudiger geworden, wat enorme hoeveelheden gedetailleerde informatie oplevert. De uitdaging is dat bacterieel DNA extreem hoog-dimensionaal is, met miljoenen bouwstenen, en er geen eenduidige methode bestaat om deze genetische code om te zetten in een formaat dat computers gemakkelijk kunnen gebruiken om resistentie te voorspellen. Eerdere hulpmiddelen concentreerden zich vaak op een paar bekende resistentiegenen of eenvoudige patronen; dat werkt goed wanneer resistentie door één enkele mutatie veroorzaakt wordt, maar faalt wanneer veel subtiele veranderingen op elkaar inwerken.
Verschillende genomische gezichtspunten combineren tot één beeld
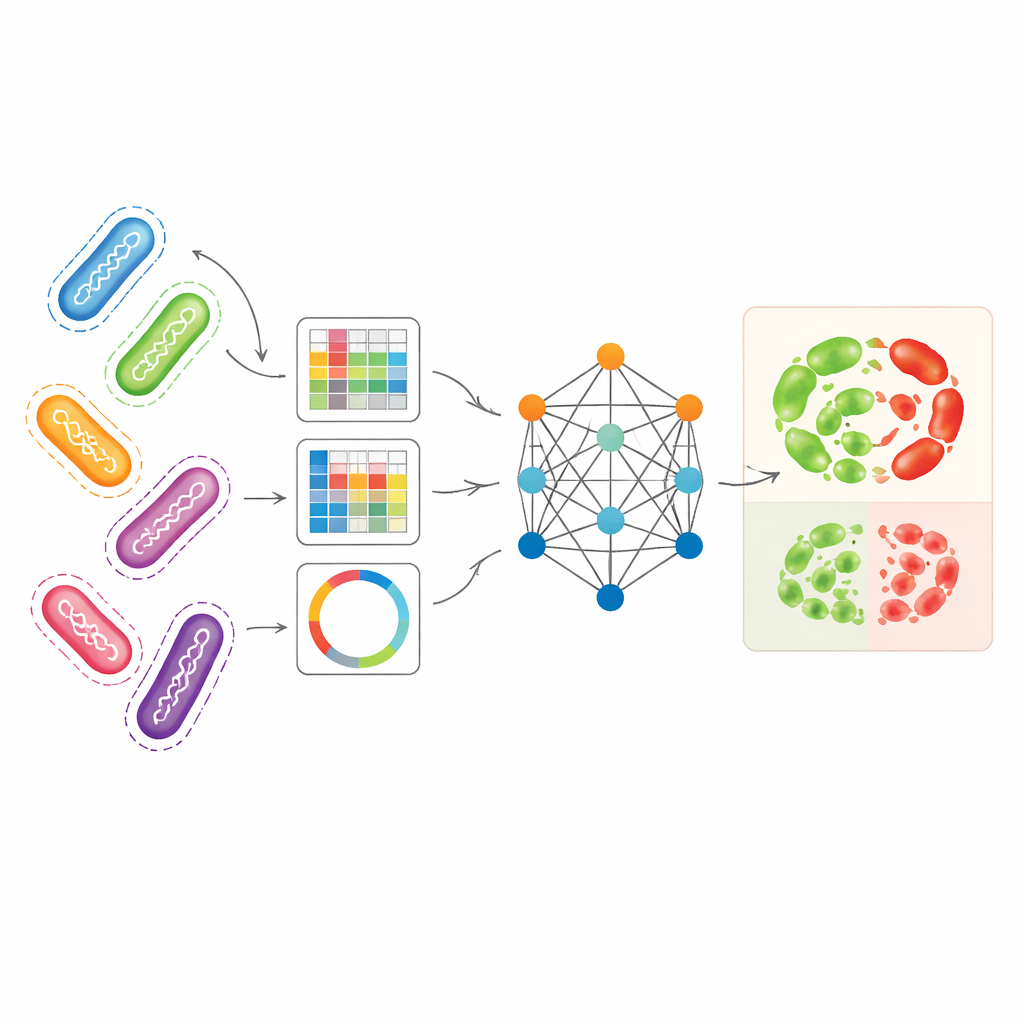
De onderzoekers wilden meerdere complementaire manieren om bacteriële genomen te representeren tegelijkertijd benutten. Ze gebruikten Pseudomonas aeruginosa — een in het ziekenhuis verworven pathogeen met bijzonder complexe resistentiepatronen — als hoofdcasus. Eén representatie, unitigs genoemd, vangt terugkerende DNA-fragmenten zonder afhankelijk te zijn van een referentiegenoom. Een andere representatie volgt kleine DNA-veranderingen op specifieke posities, terwijl een derde geselecteerde resistentie-gerelateerde genen omzet in beeldachtige patronen die samenvatten hoe korte DNA-stukken zijn gerangschikt. Op zichzelf lieten deze representaties standaard machine-learningmodellen al toe om resistentie met redelijke nauwkeurigheid te voorspellen, vooral unitigs voor bepaalde antibiotica. Maar elk gezichtspunt mist een deel van het biologische verhaal, en ze afzonderlijk gebruiken onderbenut de rijkdom van de onderliggende genoomdata.
Hoe het graafgebaseerde model leert van verwante stammen
AMR-GNN gebruikt een vorm van deep learning die bekend staat als een graf-neuraal netwerk, waarbij elke bacteriële isolate als een punt (een knoop) wordt behandeld en isolates die genetisch vergelijkbaar zijn met elkaar verbonden worden met randen. In deze opzet vormt het gedetailleerde unitig-profiel van elke isolate de belangrijkste feature-vector, terwijl de andere genomische gezichtspunten bepalen hoe isolates in de graaf verbonden zijn. Het model geeft vervolgens informatie door langs deze verbindingen, waardoor het kan leren van patronen die gedeeld worden door verwante genomen. Om te voorkomen dat het model misleid wordt door eenvoudige klonale relaties — waarbij bacteriën nauw verwant zijn maar om redenen die het model moet ophelderen verschillen in resistentie — verwijderden de auteurs doelbewust randen die isolates binnen dezelfde genetische lijn verbonden. Deze "ontkoppeling" dwingt het netwerk om meer aandacht te besteden aan de specifieke DNA-eigenschappen die met resistentie samenhangen, in plaats van te vertrouwen op brede lijnlabels als kortere routes.
Sterkere voorspellingen over bacteriën en geneesmiddelen heen
Toen het team AMR-GNN vergeleek met eenvoudigere modellen die op één genomisch gezichtspunt leunden, verbeterde de graafgebaseerde aanpak de prestaties voor bijna alle 12 geteste antibiotica bij P. aeruginosa, met de grootste winst voor middelen die eerder het moeilijkst voorspelbaar waren. Het model generaliseerde ook beter naar onafhankelijke testdatasets, hoewel de prestaties buiten de trainingsdata nog steeds enigszins afnamen, wat het belang benadrukt van grotere en diversere genoomcollecties. Buiten P. aeruginosa pasten de onderzoekers AMR-GNN toe op meer dan 23.000 genomen van andere belangrijke pathogenen, waaronder Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus en Enterococcus faecium, voor veel klinisch relevante antibiotica. In de meeste soort–geneesmiddelcombinaties behaalde het raamwerk zeer hoge nauwkeurigheid en overtrof het veelgebruikte regelgebaseerde tools die afhankelijk zijn van gecureerde lijsten met bekende resistentiegenen.
Zwarte-doosmodellen beter verklaarbaar maken
Een belangrijke zorg voor klinisch gebruik is of zo’n AI-systeem inzicht kan geven in waarom het een specifieke voorspelling doet. Het team ging hiermee om door interpretatiemethoden toe te passen die terugvolgen welke DNA-features het meest bijdragen aan de beslissingen van het model. Voor geneesmiddelen waarbij het model het best presteerde, belichtte AMR-GNN veel bekende resistentiegenen en mutaties, zoals klassieke doelwitten van fluoroquinoloonantibiotica. Het wees ook op minder goed begrepen genen waarvan veranderingen sterk geassocieerd waren met hogere concentraties van middelen die nodig zijn om bacteriële groei te remmen, wat nieuwe kandidaten voor laboratoriumonderzoek suggereert. Deze mogelijkheid om zowel resistentie te voorspellen als potentiële biologische drijfveren te markeren helpt de kloof te overbruggen tussen zuivere voorspelling en mechanistisch begrip.
Wat dit betekent voor toekomstige patiëntenzorg
In wezen toont dit werk aan dat het combineren van meerdere DNA-"gezichten" binnen een graafgebaseerd deep-learningmodel de voorspelling van antibioticareactie uit bacteriële genomen aanzienlijk kan verbeteren. AMR-GNN wordt gepresenteerd als een flexibel, uitlegbaar raamwerk dat kan worden uitgebreid naar andere datatypes, zoals genactiviteitsmetingen of klinische informatie. Hoewel er meer werk nodig is — met name grotere, geografisch diverse datasets en prospectieve klinische trials — brengt deze benadering ons dichter bij een toekomst waarin een bacterieel genoom, rechtstreeks verkregen uit een patiëntmonster, artsen snel kan wijzen op het juiste middel en zo kan helpen de verspreiding van resistente infecties te vertragen.
Bronvermelding: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
Trefwoorden: antimicrobiële resistentie, graf-neurale netwerken, bacteriële genomica, machine learning, voorspelling van antibioticagevoeligheid