Clear Sky Science · he
AMR-GNN: מסגרת רשת עצבית גרפית רב־ייצוגית לאפשר חיזוי עמידות אנטי־מיקרוביאלית ממידע גנומי
למה חשוב לחזות עמידות לתרופות
זיהומים עמידים לאנטיביוטיקה מהווים אחד האיומים הרפואיים המרכזיים של זמננו, והורגים יותר ממיליון איש בשנה. לרופאים נחוצים דרכים מהירות יותר להחליט אילו אנטיביוטיקות יעבדו עבור זיהום מסוים, אך בדיקות מעבדה מסורתיות עלולות לקחת מספר ימים. המחקר הזה מציג מסגרת בינה מלאכותית חדשה, בשם AMR-GNN, שקוראת את הרצף הגנומי המלא של חיידקים ומנבאת האם יהיו עמידים או רגישים לאנטיביוטיקה מסוימת, ובכך עשויה לאפשר הנחיה באותו היום ליד המיטה.
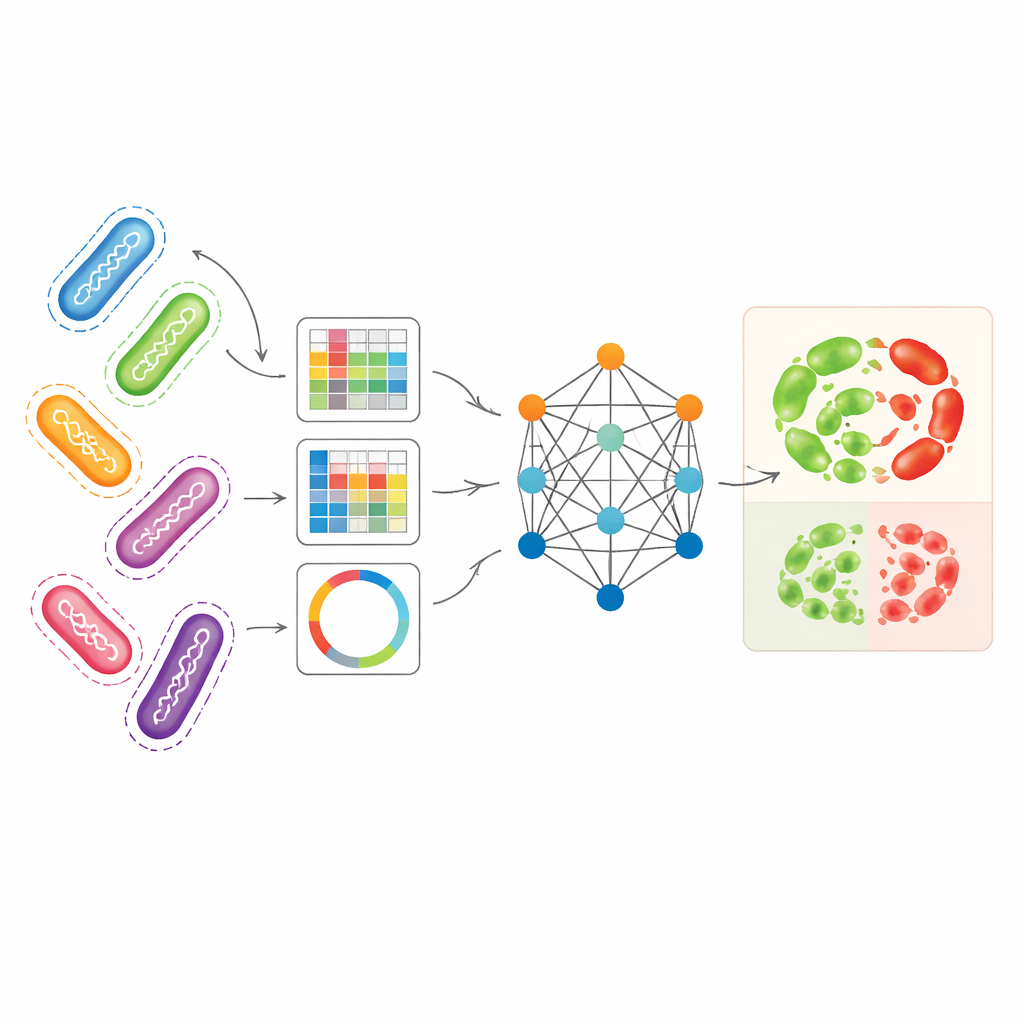
מתרביות איטיות לבדיקות דיגיטליות של DNA
כיום, רוב בתי החולים עדיין מסתמכים על בדיקות מבוססות תרבית: מגדלים חיידקים במעבדה ומחשפים אותם לתרופות שונות כדי לראות מה עוצר את הצמיחה. למרות שהשיטה אמינה, היא איטית ותובענית מבחינת עבודה. במקביל, רצפי הגנומים המלאים של חיידקים הפכו לזולים וקלים יותר להשגה, ומייצרים כמויות עצומות של מידע מפורט. האתגר הוא ש‑DNA חיידקי הוא בעל מימדיות גבוהה מאוד, מכיל מיליוני יחידות בניין, ואין שיטה אחת מוסכמת להמיר את הקוד הגנטי לפורמט שקל למחשבים להשתמש בו לחיזוי עמידות. כלים קודמים התרכזו לעיתים בכמה גנים מוכרים לעמידות או בדפוסים פשוטים — מה שעובד היטב כשהעמידות נגרמת על ידי מוטציה בודדת, אך נכשל כששינויים עדינים רבים מתקיימים באינטראקציה.
שילוב מבטים גנומיים שונים לתמונה אחת
החוקרים שאפו לנצל מספר דרכים משלימות לייצוג גנומי של חיידקים בו‑זמנית. הם השתמשו ב‑Pseudomonas aeruginosa — פתוגן הנרכש בבתי חולים עם דפוסי עמידות מורכבים במיוחד — כמודל ראשי. ייצוג אחד, שנקרא unitigs, תופס קטעי DNA החוזרים על עצמם ללא תלות בגנום ייחוס. ייצוג אחר עוקב אחרי שינויים קטנים ב‑DNA במיקומים ספציפיים, בעוד שיוצג שלישי ממיר גנים שבעלי קשר לעמידות לתבניות דמוי‑תמונה שמסכמות כיצד מקטעי DNA קצרים מסודרים. כל אחד מהייצוגים האלו בפני עצמו איפשר למודלים סטנדרטיים של למידת מכונה לחזות עמידות בדיוק סביר, במיוחד unitigs עבור אנטיביוטיקות מסוימות. אבל כל מבט מפספס חלק מהסיפור הביולוגי, ושימוש נפרד בהם מנצל באופן חלקי את העושר של נתוני הגנום הבסיסיים.
כיצד המודל המבוסס גרף לומד ממינים קשורים
AMR-GNN משתמש בצורת למידה עמוקה הידועה כרשת עצבית גרפית, שמטפלת בכל איזולט של חיידק כנקודה (צומת) ומחברת איזולטים הדומים גנטית בקישורים (קצוות). במבנה זה, פרופיל ה‑unitig המפורט של כל איזולט מהווה את וקטור התכונות הראשי שלו, בעוד המראות הגנומיות האחרות מגדירות כיצד האיזולטים מקושרים בגרף. המודל מעביר אז מידע לאורך הקישורים הללו, ומאפשר לו ללמוד מתוך דפוסים שמשותפים בין גנומים קרובים. כדי למנוע שהמודל יטעה בקשרים קלוניים פשוטים — שבהם חיידקים קרובים גנטית אך שונים בעמידות מסיבות שהמודל צריך לגלות — המחברים הסירו במכוון קצוות שקישרו איזולטים מאותה קבוצת שושלת גנטית. שלב ה"ניתוק" הזה מאלץ את הרשת לשים יותר לב לתכונות ה‑DNA הספציפיות המקושרות לעמידות, במקום להסתמך על תוויות שושלת רחבות כקיצורי דרך.
חיזויים חזקים יותר בחיידקים ותרופות שונות
כאשר הצוות השווה את AMR-GNN למודלים פשוטים שהסתמכו על מבט גנומי יחיד, הגישה המבוססת גרף שיפרה את הביצועים עבור כמעט כל אחת מ‑12 האנטיביוטיקות שנבדקו ב‑P. aeruginosa, עם השיפורים הגדולים ביותר עבור תרופות שהיו הקשות לחיזוי קודם לכן. המודל גם הכליל טוב יותר לסטי בדיקה עצמאיים, אם כי הביצועים עדיין ירדו במידה מסוימת מחוץ לנתוני האימון, מה שמדגיש את הצורך באוספים גדולים ומגוונים יותר של גנומים. מעבר ל‑P. aeruginosa, החוקרים יישמו את AMR-GNN על יותר מ‑23,000 גנומים מפתוגנים מרכזיים אחרים, כולל Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus ו‑Enterococcus faecium, על פני אנטיביוטיקות קליניות חשובות רבות. ברוב הצירופים של מין–תרופה, המסגרת הגיעה לדיוק גבוה והביאה לתוצאות טובות יותר מכלים מבוססי‑חוקים בשימוש נרחב שתלויים ברשימות מתוחזקות של גנים ידועים לעמידות.
להפוך מודלים "קופסה שחורה" ליותר ניתנים להסבר
דאגה חשובה לשימוש קליני היא האם מערכת כזו של בינה מלאכותית יכולה לספק תובנה מדוע היא מבצעת חיזוי מסוים. הצוות טיפל בכך באמצעות שיטות פרשנות שעוקבות אילו תכונות DNA תורמות ביותר להחלטות המודל. עבור תרופות שבהן המודל הצטיין, AMR-GNN הדגיש גנים ומוטציות ידועים לעמידות, כגון מטרות קלאסיות של אנטיביוטיקות פלואורוקינולון. הוא גם הצביע על גנים פחות מוכרים ששינויים בהם היו קשורים בחוזקה לריכוזי־תרופה גבוהים יותר הדרושים לעצור את צמיחת החיידקים, מה שמציע מועמדים חדשים למעקבים במעבדה. היכולת הזו לחזות עמידות ולסמן מניעים ביולוגיים פוטנציאליים עוזרת לגשר בין חיזוי טהור לבין הבנה מכניסטית.
מה המשמעות לחיי החולה בעתיד
בעיקרו של דבר, עבודה זו מראה ששילוב מספר "מבטי" DNA בתוך מודל למידה עמוקה מבוסס גרף יכול לשפר משמעותית את חיזוי העמידות לאנטיביוטיקה מתוך גנומי חיידקים. AMR-GNN מוצגת כמסגרת גמישה וניתנת לפרשנות שניתן להרחיב לסוגי נתונים אחרים, כגון מדידות פעילות גנים או מידע קליני. בעוד שעדיין נדרש מחקר נוסף — במיוחד אוספים גדולים יותר, גיאוגרפית מגוונים וניסויים קליניים פרוספקטיביים — הגישה מקרבת אותנו לעתיד שבו רצף גנום חיידקי, שהושג ישירות מדגימת מטופל, יוכל במהירות לכוון רופאים לתרופה המתאימה ולעזור להאט את התפשטות הזיהומים העמידים.
ציטוט: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
מילות מפתח: עמידות אנטי־מיקרוביאלית, רשתות עצביות גרפיות, גנומיקה חיידקית, למידת מכונה, חיזוי רגישות לאנטיביוטיקה