Clear Sky Science · ar
AMR-GNN: إطار شبكة عصبية بيانية متعدد التمثيلات لتمكين التنبؤ بالمقاومة المضادة للميكروبات من الجينوم
لماذا يهم التنبؤ بمقاومة الأدوية
تُعدّ العدوى المقاومة للمضادات الحيوية أحد أهم التهديدات الطبية في وقتنا الحالي، حيث تقتل أكثر من مليون شخص سنوياً. يحتاج الأطباء بشكل عاجل إلى طرق أسرع لمعرفة أي المضادات الحيوية ستنجح في علاج عدوى معينة، لكن الاختبارات المختبرية التقليدية قد تستغرق عدة أيام. تقدم هذه الدراسة إطار عمل جديداً للذكاء الاصطناعي، يُدعى AMR-GNN، يقرأ التسلسل الكامل للحمض النووي للبكتيريا ويتنبأ بما إذا كانت مقاومة أو حساسة لمضادات حيوية مختلفة، مما قد يمهد الطريق لتوجيهات في نفس اليوم عند السرير.
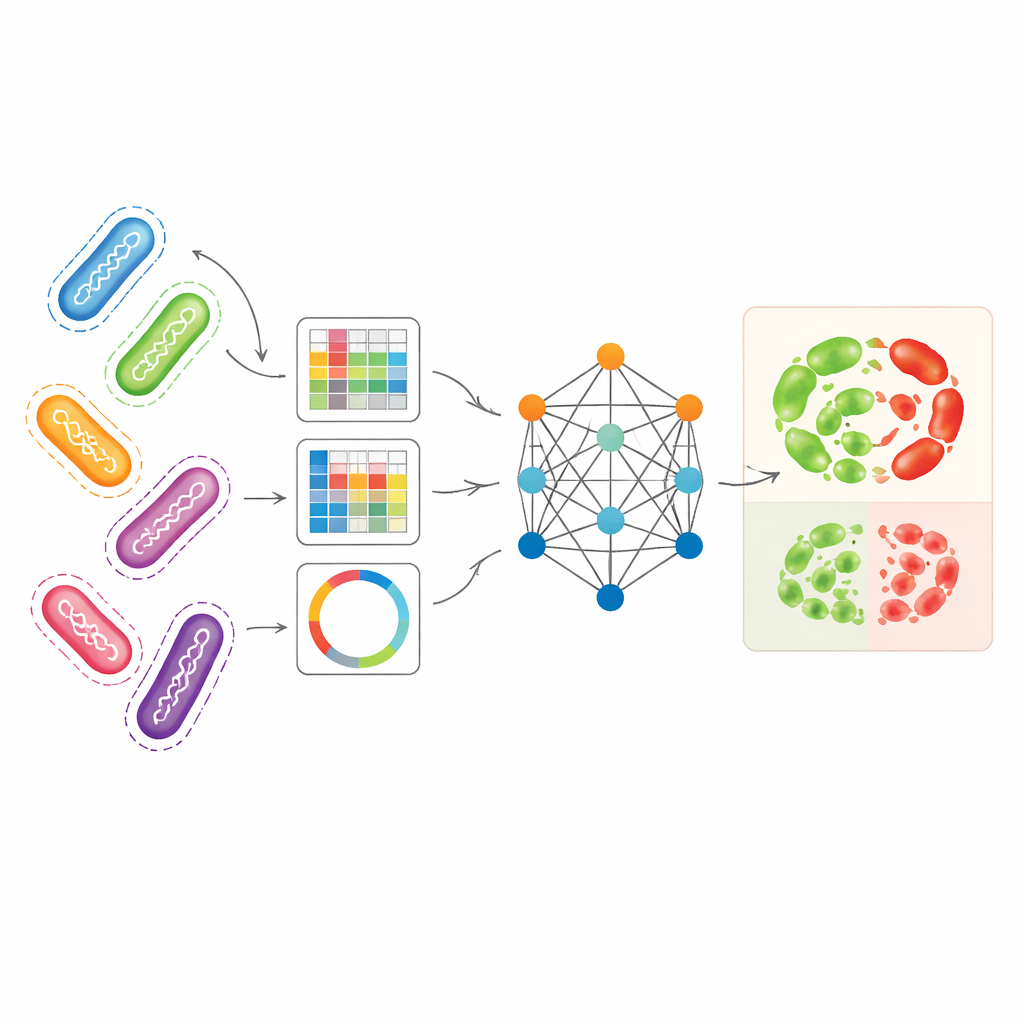
من الزرعات البطيئة إلى اختبارات الحمض النووي الرقمية
يعتمد معظم المستشفيات اليوم على اختبارات قائمة على الزرع: حيث تُنمى البكتيريا في المختبر وتُعرض لمواد دوائية مختلفة لمعرفة أيها يوقف نموها. وعلى الرغم من موثوقيتها، فإن هذه الطريقة بطيئة ومجهدة. في المقابل، أصبح تسلسل الجينومات البكتيرية بالكامل أرخص وأسهل، مما يولد كميات هائلة من المعلومات التفصيلية. التحدي هو أن الحمض النووي البكتيري عالي الأبعاد للغاية، إذ يحتوي على ملايين الوحدات البنائية، ولا توجد طريقة موحدة متفق عليها لتحويل هذا الترميز الجيني إلى صيغة يمكن لأجهزة الحاسوب استخدامها بسهولة لتوقع المقاومة. ركزت الأدوات السابقة غالباً على بعض جينات المقاومة المعروفة أو أنماط بسيطة، وهو ما ينجح عندما تنجم المقاومة عن طفرة واحدة، لكنه يفشل عندما تتفاعل العديد من التغيرات الطفيفة.
دمج وجهات نظر جينومية مختلفة في صورة واحدة
سعى الباحثون إلى استغلال عدة طرق تكميلية لتمثيل الجينومات البكتيرية في آن واحد. استخدموا Pseudomonas aeruginosa — ممرض مرتبط بالمستشفيات له أنماط مقاومة معقدة بشكل خاص — كحالة اختبار رئيسية. تمثيل واحد، يُسمى unitigs، يلتقط شظايا الحمض النووي المتكررة دون الاعتماد على جينوم مرجعي. تمثيل آخر يتتبع تغيرات صغيرة في مواقع محددة، بينما يحول تمثيل ثالث جينات مرتبطة بالمقاومة إلى أنماط شبيهة بالصور تلخّص كيف تُصفّف سلاسل قصيرة من الحمض النووي. بمفردها، سمحت هذه التمثيلات للنماذج التقليدية للتعلم الآلي بتوقع المقاومة بدقة معقولة، لا سيما تمثيل unitigs لبعض المضادات الحيوية. لكن كل منظور يغفل جزءاً من القصة البيولوجية، واستخدامها بشكل منفصل لا يستغل ثراء بيانات الجينوم الأساسية.
كيف يتعلّم النموذج البياني من السلالات المرتبطة
يستخدم AMR-GNN شكلاً من التعلم العميق يعرف بالشبكة العصبية البيانية، التي تعامل كل عزلة بكتيرية كنقطة (عقدة) وتوصل العزلات المتشابهة وراثياً بروابط (حواف). في هذا الإعداد، يشكل ملف وحدة unitig التفصيلي لكل عزلة متجه الميزات الرئيسي لها، بينما تحدد وجهات النظر الجينومية الأخرى كيفية وصل العزلات في الرسم البياني. ثم يمرر النموذج المعلومات عبر هذه الاتصالات، مما يتيح له التعلم من الأنماط المشتركة بين الجينومات المرتبطة. ولتجنّب الالتباس الناجم عن العلاقات النمطية البسيطة — حيث تكون البكتيريا مرتبطة ارتباطاً وثيقاً لكن تختلف في المقاومة لأسباب يجب أن يكتشفها النموذج — أزال المؤلفون عمداً الحواف التي كانت تربط عزلات من نفس مجموعة السلالة الجينية. يُجبر هذا خطوة "فصل الارتباط" الشبكة على إيلاء اهتمام أكبر للميزات الجينية الخاصة المرتبطة بالمقاومة، بدلاً من الاعتماد على تسميات السلالة العريضة كاختصارات.
تنبؤات أقوى عبر بكتيريا وأدوية مختلفة
عندما قارن الفريق AMR-GNN بالنماذج الأبسط التي اعتمدت على وجه جينومي واحد، حسّن النهج القائم على الرسم البياني الأداء لمعظم المضادات الحيوية الـ12 المختبرة في P. aeruginosa، مع تحقيق أكبر مكاسب للأدوية التي كانت أصعب للتنبؤ سابقاً. كما عمم النموذج أداءه بشكل أفضل على مجموعات اختبار مستقلة، رغم أن الأداء انخفض بعض الشيء خارج بيانات التدريب، مما يبرز الحاجة إلى مجموعات جينومات أكبر وأكثر تنوعاً جغرافياً. بالإضافة إلى P. aeruginosa، طبّق الباحثون AMR-GNN على أكثر من 23,000 جينوم من ممرضات رئيسية أخرى، بما في ذلك Escherichia coli وKlebsiella pneumoniae وStaphylococcus aureus وEnterococcus faecium، عبر العديد من المضادات الحيوية ذات الأهمية السريرية. في معظم تركيبات النوع–الدواء، وصل الإطار إلى دقة عالية جداً وتفوق على أدوات قاعدة القواعد المستخدمة على نطاق واسع التي تعتمد على قوائم منسقة من جينات المقاومة المعروفة.
جعل النماذج المظلمة أكثر قابلية للتفسير
مخاوف مهمة للاستخدام السريري تتعلق بما إذا كان بإمكان نظام ذكاء اصطناعي من هذا النوع أن يوضح سبب إصدار تنبؤ معين. تعامل الفريق مع ذلك بتطبيق طرق قابلية التفسير التي تتتبع أي الميزات الجينية تسهم أكثر في قرارات النموذج. للأدوية التي قدم فيها النموذج أفضل أداء، ركز AMR-GNN على العديد من جينات ومضاعفات المقاومة المعروفة، مثل الأهداف الكلاسيكية لمضادات الفلوروكينولون. كما أشار إلى جينات أقل فهماً حتى الآن كانت تغيراتها مرتبطة بقوة بزيادة التركيزات الدوائية المطلوبة لإيقاف نمو البكتيريا، مما يقترح مرشحين جدداً للمتابعة المختبرية. تساعد هذه القدرة على التنبؤ بالمقاومة وفي الوقت نفسه الإشارة إلى السائقين البيولوجيين المحتملين على جسر الفجوة بين التنبؤ المحض والفهم الآلي للآليات.
ماذا يعني ذلك لرعاية المرضى في المستقبل
جوهر هذه الدراسة أن دمج وجهات نظر DNA متعددة داخل نموذج تعلم عميق قائم على الرسم البياني يمكن أن يحسّن بشكل كبير التنبؤ بمقاومة المضادات الحيوية من الجينومات البكتيرية. يُعرض AMR-GNN كإطار مرن وقابل للتفسير يمكن توسيعه ليشمل أنواع بيانات أخرى، مثل قياسات نشاط الجينات أو المعلومات السريرية. ورغم أن هناك حاجة إلى مزيد من العمل — لا سيما مجموعات بيانات أكبر ومتنوعة جغرافياً وتجارب سريرية مستقبلية — فإن هذا النهج يقربنا من مستقبل يمكن فيه لتسلسل جينوم البكتيريا، المستخرج مباشرة من عينة المريض، أن يوجه الأطباء بسرعة نحو الدواء المناسب ويساعد في إبطاء انتشار العدوى المقاومة.
الاستشهاد: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
الكلمات المفتاحية: المقاومة المضادة للميكروبات, الشبكات العصبية البيانية, علم الجينات البكتيري, التعلّم الآلي, التنبؤ بحساسية المضادات الحيوية