Clear Sky Science · pt
AMR-GNN: uma estrutura de rede neural gráfica de múltiplas representações para viabilizar a predição genômica de resistência antimicrobiana
Por que prever resistência a medicamentos importa
Infecções resistentes a antibióticos são uma das maiores ameaças médicas do nosso tempo, matando mais de um milhão de pessoas por ano. Os médicos precisam com urgência de métodos mais rápidos para saber quais antibióticos serão eficazes em cada infecção, mas os testes laboratoriais tradicionais podem levar vários dias. Este estudo apresenta uma nova estrutura de inteligência artificial, chamada AMR-GNN, que lê a sequência completa do DNA de bactérias e prevê se elas serão resistentes ou suscetíveis a diferentes antibióticos, abrindo potencialmente o caminho para orientações no mesmo dia junto ao leito do paciente.
De culturas lentas para testes digitais de DNA
Hoje, a maioria dos hospitais ainda depende de testes baseados em cultura: as bactérias são cultivadas no laboratório e expostas a vários fármacos para verificar quais impedem seu crescimento. Apesar de confiável, essa abordagem é lenta e trabalhos a. Ao mesmo tempo, o sequenciamento de genomas bacterianos inteiros tornou-se mais barato e mais fácil, gerando enormes quantidades de informação detalhada. O desafio é que o DNA bacteriano é extremamente de alta dimensão, contendo milhões de unidades, e não existe uma única maneira consensual de converter esse código genético em um formato que computadores possam usar facilmente para prever resistência a medicamentos. Ferramentas anteriores costumavam focar em alguns genes de resistência conhecidos ou em padrões simples, o que funciona bem quando a resistência se deve a uma única mutação, mas falha quando muitas mudanças sutis interagem.
Combinando diferentes visões genômicas em uma única imagem
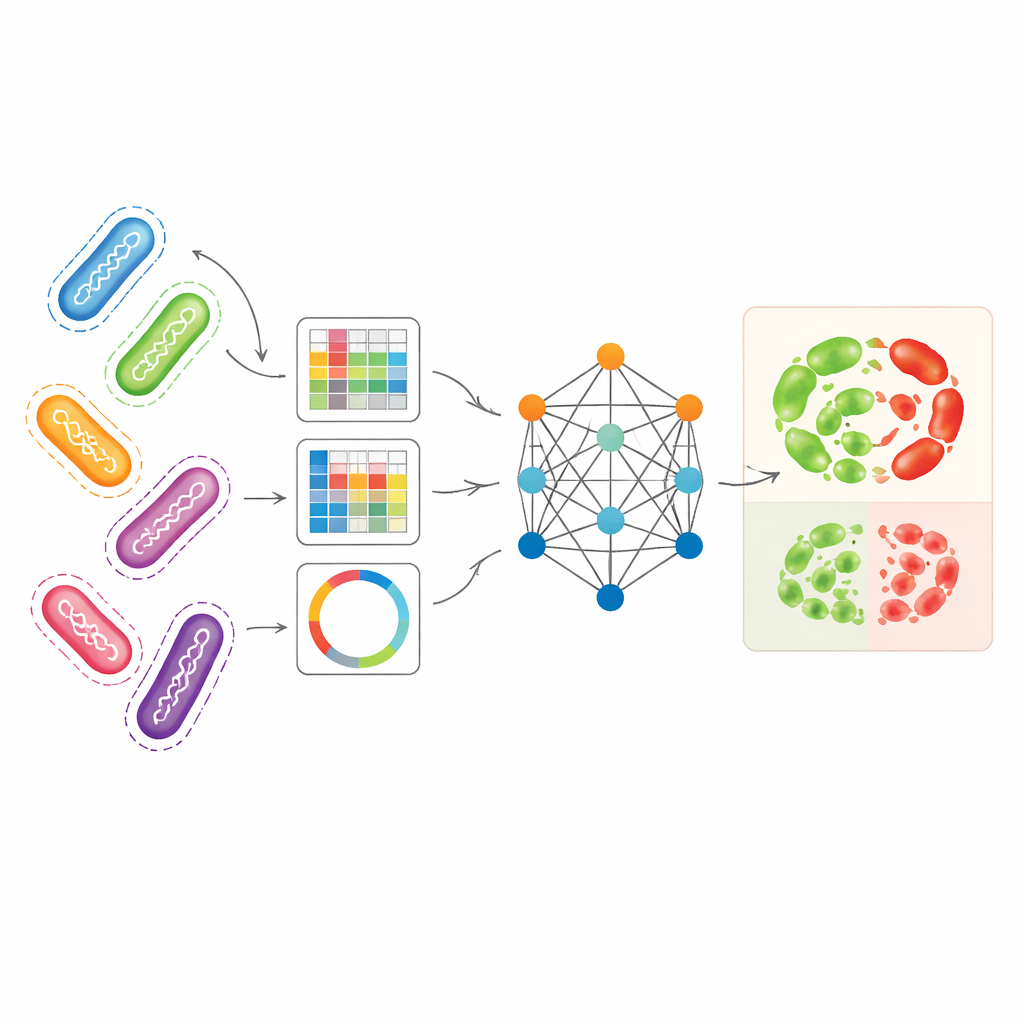
Os pesquisadores buscaram explorar várias maneiras complementares de representar genomas bacterianos simultaneamente. Eles usaram Pseudomonas aeruginosa — um patógeno adquirido em hospitais com padrões de resistência particularmente complexos — como caso de teste principal. Uma representação, chamada unitigs, captura fragmentos de DNA recorrentes sem depender de um genoma de referência. Outra representação rastreia pequenas alterações de DNA em posições específicas, enquanto uma terceira converte genes selecionados relacionados à resistência em padrões semelhantes a imagens que resumem como trechos curtos de DNA estão organizados. Isoladamente, essas representações já permitiam que modelos padrão de aprendizado de máquina previssem resistência com precisão razoável, especialmente as unitigs para certos antibióticos. Mas cada visão perde parte da história biológica, e usá-las separadamente subutiliza a riqueza dos dados genômicos subjacentes.
Como o modelo baseado em grafo aprende com linhagens relacionadas
O AMR-GNN usa uma forma de aprendizado profundo conhecida como rede neural gráfica, que trata cada isolado bacteriano como um ponto (nó) e conecta isolados geneticamente semelhantes com ligações (arestas). Nesse arranjo, o perfil detalhado de unitigs de cada isolado forma seu principal vetor de características, enquanto as outras visões genômicas definem como os isolados estão conectados no grafo. O modelo então transmite informações ao longo dessas conexões, permitindo-lhe aprender com padrões compartilhados entre genomas relacionados. Para evitar ser enganado por relações clonal simples — onde bactérias são intimamente relacionadas, mas diferem em resistência por razões que o modelo precisa identificar — os autores deliberadamente removeram arestas que ligavam isolados do mesmo grupo de linhagem genética. Essa etapa de "desacoplamento" força a rede a prestar mais atenção às características específicas do DNA associadas à resistência, em vez de confiar em rótulos amplos de linhagem como atalhos.
Previsões mais robustas através de bactérias e medicamentos
Quando a equipe comparou o AMR-GNN com modelos mais simples que se apoiavam em visões genômicas únicas, a abordagem baseada em grafo melhorou o desempenho para quase todos os 12 antibióticos testados em P. aeruginosa, com os maiores ganhos para drogas que antes eram mais difíceis de prever. O modelo também generalizou melhor para conjuntos de teste independentes, embora o desempenho ainda caísse um pouco fora dos dados de treinamento, ressaltando a necessidade de coleções maiores e mais diversas de genomas. Além de P. aeruginosa, os pesquisadores aplicaram o AMR-GNN a mais de 23.000 genomas de outros patógenos importantes, incluindo Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus e Enterococcus faecium, abrangendo muitos antibióticos clinicamente relevantes. Na maioria das combinações espécie–droga, a estrutura alcançou precisão muito alta e superou ferramentas baseadas em regras amplamente utilizadas que dependem de listas curadas de genes de resistência conhecidos.
Tornando modelos "caixa-preta" mais explicáveis
Uma preocupação importante para uso clínico é se um sistema de IA desse tipo pode oferecer insight sobre por que faz uma previsão particular. A equipe abordou isso aplicando métodos de interpretabilidade que rastreiam quais características do DNA contribuem mais para as decisões do modelo. Para os medicamentos em que o modelo teve melhor desempenho, o AMR-GNN destacou muitos genes e mutações de resistência conhecidos, como alvos clássicos dos antibióticos fluoroquinolonas. Também apontou genes menos bem compreendidos cujas alterações estavam fortemente associadas a concentrações mais altas de droga necessárias para interromper o crescimento bacteriano, sugerindo novos candidatos para investigação laboratorial. Essa capacidade de tanto prever resistência quanto sinalizar possíveis motores biológicos ajuda a reduzir a lacuna entre predição pura e compreensão mecanística.
O que isso significa para o atendimento futuro ao paciente
Em essência, este trabalho mostra que combinar múltiplas "visões" do DNA dentro de um modelo de aprendizado profundo baseado em grafo pode melhorar substancialmente a predição de resistência a antibióticos a partir de genomas bacterianos. O AMR-GNN é apresentado como uma estrutura flexível e interpretável que pode ser estendida a outros tipos de dados, como medidas de atividade gênica ou informações clínicas. Embora sejam necessários mais estudos — em especial conjuntos de dados maiores, geograficamente variados e ensaios clínicos prospectivos —, a abordagem nos aproxima de um futuro em que a sequência do genoma bacteriano, obtida diretamente da amostra do paciente, possa rapidamente orientar os médicos na escolha do fármaco adequado e ajudar a frear a disseminação de infecções resistentes.
Citação: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
Palavras-chave: resistência antimicrobiana, redes neurais gráficas, genômica bacteriana, aprendizado de máquina, predição de suscetibilidade a antibióticos