Clear Sky Science · sv
AMR-GNN: ett grafneuronätverk med flera representationer för att möjliggöra genomisk prediktion av antibiotikaresistens
Varför det är viktigt att förutsäga läkemedelsresistens
Infektioner orsakade av antibiotikaresistenta bakterier är ett av vår tids stora medicinska hot och dödar mer än en miljon människor varje år. Läkare behöver snabbt veta vilka antibiotika som fungerar för en given infektion, men traditionella laboratorietester kan ta flera dagar. Denna studie presenterar en ny artificiell intelligens-ramverk, kallat AMR-GNN, som läser hela bakteriers DNA-sekvens och förutsäger om de är resistenta eller känsliga mot olika antibiotika, vilket potentiellt kan möjliggöra vägledning samma dag vid patientens sida.
Från långsamma odlingar till digitala DNA-tester
I dag förlitar sig de flesta sjukhus fortfarande på odlingsbaserade tester: bakterier odlas i labbet och utsätts för olika läkemedel för att se vilka som stoppar deras tillväxt. Även om detta är tillförlitligt är det långsamt och arbetsintensivt. Samtidigt har helgenomsekvensering av bakterier blivit billigare och enklare och genererar enorma mängder detaljerad information. Utmaningen är att bakterie-DNA är extremt högdimensionellt, innehållande miljontals byggstenar, och det finns inget enhetligt sätt att omvandla denna genetiska kod till ett format som datorer enkelt kan använda för att förutsäga läkemedelsresistens. Tidigare verktyg fokuserade ofta på ett fåtal kända resistensgener eller enkla mönster, vilket fungerar bra när resistens beror på en enstaka mutation men misslyckas när många subtila förändringar samverkar.
Kombinera olika genomiska vyer till en helhetsbild
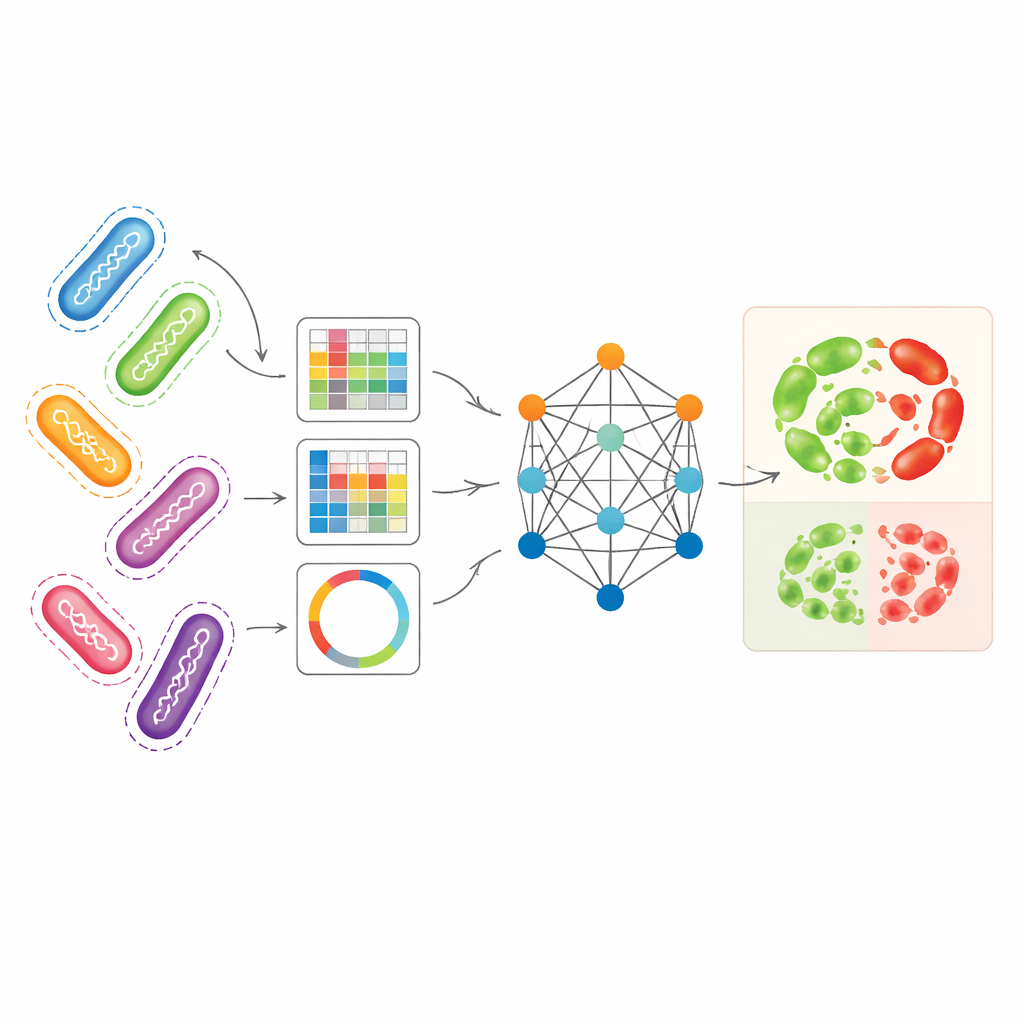
Forskarna strävade efter att använda flera kompletterande sätt att representera bakteriegenom samtidigt. De använde Pseudomonas aeruginosa—en sjukhusförvärvad patogen med särskilt komplexa resistensmönster—som sitt huvudsakliga testfall. En representation, kallad unitigs, fångar återkommande DNA-fragment utan att förlita sig på ett referensgenom. En annan representation spårar små DNA-förändringar på specifika positioner, medan en tredje omvandlar utvalda resistensrelaterade gener till bildliknande mönster som sammanfattar hur korta DNA-sekvenser är ordnade. Var för sig gjorde dessa representationer det möjligt för standardmodeller inom maskininlärning att förutsäga resistens med rimlig noggrannhet, särskilt unitigs för vissa antibiotika. Men varje vy missar delar av den biologiska historien, och att använda dem separat utnyttjar inte rikedomen i det underliggande genomdatat fullt ut.
Hur den grafbaserade modellen lär från släktingstammar
AMR-GNN använder en form av djupinlärning känd som grafneuronätverk, som behandlar varje bakterieisolat som en punkt (en nod) och kopplar ihop isolat som är genetiskt lika med länkar (kanter). I denna uppställning bildar varje isolats detaljerade unitig-profil dess huvudsakliga funktionsvektor, medan de andra genomiska vyerna definierar hur isolaten är sammankopplade i grafen. Modellen för vidare information längs dessa kopplingar, vilket gör att den kan lära sig av mönster som delas mellan besläktade genom. För att undvika att vilseledas av enkla klonala relationer—där bakterier är nära besläktade men skiljer sig i resistens av skäl som modellen bör upptäcka—tog författarna medvetet bort kanter som länkar isolat från samma genetiska linjegrupp. Detta "avkopplingssteg" tvingar nätverket att fästa större uppmärksamhet vid de specifika DNA-egenskaper som är kopplade till resistens, istället för att förlita sig på breda linjeetiketter som genvägar.
Starkare prediktioner över bakterier och läkemedel
När teamet jämförde AMR-GNN med enklare modeller som förlitade sig på enstaka genomiska vyer förbättrade den grafbaserade metoden prestandan för nästan alla av de 12 antibiotika som testades på P. aeruginosa, med de största vinsterna för läkemedel som tidigare var svårast att förutsäga. Modellen generaliserade också bättre till oberoende testdatasätt, även om prestandan fortfarande sjönk något utanför träningsdata, vilket belyser behovet av större och mer varierade genomkollektioner. Utöver P. aeruginosa tillämpade forskarna AMR-GNN på mer än 23 000 genom från andra viktiga patogener, inklusive Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus och Enterococcus faecium, över många kliniskt viktiga antibiotika. I de flesta art–läkemedelskombinationer nådde ramverket mycket hög noggrannhet och överträffade ofta välanvända regelbaserade verktyg som bygger på kurerade listor över kända resistensgener.
Göra svartlådemodeller mer förklarliga
En viktig fråga för klinisk användning är om ett sådant AI-system kan ge insikt i varför det gör en viss förutsägelse. Teamet angrep detta genom att tillämpa tolkningsmetoder som spårar vilka DNA-funktioner som bidrar mest till modellens beslut. För de läkemedel där modellen presterade bäst framhävde AMR-GNN många kända resistensgener och mutationer, såsom klassiska mål för fluorokinolonantibiotika. Det pekade också på mindre kända gener vars förändringar starkt associerades med högre läkemedelskoncentrationer som krävdes för att stoppa bakterietillväxt, vilket föreslår nya kandidater för laboratorieuppföljning. Denna förmåga att både förutsäga resistens och flagga potentiella biologiska drivkrafter hjälper till att överbrygga klyftan mellan ren prediktion och mekanistisk förståelse.
Vad detta betyder för framtida patientvård
Sammanfattningsvis visar detta arbete att kombinationen av flera DNA-"vyer" i en grafbaserad djupinlärningsmodell kan avsevärt förbättra förutsägelsen av antibiotikaresistens från bakteriegenom. AMR-GNN presenteras som ett flexibelt, tolkbart ramverk som kan utvidgas till andra datatyper, såsom mätningar av genaktivitet eller klinisk information. Även om mer arbete krävs—särskilt större, geografiskt varierade dataset och prospektiva kliniska prövningar—tar tillvägagångssättet oss närmare en framtid där en bakteriegenomsekvens, erhållen direkt från ett patientprov, snabbt kan vägleda läkare mot rätt läkemedel och bidra till att bromsa spridningen av resistenta infektioner.
Citering: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
Nyckelord: antimikrobiell resistens, grafneuronätverk, bakteriegenomik, maskininlärning, prediktion av antibiotikas känslighet