Clear Sky Science · it
AMR-GNN: un framework di reti neurali a grafi multi-rappresentazione per abilitare la predizione genomica della resistenza antimicrobica
Perché è importante prevedere la resistenza ai farmaci
Le infezioni resistenti agli antibiotici rappresentano una delle maggiori minacce mediche del nostro tempo, causando oltre un milione di morti l'anno. I medici hanno urgente bisogno di modi più rapidi per capire quali antibiotici funzioneranno per una data infezione, ma i test di laboratorio tradizionali possono richiedere diversi giorni. Questo studio presenta un nuovo framework di intelligenza artificiale, chiamato AMR-GNN, che analizza l'intero sequenziamento del DNA batterico e prevede se i ceppi saranno resistenti o suscettibili a diversi antibiotici, aprendo potenzialmente la strada a indicazioni utili nello stesso giorno al letto del paziente.
Dalle colture lente ai test digitali sul DNA
Oggi la maggior parte degli ospedali fa ancora affidamento su test basati su colture: i batteri vengono coltivati in laboratorio ed esposti a diversi farmaci per vedere quali ne fermano la crescita. Sebbene affidabile, questo approccio è lento e richiede molto lavoro. Nel frattempo, il sequenziamento di interi genomi batterici è diventato più economico e semplice, generando enormi quantità di informazioni dettagliate. La sfida è che il DNA batterico è estremamente ad alta dimensionalità, contenendo milioni di componenti, e non esiste un unico modo condiviso per trasformare questo codice genetico in un formato che i computer possano facilmente usare per prevedere la resistenza ai farmaci. Strumenti precedenti spesso si concentravano su pochi geni di resistenza noti o su pattern semplici, che funzionano bene quando la resistenza è dovuta a una singola mutazione ma falliscono quando molte variazioni sottili interagiscono.
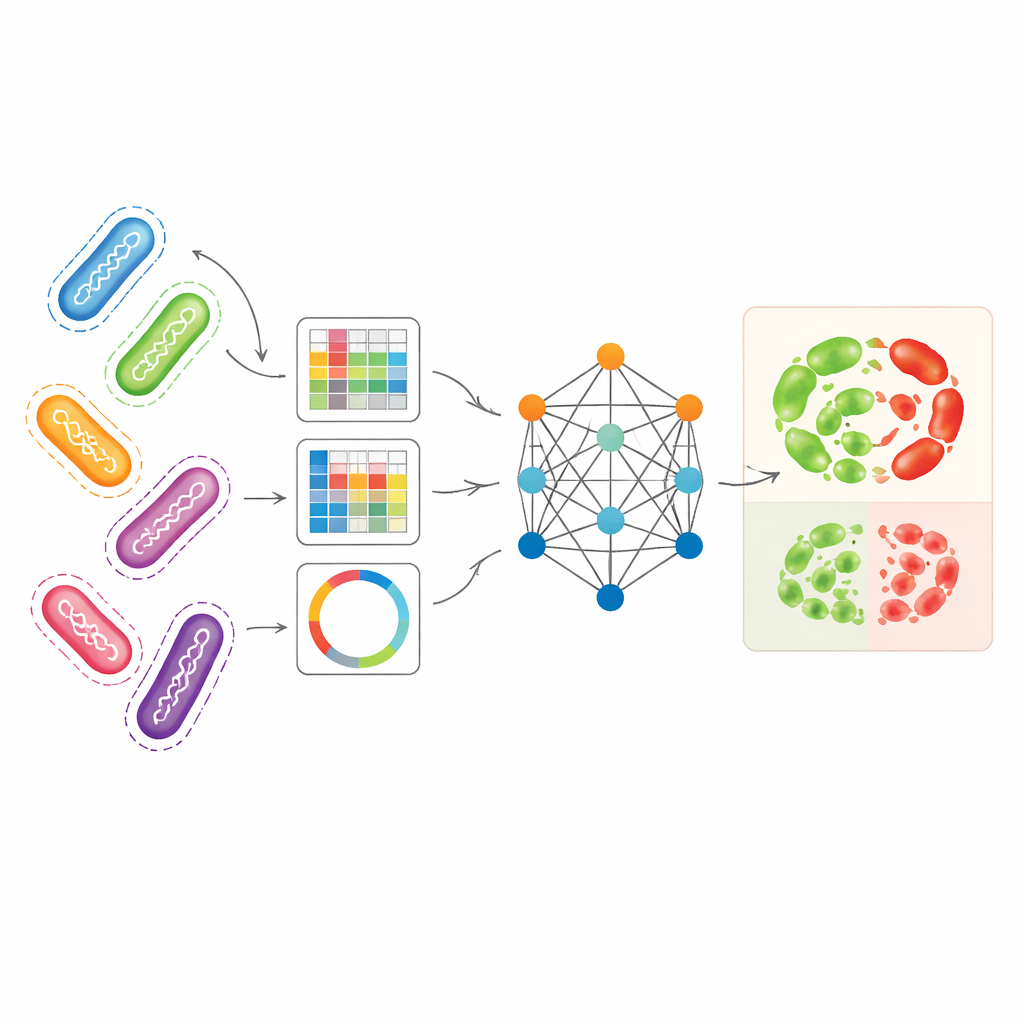
Combinare diverse viste genomiche in un’unica immagine
I ricercatori hanno cercato di sfruttare contemporaneamente più modalità complementari di rappresentare i genomi batterici. Hanno usato Pseudomonas aeruginosa — un patogeno acquisito in ambiente ospedaliero con schemi di resistenza particolarmente complessi — come caso di test principale. Una rappresentazione, chiamata unitigs, cattura frammenti ricorrenti di DNA senza fare riferimento a un genoma di riferimento. Un’altra rappresentazione registra piccole variazioni del DNA in posizioni specifiche, mentre una terza converte geni selezionati correlati alla resistenza in schemi simili a immagini che riassumono come brevi tratti di DNA sono organizzati. Da sole, queste rappresentazioni permettevano già a modelli di machine learning standard di prevedere la resistenza con una precisione ragionevole, in particolare gli unitigs per certi antibiotici. Tuttavia, ogni vista perde una parte della storia biologica e usarle separatamente sfrutta poco la ricchezza dei dati genomici sottostanti.
Come il modello a grafi apprende da ceppi correlati
AMR-GNN utilizza una forma di deep learning nota come rete neurale a grafi, che tratta ogni isolato batterico come un punto (nodo) e collega isolati geneticamente simili tramite legami (archi). In questa configurazione, il profilo dettagliato di unitigs di ciascun isolato costituisce il suo vettore di caratteristiche principale, mentre le altre viste genomiche definiscono come gli isolati sono connessi nel grafo. Il modello quindi passa informazioni lungo queste connessioni, permettendogli di apprendere da pattern condivisi tra genomi correlati. Per evitare di essere fuorviato da semplici relazioni clonali — dove i batteri sono strettamente correlati ma differiscono nella resistenza per ragioni che il modello deve scoprire — gli autori hanno deliberatamente rimosso gli archi che collegavano isolati appartenenti allo stesso gruppo di lineage genetico. Questo passo di “disaccoppiamento” costringe la rete a prestare maggiore attenzione alle caratteristiche specifiche del DNA associate alla resistenza, invece di affidarsi a etichette di lineage generali come scorciatoie.
Predizioni più robuste tra batteri e farmaci
Quando il team ha confrontato AMR-GNN con modelli più semplici basati su singole viste genomiche, l'approccio a grafi ha migliorato le prestazioni per quasi tutti i 12 antibiotici testati in P. aeruginosa, con i guadagni maggiori per i farmaci che in precedenza erano più difficili da prevedere. Il modello si è anche generalizzato meglio a set di test indipendenti, sebbene le prestazioni siano calate leggermente al di fuori dei dati di addestramento, sottolineando la necessità di collezioni di genomi più ampie e diversificate. Oltre a P. aeruginosa, i ricercatori hanno applicato AMR-GNN a oltre 23.000 genomi di altri patogeni principali, inclusi Escherichia coli, Klebsiella pneumoniae, Staphylococcus aureus ed Enterococcus faecium, su molti antibiotici di rilevanza clinica. Nella maggior parte delle combinazioni specie–farmaco, il framework ha raggiunto un'elevata accuratezza e ha superato strumenti basati su regole largamente usati che dipendono da liste curate di geni di resistenza noti.
Rendere i modelli black-box più spiegabili
Una preoccupazione importante per l'uso clinico è se un sistema di IA del genere può fornire indicazioni sul motivo di una specifica predizione. Il team ha affrontato questo applicando metodi di interpretabilità che tracciano quali caratteristiche del DNA contribuiscono maggiormente alle decisioni del modello. Per i farmaci in cui il modello ha reso meglio, AMR-GNN ha evidenziato molti geni e mutazioni di resistenza noti, come i classici bersagli degli antibiotici fluoroquinolonici. Ha anche indicato geni meno ben compresi i cui cambiamenti sono stati fortemente associati a concentrazioni di farmaco più alte necessarie per fermare la crescita batterica, suggerendo nuovi candidati per approfondimenti sperimentali in laboratorio. Questa capacità di prevedere la resistenza e al contempo segnalare potenziali determinanti biologici contribuisce a colmare il divario tra pura predizione e comprensione meccanicistica.
Cosa significa per l’assistenza ai pazienti in futuro
In sostanza, questo lavoro dimostra che combinare più “viste” del DNA all’interno di un modello di deep learning basato su grafi può migliorare sostanzialmente la predizione della resistenza antibiotica a partire dai genomi batterici. AMR-GNN è presentato come un framework flessibile e interpretabile che può essere esteso ad altri tipi di dati, come misure di attività genica o informazioni cliniche. Pur essendo necessario ancora lavoro — in particolare dataset più grandi e geograficamente vari e trial clinici prospettici — l'approccio ci avvicina a un futuro in cui una sequenza del genoma batterico, ottenuta direttamente da un campione del paziente, potrebbe guidare rapidamente i medici verso il farmaco giusto e contribuire a rallentare la diffusione delle infezioni resistenti.
Citazione: Nguyen, HA., Peleg, A.Y., Wisniewski, J.A. et al. AMR-GNN: a multi-representation graph neural network framework to enable genomic antimicrobial resistance prediction. Nat Commun 17, 3555 (2026). https://doi.org/10.1038/s41467-026-69934-8
Parole chiave: resistenza antimicrobica, reti neurali a grafi, genomica batterica, apprendimento automatico, predizione della suscettibilità agli antibiotici