Clear Sky Science · tr
Lgmn, iki ayrı GPCR olan PAR2 ve µ-OR1’i hedef alır ve ER Ca²⁺ salınımının tetiklediği hücre içi Ca²⁺ dengesizliği yoluyla akut lenfoblastik lösemide hücre ölümünü indükler
Bir Parazit Enziminin Çocuk Lösemisiyle Savaşmada Nasıl Yardımcı Olabileceği
Akut lenfoblastik lösemi (ALL), çocukların en sık görülen kan kanseridir; mevcut tedaviler birçok çocuğu iyileştirebilse de, genellikle ciddi yan etkilere ve nüks riskine yol açar. Beklenmedik bir bulgu olarak, yaygın bağırsak parazitleri tarafından insan hücrelerine saldırmakta kullanılan bir proteini inceleyen araştırmacılar, aynı molekülün lösemi hücrelerini seçici biçimde kendi kendini yok etmeye itebildiğini keşfettiler. Bu proteinin kanser hücrelerinin içindeki kalsiyum dengesini nasıl bozduğunu izleyerek, çalışma lösemi hücrelerini öldürmenin yeni yollarına işaret ediyor ve aynı zamanda potansiyel yeni ilaç hedeflerini ortaya koyuyor.
Yaygın Parazitlerden Gizli Bir Silah
Çalışma, Blastocystis ve Trichomonas gibi bağırsak ve ürogenital protozoaların salgıladığı bir enzim olan legumain üzerine odaklanıyor. Bu parazitler, konak dokulara saldırmak ve zarar vermek için legumain’i kullanır. Önceki araştırmalar, legumain’in insan hücrelerindeki PAR2 adlı bir reseptörü kesebildiğini ve bunun sonucunda hücre içi kalsiyumda artış tetiklediğini göstermişti. Ancak PAR2 kaldırıldığında veya kesilmeye dirençli hale getirildiğinde bile legumain hâlâ kalsiyum seviyelerini yükseltebiliyordu; bu da başka bir tetikleyicinin devrede olduğunu düşündürdü. Yaygın kullanılan bir lösemi ilacı olan L-asparaginaz’ın da PAR2 ve µ-OR1 adlı ikinci bir reseptör üzerinde etkili olması nedeniyle, yazarlar legumain’in lösemi hücrelerinin iç yaşamını bozmak için birden fazla yol kullanıp kullanmadığını araştırdılar.
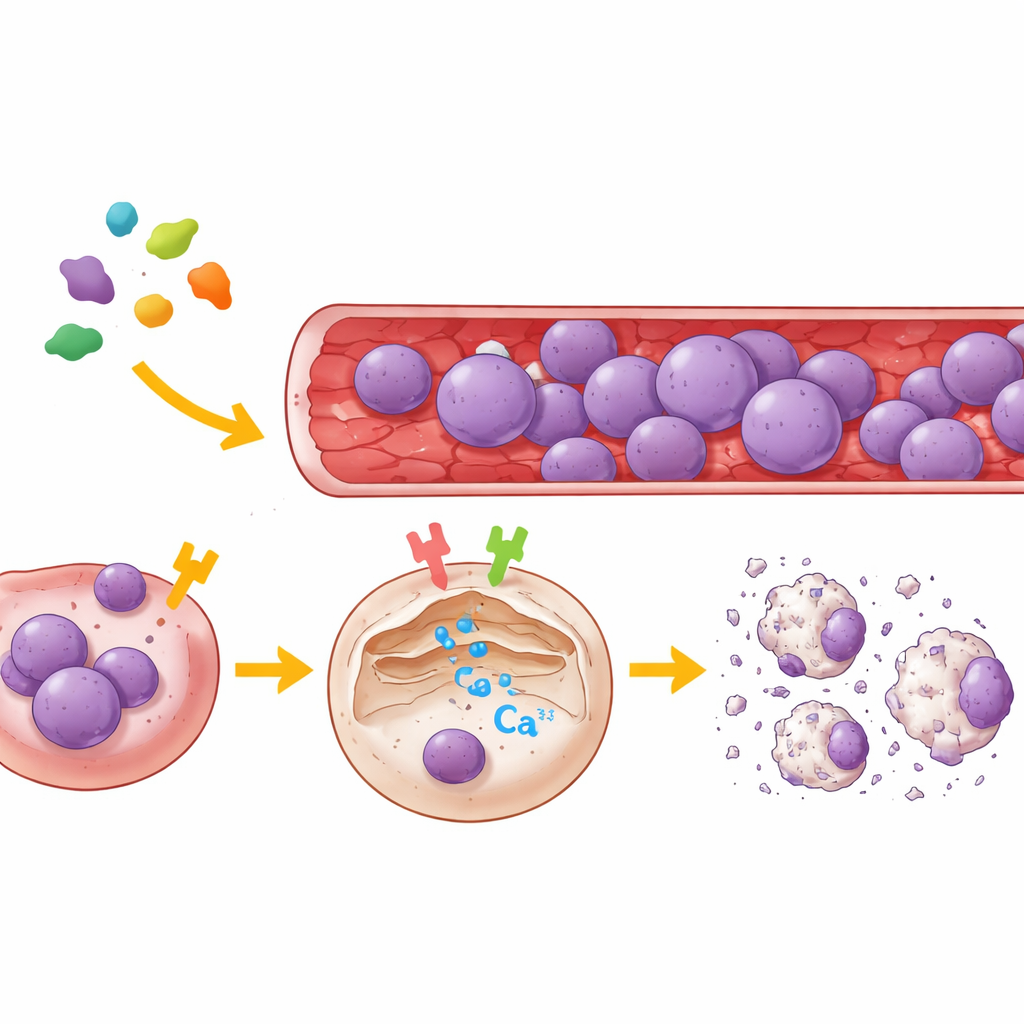
Kalsiyumu Kontrol Eden İki Hücre Anahtarı
Legumain’in hedeflerini haritalamak için ekip hem insan böbrek hücreleri hem de hastalardan alınmış birkaç ALL hücre türünü kullandı. Bu hücrelerde PAR2 veya µ-OR1’i seçici şekilde azalttılar ya da çok spesifik küçük moleküllü inhibitörlerle bloke ettiler; ardından endoplazmik retikulumdan, hücrenin başlıca iç kalsiyum deposundan kalsiyum salınımını bildiren floresan bir probla tek tek hücrelerdeki kalsiyum hareketlerini izlediler. Sonuçlar açıktı: legumain, en az bir reseptör aktif olduğunda bu depodan güçlü bir kalsiyum patlaması başlattı. µ-OR1’in inhibisyonu kalsiyum dalgasını büyük ölçüde azalttı, PAR2’nin bloke edilmesi ise daha küçük ancak dikkate değer bir düşüş yarattı. Her iki reseptör devre dışı bırakıldığında legumain artık kalsiyum salınımını tetikleyemedi. Birkaç B-hücre ve T-hücre lösemi hattında µ-OR1 baskın anahtar olarak öne çıkarken, PAR2 destekleyici bir rol oynadı.
Dengesiz Sinyaller Hücreleri Ölüme Gönderiyor
Legumain’in her iki reseptöre de etki ettiğini belirledikten sonra araştırmacılar, bu yüzey anahtarlarını hücrenin derinlerindeki olaylara bağlayan sinyal zincirlerini izlediler. PAR2, doğrudan PLC adlı bir enzimi aktive eden bir G proteiniyle eşleşir; PLC ise endoplazmik retikulumdeki kalsiyum kapılarını açar. Buna karşılık µ-OR1, esas olarak cAMP adlı haberci molekülün üretimini azaltan ve böylece protein kinaz A (PKA) olarak bilinen enzimi susturan farklı bir G proteini aracılığıyla sinyal verir. Normalde PKA, PLC üzerinde inhibitör “frenler” uygular ve BAD adlı hayatta kalma proteininin ölümcül olmayan bir durumda kalmasını sağlar. Legumain µ-OR1’i uyardığında cAMP düzeyleri düşer, PKA aktivitesi azalır, bu frenler serbest bırakılır ve PLC depodan daha fazla kalsiyum çıkarmakta özgürleşir. Aynı zamanda BAD, hücrenin ölüme karşı yerleşik savunmasını zayıflatan bir form değişikliğine uğrar.
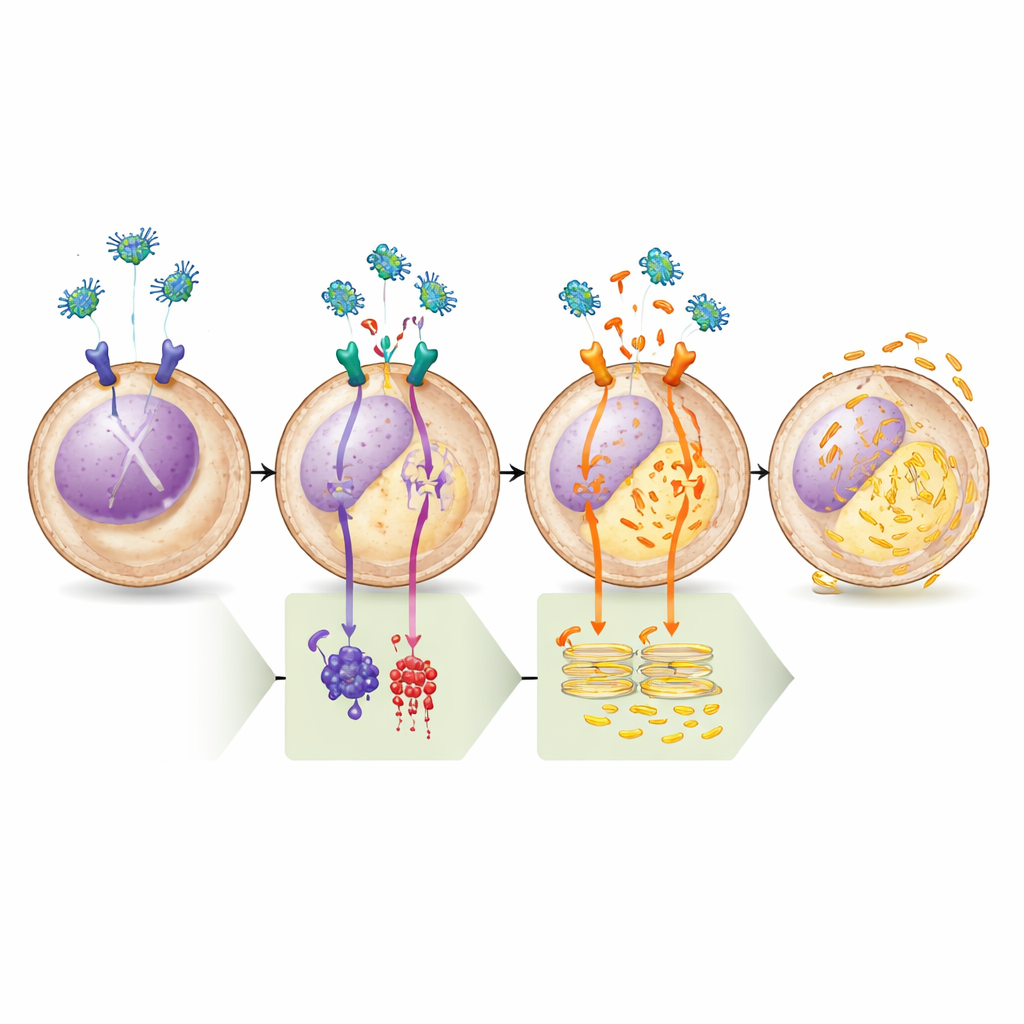
Yolu Adım Adım Kanıtlamak
Ekip bu modeli bir dizi farmakolojik testle doğruladı. cAMP’i artıran veya onu doğrudan yapan enzimi (adenilil siklazı) aktive eden ilaçlar, legumain’in endoplazmik retikulumdan kalsiyumu boşaltma yeteneğini tamamen engelledi; bu da µ-OR1–cAMP–PKA kolunun önemini vurguladı. Tersine, çok seçici bir PKA inhibitörü tek başına kalsiyum salınımını tetiklemek için yeterliydi ve üzerine legumain eklenmesi daha fazla etki yaratmadı; bu, PKA kapandığında yolun zaten tamamen devreye girdiğini gösteriyor. Biyokimyasal analizler, legumain tedavisinin PLC ve BAD üzerindeki PKA tarafından kontrol edilen fosfat “etiketlerini” azalttığını doğruladı; bu, aktivitelerindeki öngörülen değişiklikle uyumluydu. Son olarak, endoplazmik retikulumdaki kalsiyum kanalını bloke ettiklerinde veya bu kanal için gerekli ana bir iskele proteinini kaldırdıklarında legumain artık hücre ölümünü indükleyemedi; bu da ölümcü sonuçla kalsiyum dengesizliğini kesin olarak ilişkilendirdi.
Bu Bulguların Gelecek Lösemi Tedavileri İçin Anlamı
Bu sinyal kaskadının sonunda lösemi hücreleri, iç depolarından sürekli bir kalsiyum seli yaşar ve kritik bir hayatta kalma devresi kapanır. Bu değişiklikler birlikte hücreleri programlı hücre ölümü yani apoptoza iter. Bir düz okuyucu için mesaj şudur: legumain iki elli bir sabotajcı gibi davranır—kalsiyum salınımı için hücrenin iki “git” düğmesine aynı anda basarken, eşzamanlı olarak güvenlik sistemlerinin bağlantılarını keser. Legumain’in kendisi parazit kaynaklı olduğundan ve terapötik kullanım için dikkatli değerlendirme gerektirecektir, çalışma µ-OR1, PAR2 ve PKA’yı umut verici ilaç hedefleri olarak öne çıkarıyor. Legumain’in lösemi hücrelerinde kalsiyum dengesini seçici biçimde bozmasını taklit eden veya stratejik olarak PKA’yı inhibe eden ilaçlar, bir gün mevcut tedavilere direnç gösteren hastaların tedavisine yardımcı olabilir.
Atıf: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Anahtar kelimeler: akut lenfoblastik lösemi, legumain, kalsiyum sinyallemesi, G proteinine bağlı reseptörler, apoptoz