Clear Sky Science · sv
Lgmn riktar in sig på två distinkta GPCR:er, PAR2 och µ-OR1, och inducerar celldöd i akut lymfatisk leukemi genom en intracellulär Ca²⁺-obalans utlösts av ER:s Ca²⁺-frigöring
Hur ett parasitent enzym kan hjälpa till att bekämpa barndomsleukemi
Akut lymfatisk leukemi (ALL) är den vanligaste blodcancern hos barn, och även om nuvarande behandlingar kan bota många barn följs de ofta av svåra biverkningar och risk för återfall. I en oväntad vändning har forskare som studerat ett protein som vanliga tarmparasiter använder för att angripa mänskliga celler upptäckt att samma molekyl selektivt kan driva leukemiceller mot självdestruktion. Genom att följa hur detta protein rubbar balansen av kalcium inuti cancerceller pekar studien på nya sätt att döda leukemiceller och antyder samtidigt nya läkemedelsmål.
Ett dolt vapen från vanliga parasiter
Arbetet kretsar kring legumain, ett enzym som utsöndras av tarm- och urogenitala protister som Blastocystis och Trichomonas. Dessa parasiter använder legumain som en del av sitt arsenalkit för att invadera och skada värdvävnad. Tidigare forskning visade att legumain kan klyva en receptor på mänskliga celler som kallas PAR2 och därigenom utlösa en ökning av kalcium i cellen. Men även när PAR2 togs bort eller gjordes resistent mot klyvning lyckades legumain ändå öka kalciumnivåerna, vilket antydde att en annan trigger var inblandad. Eftersom ett ofta använt leukemiläkemedel, L-asparaginase, också verkar på PAR2 och på en andra receptor kallad μ-OR1, undersökte författarna om legumain på liknande sätt kunde använda mer än en väg för att rubba leukemicellernas inre balans.
Två celularbrytare som kontrollerar kalcium
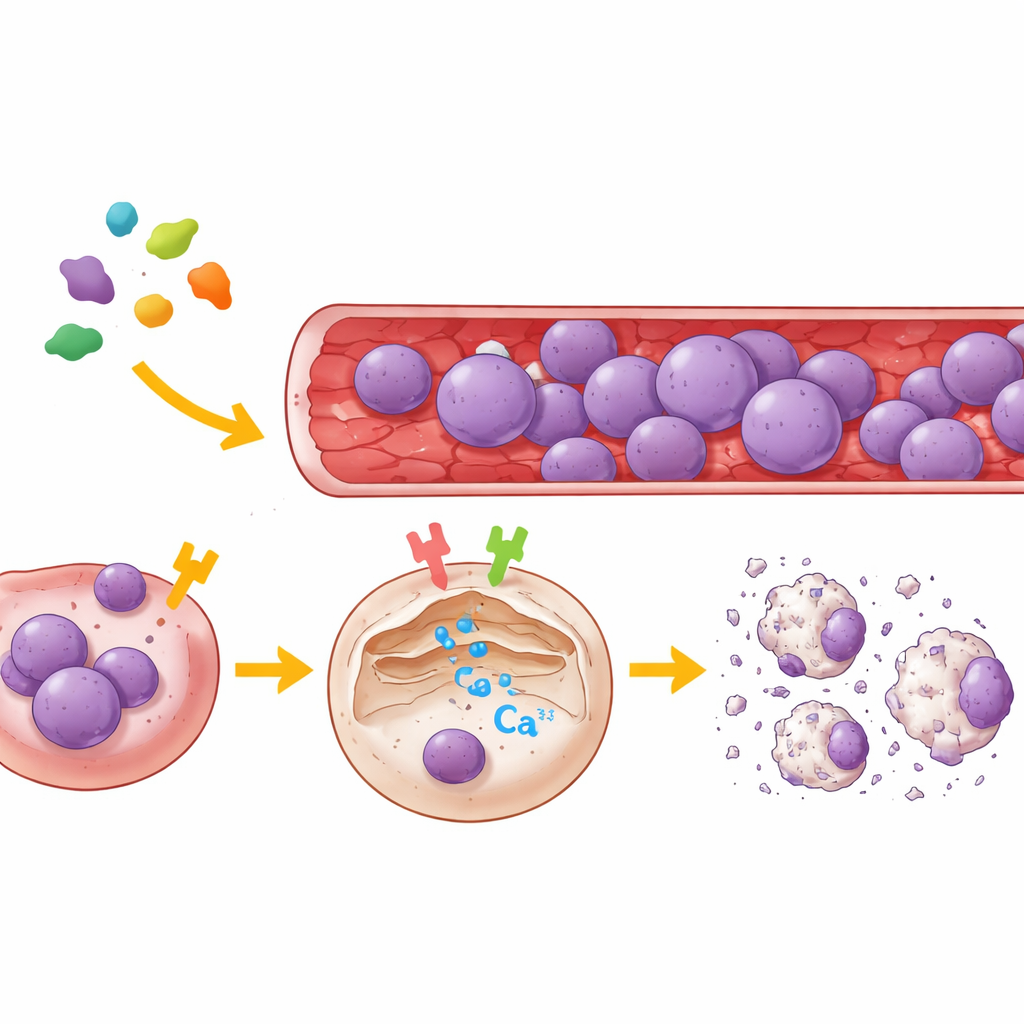
För att kartlägga legumains måltavlor använde teamet både humana njurceller och flera typer av ALL-celler från patienter. De minskade selektivt uttrycket av antingen PAR2 eller μ-OR1 i dessa celler, eller blockerade dem med högspecifika småmolekylära hämmare, och följde sedan kalciumsignaler i enskilda celler med en fluorescerande probe som rapporterar kalciumfrigörelse från det endoplasmatiska retikulumet, cellens huvudsakliga interna kalciumförråd. Resultaten var tydliga: legumain drev en kraftig burst av kalcium ut ur detta förråd bara när minst en av de två receptorerna var aktiv. Inhibering av μ-OR1 dämpade kalciumtoppen kraftigt, medan blockad av PAR2 gav en mindre men märkbar minskning. När båda receptorerna var inaktiverade kunde legumain inte längre framkalla kalciumfrigörelse. Över flera B‑cells- och T‑cellsleukemilinjer framträdde μ-OR1 som den dominerande brytaren, med PAR2 i en stödjande roll.
Obalanserade signaler tippar celler mot död
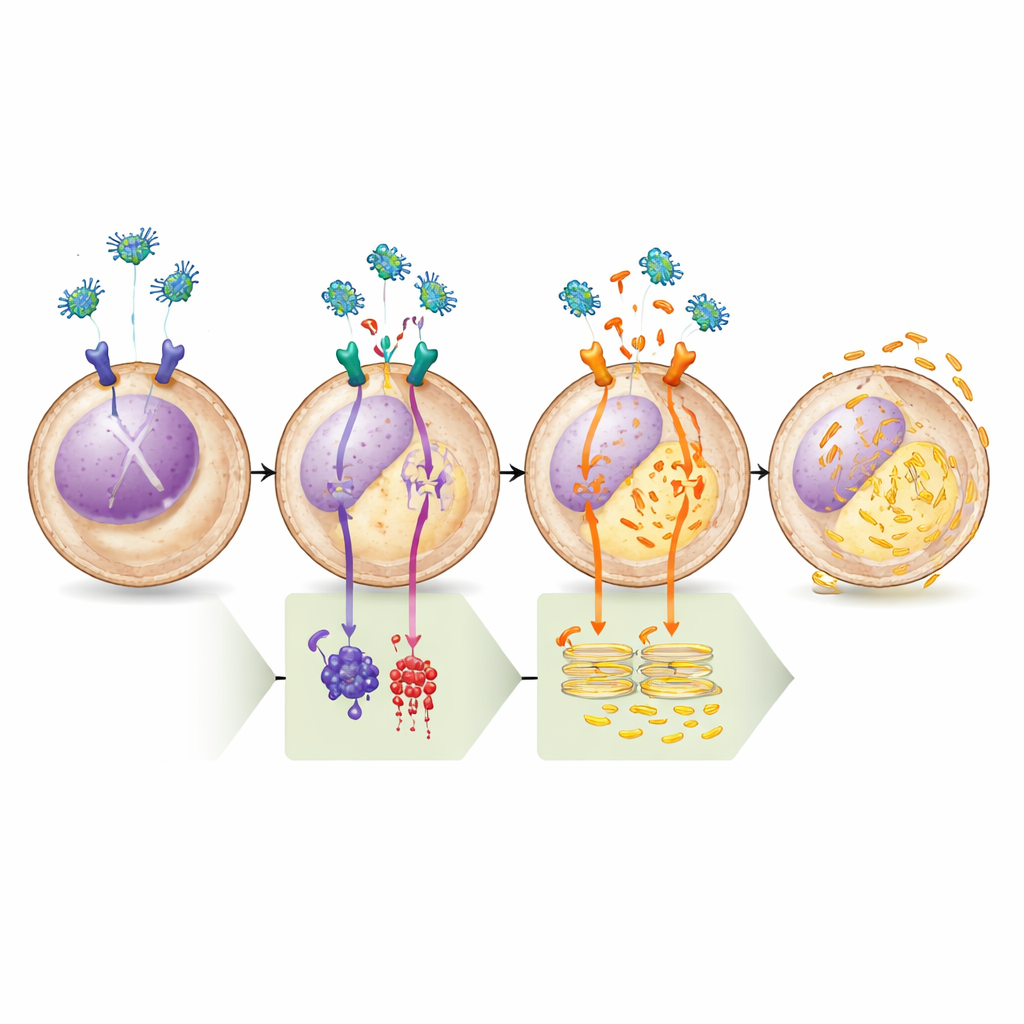
När forskarna fastställt att legumain påverkar båda receptorerna följde de de signalvägar som kopplar dessa ytbrytare till händelser djupt inne i cellen. PAR2 kopplas till ett G-protein som direkt aktiverar ett enzym kallat PLC, vilket i sin tur öppnar kalciumventiler på det endoplasmatiska retikulumet. μ-OR1 signalerar däremot huvudsakligen via ett annat G-protein som dämpar produktionen av budbärarmolekylen cAMP och därmed tystar ett enzym känt som protein kinas A (PKA). Normalt sätter PKA på inhibitoriska ”bromsar” på PLC och håller aktiviteten hos ett överlevnadsprotein kallat BAD i ett icke-dödligt tillstånd. När legumain stimulerar μ-OR1 faller cAMP-nivåerna, PKA-aktiviteten sjunker, dessa bromsar släpps och PLC kan driva mer kalcium ut från förrådet. Samtidigt övergår BAD till en form som försvagar cellens inbyggda försvar mot död.
Bevisa vägen steg för steg
Teamet verifierade denna modell med en serie farmakologiska tester. Läkemedel som ökade cAMP eller direkt aktiverade enzymet som tillverkar det (adenylatcyklas) blockerade helt legumains förmåga att tömma kalcium från det endoplasmatiska retikulumet, vilket understryker vikten av μ-OR1–cAMP–PKA-grenen. Omvänt var en högselektiv PKA-hämmare ensam tillräcklig för att utlösa kalciumfrigörelse, och tillsats av legumain därefter gav ingen ytterligare effekt, vilket visar att när PKA väl är avstängd är vägen redan fullt aktiverad. Biokemiska analyser bekräftade att legumainbehandling sänkte fosfat-”taggarna” på både PLC och BAD vid platser som är kända för att kontrolleras av PKA, vilket stämmer med den förutsagda förändringen i deras aktivitet. Slutligen, när forskarna blockerade kalciumkanalen på det endoplasmatiska retikulumet eller avlägsnade ett nyckelstödjande protein som krävs för denna kanal, inducerade legumain inte längre celldöd, vilket starkt kopplade det dödliga utfallet till kalciumobalans.
Vad detta kan betyda för framtida leukemibehandlingar
I slutet av denna signaleringskaskad upplever leukemiceller en långvarig översvämning av kalcium från sina interna förråd, tillsammans med avstängningen av en kritisk överlevnadskrets. Tillsammans pressar dessa förändringar cellerna in i programmerad celldöd, eller apoptos. För en lekmannaläsare är budskapet att legumain fungerar som en tvåhands-saboteur: den trycker på båda cellens ”gå”-knappar för kalciumfrigörelse samtidigt som den kapar ledningarna till säkerhetssystemen. Även om legumain i sig kommer från parasiter och skulle kräva noggrann utvärdering innan användning som terapi, framhäver studien μ-OR1, PAR2 och PKA som lovande läkemedelsmål. Läkemedel som efterliknar legumains selektiva störning av kalciumbalansen i leukemiceller — eller som strategiskt hämmar PKA — skulle en dag kunna hjälpa patienter vars cancer är resistent mot nuvarande behandlingar.
Citering: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Nyckelord: akut lymfatisk leukemi, legumain, kalciumsignalering, G-proteinkopplade receptorer, apoptos