Clear Sky Science · nl
Lgmn richt zich op twee verschillende GPCR's, PAR2 en µ-OR1, en veroorzaakt celdood bij acute lymfatische leukemie via een intracellulaire Ca²⁺-verstoring door vrijgave van ER-Ca²⁺
Hoe een parasitaire enzym kan helpen kinderleukemie te bestrijden
Acute lymfatische leukemie (ALL) is de meest voorkomende bloedkanker bij kinderen, en hoewel huidige behandelingen veel kinderen kunnen genezen, gaan ze vaak gepaard met zware bijwerkingen en het risico op terugkeer. In een onverwachte wending ontdekten onderzoekers die een eiwit bestudeerden dat door veelvoorkomende darmparasieten wordt gebruikt om menselijke cellen aan te vallen, dat ditzelfde molecuul leukemiecellen selectief kan aanzetten tot zelfvernietiging. Door na te gaan hoe dit eiwit de balans van calcium binnen kankercellen verstoort, wijst de studie op nieuwe manieren om leukemiecellen te doden en belicht ze potentiële nieuwe medicijndoelen.
Een verborgen wapen van veelvoorkomende parasieten
Het werk richt zich op legumain, een enzym dat wordt uitgescheiden door intestinale en urogenitale protozoa zoals Blastocystis en Trichomonas. Deze parasieten gebruiken legumain als onderdeel van hun arsenaal om gastweefsels binnen te dringen en te beschadigen. Eerder onderzoek toonde aan dat legumain een receptor op menselijke cellen, bekend als PAR2, kan knippen en daarmee een toename van calcium in de cel kan veroorzaken. Maar zelfs wanneer PAR2 werd verwijderd of resistent gemaakt tegen knippen, slaagde legumain er toch in de calciumniveaus te verhogen, wat suggereert dat een andere trigger in werking was. Omdat een veelgebruikt leukemiemedicijn, L-asparaginase, ook werkt op PAR2 en op een tweede receptor genaamd μ-OR1, vroegen de auteurs zich af of legumain op vergelijkbare wijze meer dan één route gebruikt om het binnenleven van leukemiecellen te verstoren.
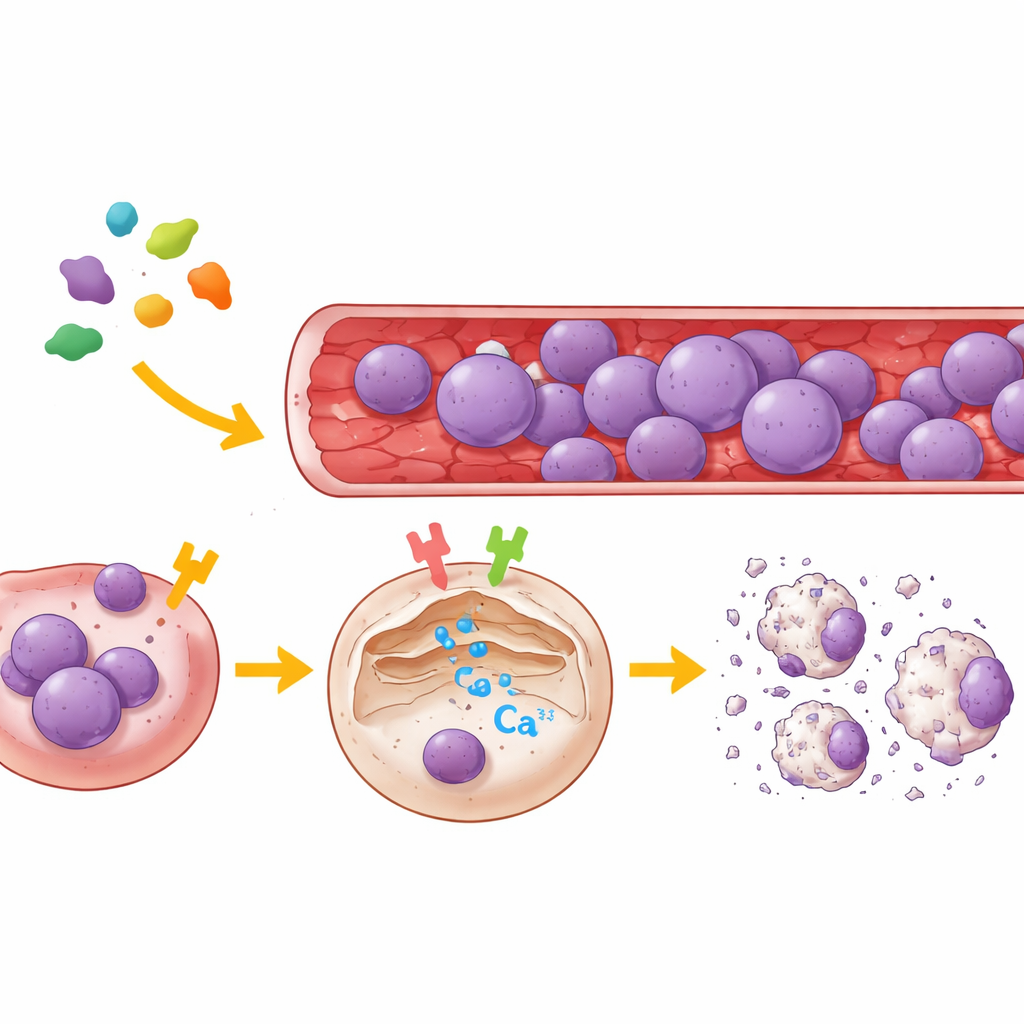
Twee schakelaars op de cel die calcium regelen
Om de doelen van legumain in kaart te brengen, gebruikte het team zowel menselijke niercellen als verschillende typen ALL-cellen van patiënten. Ze verminderden selectief ofwel PAR2 ofwel μ-OR1 in deze cellen, of blokkeerden ze met zeer specifieke kleinmolecuulremmers, en observeerden vervolgens calciumbewegingen in individuele cellen met een fluorescente probe die calciumvrijgave uit het endoplasmatisch reticulum rapporteert, de belangrijkste intracellulaire calciumopslag. De resultaten waren duidelijk: legumain veroorzaakte een sterke uitbarsting van calcium uit deze opslag alleen wanneer ten minste een van de twee receptoren actief was. Het remmen van μ-OR1 dempte de calciumpiek sterk, terwijl blokkering van PAR2 een kleinere maar merkbare vermindering opleverde. Wanneer beide receptoren waren uitgeschakeld, kon legumain geen calciumvrijgave meer opwekken. In verschillende B‑cel- en T‑cel-leukemielijnen bleek μ-OR1 de dominante schakel te zijn, met PAR2 in een ondersteunende rol.
Ontregelde signalen duwen cellen richting dood
Nadat was vastgesteld dat legumain beide receptoren aantast, volgden de onderzoekers de signaalroutes die deze oppervlakte-schakelaars verbinden met gebeurtenissen diep in de cel. PAR2 koppelt aan een G-eiwit dat direct een enzym genaamd PLC activeert, dat op zijn beurt calciumkleppen op het endoplasmatisch reticulum opent. μ-OR1 signaleert daarentegen voornamelijk via een ander G-eiwit dat de productie van de boodschapper cAMP vermindert en daarmee een enzym genaamd proteïnekinase A (PKA) dempt. Normaal gesproken legt PKA remmende "remmen" op PLC en houdt het een overlevingsproteïne genaamd BAD in een niet-dodelijke toestand. Wanneer legumain μ-OR1 stimuleert, dalen de cAMP-niveaus, neemt de PKA-activiteit af, worden deze remmen losgelaten en kan PLC meer calcium uit de opslag vrijmaken. Tegelijkertijd verschuift BAD naar een vorm die de ingebouwde afweer van de cel tegen celdood verzwakt.
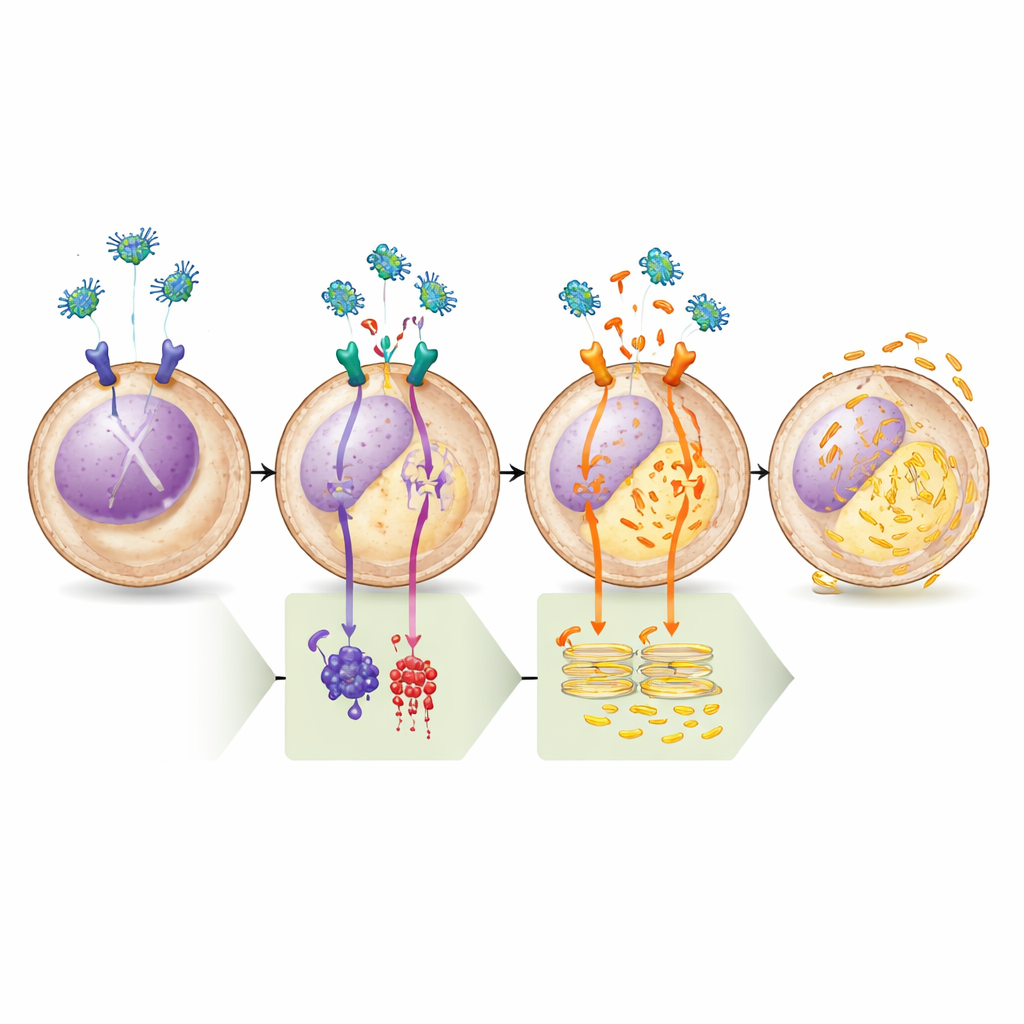
De route stap voor stap aantonen
Het team bevestigde dit model met een reeks farmacologische proeven. Middelen die cAMP verhoogden of direct het enzym activeerden dat het maakt (adenylaatcyclase) blokkeerden volledig het vermogen van legumain om calcium uit het endoplasmatisch reticulum te legen, waarmee het belang van de μ-OR1–cAMP–PKA-tak werd onderstreept. Omgekeerd was een zeer selectieve PKA-remmer op zichzelf voldoende om calciumvrijgave te veroorzaken, en toevoeging van legumain daarna leverde geen bijkomend effect op, wat aantoont dat zodra PKA is uitgeschakeld de route al volledig geactiveerd is. Biochemische analyses bevestigden dat legumainbehandeling de fosfaat-"labels" op zowel PLC als BAD op de door PKA gecontroleerde plekken verlaagde, wat overeenkomt met de voorspelde verandering in hun activiteit. Ten slotte, wanneer de onderzoekers het calciumkanaal op het endoplasmatisch reticulum blokkeerden of een cruciaal randproteïne verwijderden dat voor dit kanaal nodig is, induceerde legumain geen celdood meer, waarmee de dodelijke uitkomst stevig aan de calciumverstoring werd gekoppeld.
Wat dit kan betekenen voor toekomstige behandelingen van leukemie
Aan het eind van deze signaalcascade ondervinden leukemiecellen een aanhoudende stortvloed van calcium uit hun interne opslag, samen met de stillegging van een cruciaal overlevingscircuit. Samen duwen deze veranderingen de cellen in geprogrammeerde celdood, of apoptose. Voor de niet-specialist is de boodschap dat legumain fungeert als een tweehands saboteur: het activeert beide "startknoppen" voor calciumvrijgave terwijl het tegelijkertijd de draden naar de veiligheidsmechanismen doorsnijdt. Hoewel legumain zelf van parasieten afkomstig is en zorgvuldig geëvalueerd zou moeten worden voordat het als therapie wordt gebruikt, benadrukt de studie μ-OR1, PAR2 en PKA als veelbelovende medicijndoelen. Geneesmiddelen die legumains selectieve ontregeling van de calciumbalans in leukemiecellen nabootsen — of die PKA strategisch remmen — zouden op een dag kunnen helpen bij de behandeling van patiënten wier kanker resistent is tegen huidige therapieën.
Bronvermelding: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Trefwoorden: acute lymfatische leukemie, legumain, calciumsignalering, G-eiwit gekoppelde receptoren, apoptose