Clear Sky Science · pt
Lgmn mira dois GPCRs distintos, PAR2 e µ-OR1, e induz morte celular na leucemia linfoblástica aguda por meio de um desequilíbrio intracelular de Ca²⁺ desencadeado pela liberação de Ca²⁺ do RE
Como uma enzima de parasita pode ajudar a combater a leucemia infantil
A leucemia linfoblástica aguda (LLA) é o câncer sanguíneo infantil mais comum e, embora os tratamentos atuais possam curar muitas crianças, eles frequentemente vêm com efeitos colaterais severos e risco de recaída. Em uma reviravolta inesperada, pesquisadores que estudavam uma proteína usada por parasitas intestinais comuns para atacar células humanas descobriram que essa mesma molécula pode empurrar seletivamente células leucêmicas para a autodestruição. Ao traçar como essa proteína perturba o equilíbrio de cálcio dentro das células cancerosas, o estudo aponta novas formas de matar células leucêmicas ao mesmo tempo em que sugere novos alvos farmacológicos.
Uma arma oculta de parasitas comuns
O trabalho se concentra na legumaina, uma enzima secretada por protozoários intestinais e urogenitais, como Blastocystis e Trichomonas. Esses parasitas usam a legumaina como parte de seu arsenal para invadir e danificar tecidos do hospedeiro. Pesquisas anteriores mostraram que a legumaina pode clivar um receptor em células humanas conhecido como PAR2 e, ao fazê-lo, desencadear um aumento de cálcio dentro da célula. Mas mesmo quando o PAR2 foi removido ou tornado resistente à clivagem, a legumaina ainda conseguiu elevar os níveis de cálcio, o que implica que outro gatilho estava em ação. Como um fármaco amplamente usado contra leucemia, a L-asparaginase, também atua sobre PAR2 e sobre um segundo receptor chamado μ-OR1, os autores investigaram se a legumaina poderia igualmente usar mais de uma via para perturbar a vida interna das células leucêmicas.
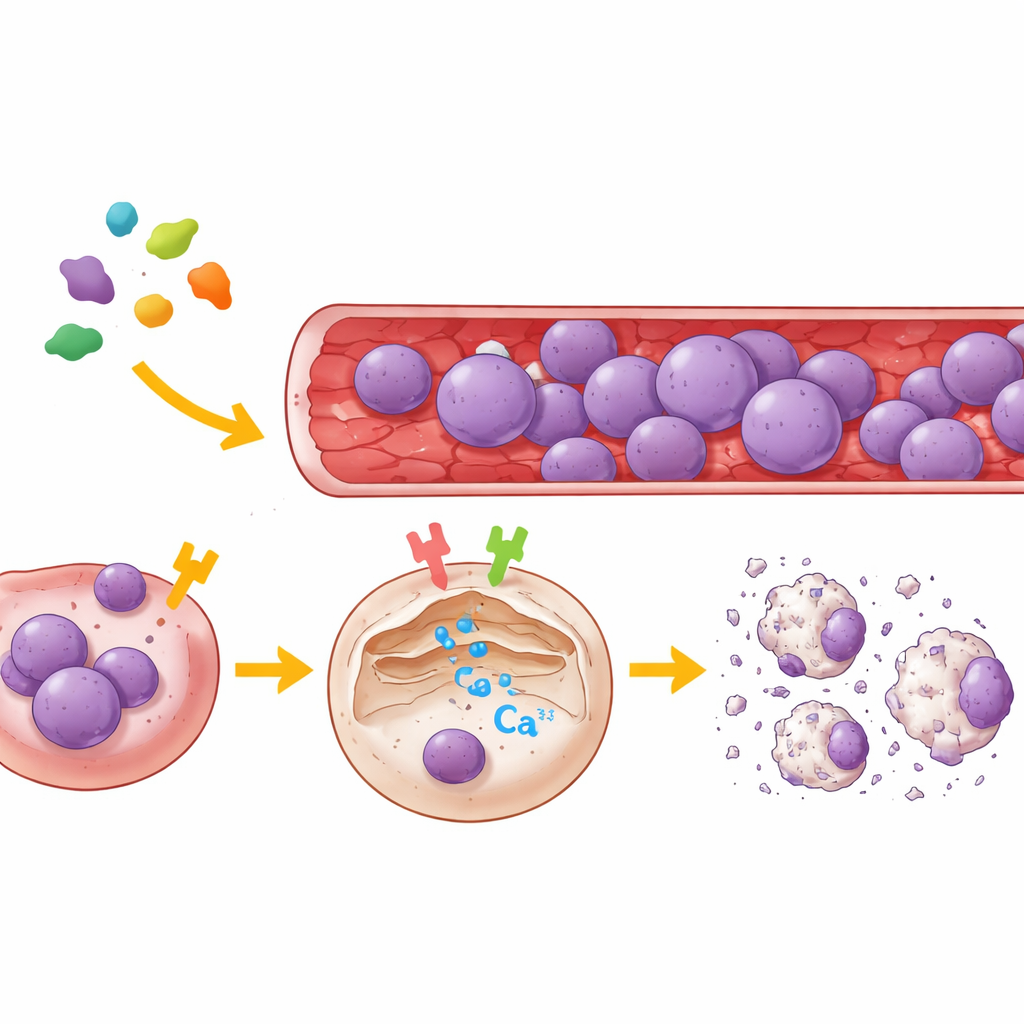
Dois interruptores celulares que controlam o cálcio
Para mapear os alvos da legumaina, a equipe usou tanto células renais humanas quanto vários tipos de células de LLA de pacientes. Eles reduziram seletivamente PAR2 ou μ-OR1 nessas células, ou os bloquearam com inibidores de pequenas moléculas altamente específicos, e então monitoraram os movimentos de cálcio em células individuais usando uma sonda fluorescente que reporta a liberação de cálcio do retículo endoplasmático, o principal depósito interno de cálcio da célula. Os resultados foram claros: a legumaina provocou uma forte descarga de cálcio desse reservatório apenas quando pelo menos um dos dois receptores estava ativo. Inibir μ-OR1 atenuou fortemente o surto de cálcio, enquanto bloquear PAR2 produziu uma redução menor, porém notável. Quando ambos os receptores foram desativados, a legumaina não pôde mais provocar a liberação de cálcio. Em várias linhagens de leucemia de células B e T, μ-OR1 emergiu como o interruptor dominante, com PAR2 desempenhando um papel de apoio.
Sinais desequilibrados inclinam as células para a morte
Depois de estabelecer que a legumaina atinge ambos os receptores, os pesquisadores seguiram as cadeias de sinalização que conectam esses interruptores de superfície a eventos no interior da célula. PAR2 se acopla a uma proteína G que ativa diretamente uma enzima chamada PLC, que por sua vez abre válvulas de cálcio no retículo endoplasmático. μ-OR1, por contraste, sinaliza principalmente por meio de uma proteína G diferente que reduz a produção do mensageiro cAMP e, assim, silencia uma enzima conhecida como proteína quinase A (PKA). Normalmente, a PKA aplica "freios" inibitórios sobre a PLC e mantém a atividade de uma proteína de sobrevivência chamada BAD em um estado não letal. Quando a legumaina estimula μ-OR1, os níveis de cAMP caem, a atividade da PKA diminui, esses freios são liberados e a PLC fica livre para promover mais liberação de cálcio das reservas. Ao mesmo tempo, BAD muda para uma forma que enfraquece as defesas internas da célula contra a morte.
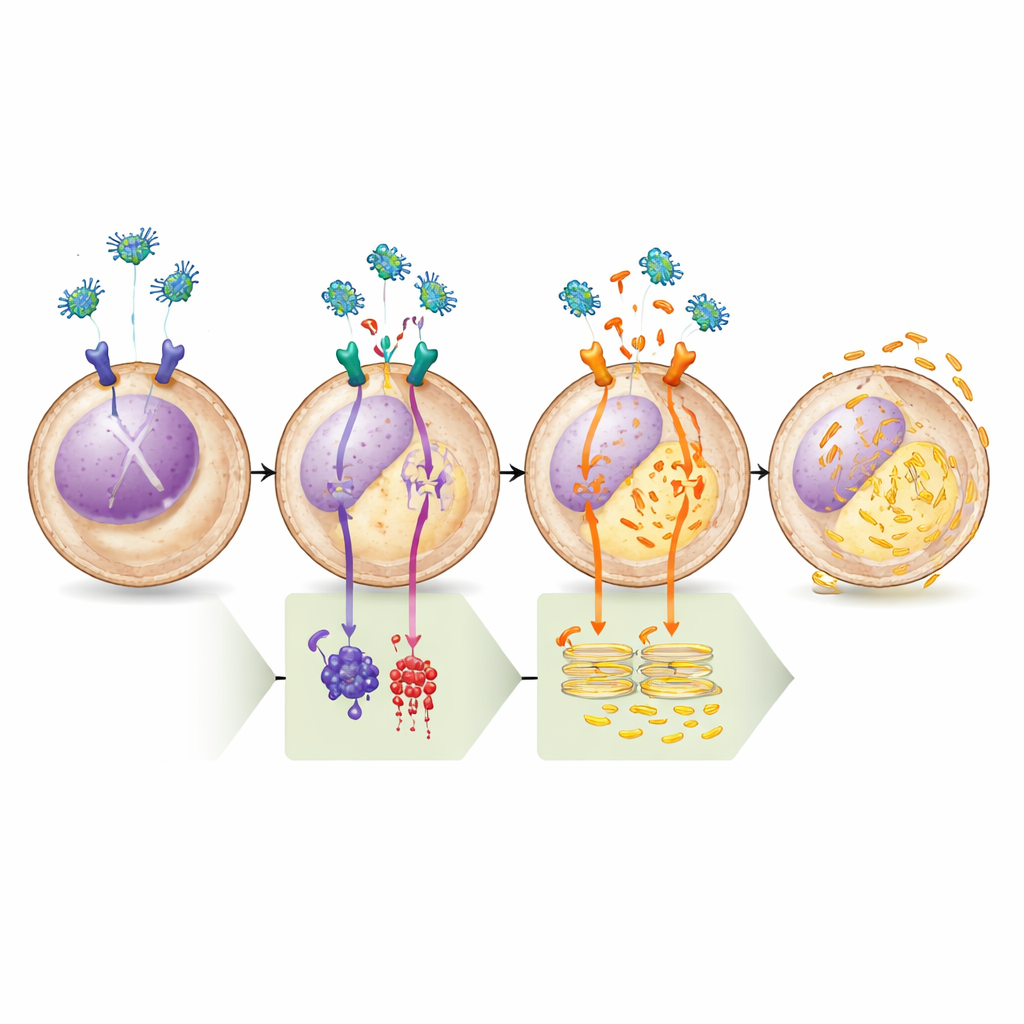
Comprovando a via passo a passo
A equipe verificou esse modelo com uma série de testes farmacológicos. Fármacos que aumentaram o cAMP ou ativaram diretamente a enzima que o produz (adenilato ciclase) bloquearam completamente a capacidade da legumaina de esvaziar o cálcio do retículo endoplasmático, ressaltando a importância do ramo μ-OR1–cAMP–PKA. Por outro lado, um inibidor de PKA altamente seletivo isoladamente foi suficiente para desencadear a liberação de cálcio, e adicionar legumaina em seguida não produziu efeito adicional, mostrando que uma vez que a PKA é desligada, a via já está totalmente ativada. Análises bioquímicas confirmaram que o tratamento com legumaina reduziu as "etiquetas" de fosfato tanto na PLC quanto na BAD em sítios conhecidos por serem controlados pela PKA, correspondendo à mudança prevista em suas atividades. Finalmente, quando os pesquisadores bloquearam o canal de cálcio no retículo endoplasmático ou eliminaram uma proteína estrutural chave necessária para esse canal, a legumaina deixou de induzir morte celular, vinculando firmemente o desfecho letal ao desequilíbrio de cálcio.
O que isso pode significar para futuros tratamentos da leucemia
No final dessa cascata de sinalização, as células leucêmicas experimentam uma inundação sustentada de cálcio de seus estoques internos, juntamente com o desligamento de um circuito crítico de sobrevivência. Juntas, essas mudanças empurram as células para a morte programada, ou apoptose. Para um leitor leigo, a mensagem é que a legumaina age como um sabotador de duas mãos: pressiona ambos os "botões de avanço" da célula para liberação de cálcio enquanto, ao mesmo tempo, corta os fios de seus sistemas de segurança. Embora a legumaina em si provenha de parasitas e exija avaliação cuidadosa antes de uso como terapia, o estudo destaca μ-OR1, PAR2 e PKA como alvos farmacológicos promissores. Medicamentos que imitem a perturbação seletiva do equilíbrio de cálcio promovida pela legumaina em células leucêmicas — ou que inibam estrategicamente a PKA — poderiam, um dia, ajudar a tratar pacientes cujos cânceres resistem às terapias atuais.
Citação: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Palavras-chave: leucemia linfoblástica aguda, legumaina, sinalização por cálcio, receptores acoplados à proteína G, apoptose