Clear Sky Science · pl
Lgmn celuje w dwa odrębne receptory GPCR, PAR2 i µ-OR1, i wywołuje śmierć komórek w ostrej białaczce limfoblastycznej poprzez wewnątrzkomórkowy brak równowagi Ca²⁺ wyzwolony uwolnieniem Ca²⁺ z ER
Jak enzym pasożyta może pomóc zwalczać białaczkę u dzieci
Ostra białaczka limfoblastyczna (ALL) jest najczęstszym nowotworem krwi u dzieci. Chociaż obecne terapie potrafią wyleczyć wielu pacjentów, często wiążą się one z silnymi efektami ubocznymi i ryzykiem nawrotu. W nieoczekiwanym zwrocie wydarzeń badacze zajmujący się białkiem wykorzystywanym przez powszechne pasożyty jelitowe do atakowania komórek ludzkich odkryli, że ta sama cząsteczka może selektywnie skłaniać komórki białaczkowe do samozniszczenia. Śledząc, jak to białko zaburza równowagę wapnia wewnątrz komórek nowotworowych, badanie wskazuje nowe sposoby zabijania komórek białaczki i sugeruje potencjalne cele lekowe.
Ukryta broń powszechnych pasożytów
Praca skupia się na legumainie, enzymie wydzielanym przez pierwotniaki jelitowe i urogenitalne, takie jak Blastocystis i Trichomonas. Pasożyty te wykorzystują legumainę jako element arsenału służącego do inwazji i uszkadzania tkanek gospodarza. Wcześniejsze badania wykazały, że legumaina może przeciąć receptor na komórkach ludzkich znany jako PAR2, co w konsekwencji wywołuje wzrost poziomu wapnia wewnątrz komórki. Jednak nawet po usunięciu PAR2 lub uczynieniu go odpornym na rozcięcie, legumaina nadal potrafiła podwyższyć poziom wapnia, co sugerowało udział dodatkowego mechanizmu. Ponieważ szeroko stosowany lek przeciwnowotworowy L-asparaginaza działa zarówno na PAR2, jak i na drugi receptor zwany μ-OR1, autorzy zapytali, czy legumaina również może korzystać z więcej niż jednej drogi do zakłócenia wewnętrznego życia komórek białaczkowych.
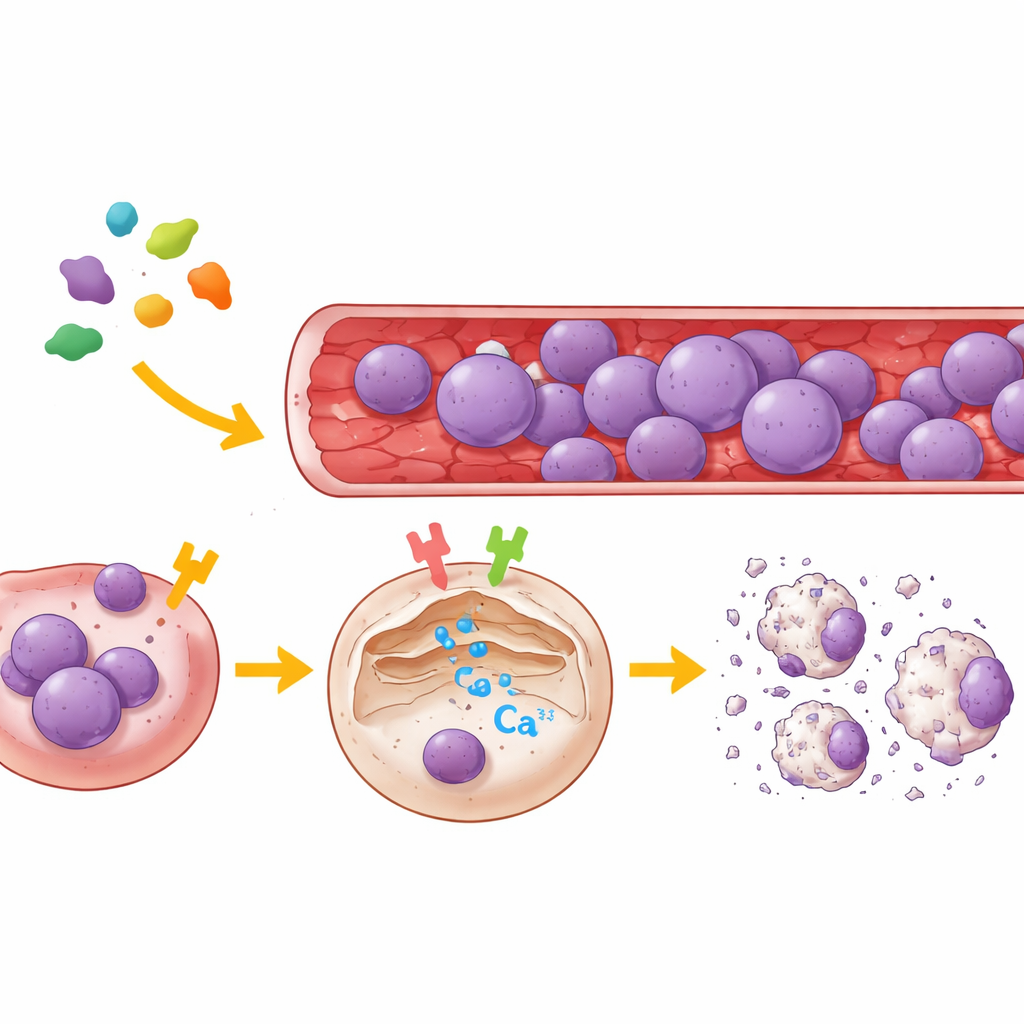
Dwa przełączniki komórkowe kontrolujące wapń
Aby zmapować cele legumainy, zespół wykorzystał zarówno ludzkie komórki nerkowe, jak i kilka typów komórek ALL pochodzących od pacjentów. Selektywnie zmniejszano ekspresję PAR2 lub μ-OR1 w tych komórkach albo blokowano je za pomocą wysoce specyficznych inhibitorów małocząsteczkowych, a następnie obserwowano ruchy wapnia w pojedynczych komórkach za pomocą fluorescencyjnego markera raportującego uwolnienie Ca²⁺ z retikulum endoplazmatycznego, głównego wewnętrznego magazynu wapnia komórki. Wyniki były jednoznaczne: legumaina wywoływała silny wyrzut wapnia z tego magazynu tylko wtedy, gdy przynajmniej jeden z obu receptorów był aktywny. Zablokowanie μ-OR1 wyraźnie osłabiało falę wapniową, podczas gdy blokada PAR2 dawała mniejsze, lecz zauważalne zmniejszenie. Gdy oba receptory zostały wyłączone, legumaina nie była już w stanie wywołać uwolnienia wapnia. W wielu liniach białaczki z komórek B i T μ-OR1 okazał się dominującym przełącznikiem, a PAR2 pełnił rolę wspierającą.
Nieprzywrócona równowaga kieruje komórki ku śmierci
Ustalając, że legumaina oddziałuje na oba receptory, badacze śledzili dalej łańcuchy sygnałowe łączące te powierzchniowe „przełączniki” z wydarzeniami głęboko w komórce. PAR2 sprzęga się z białkiem G, które bezpośrednio aktywuje enzym PLC, a ten z kolei otwiera zawory wapniowe na retikulum endoplazmatycznym. μ-OR1 natomiast sygnalizuje głównie przez inny białkowy G, który tłumi produkcję przekaźnika cAMP, a tym samym wycisza aktywność kinazy białkowej A (PKA). Normalnie PKA nakłada hamujące „zaczepy” na PLC i utrzymuje białko przeżyciowe BAD w stanie nieniszczącym. Gdy legumaina stymuluje μ-OR1, poziom cAMP spada, aktywność PKA maleje, te hamulce zostają poluzowane, a PLC może wypompować więcej wapnia ze zbiorników. Równocześnie BAD przechodzi w formę osłabiającą wewnętrzne mechanizmy obronne komórki przed śmiercią.
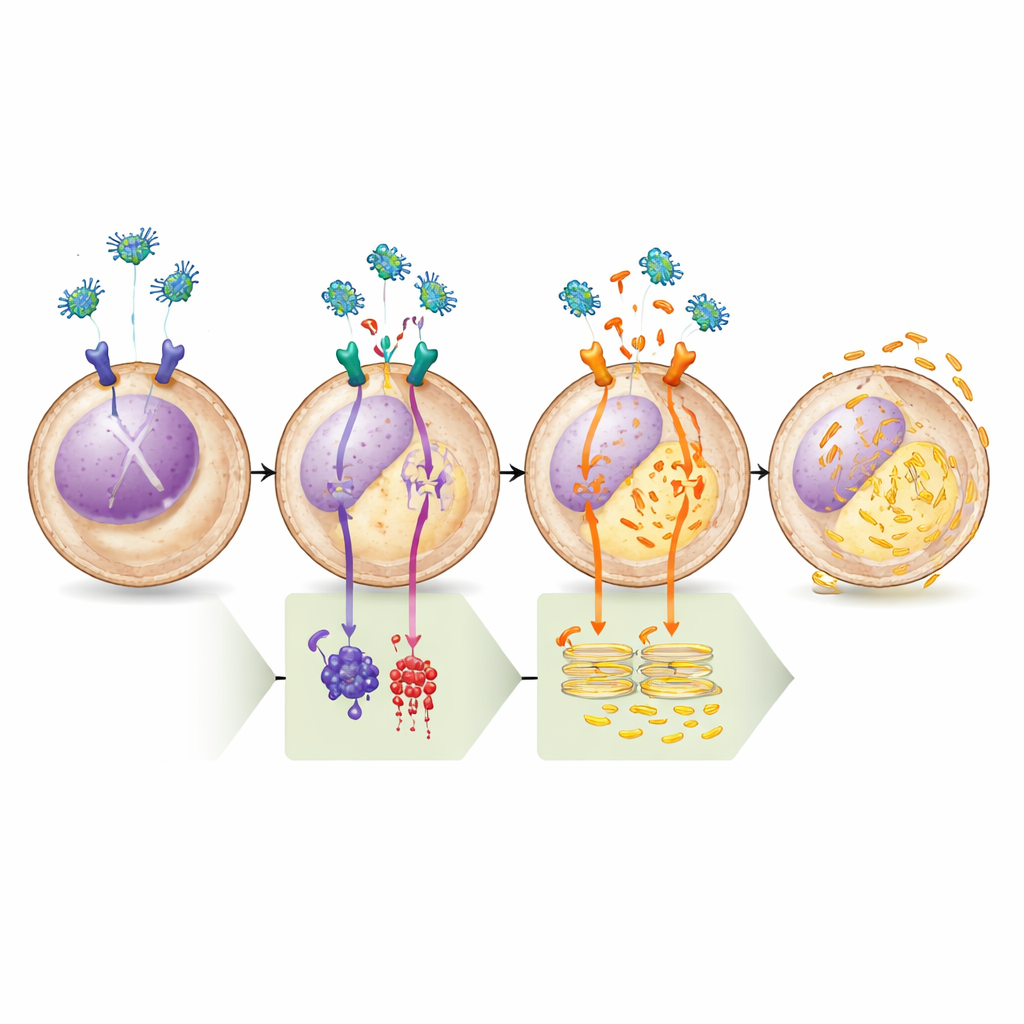
Potwierdzanie szlaku krok po kroku
Zespół zweryfikował ten model serią testów farmakologicznych. Leki zwiększające cAMP lub bezpośrednio aktywujące enzym go wytwarzający (cyklazę adenylanową) całkowicie blokowały zdolność legumainy do opróżnienia retikulum endoplazmatycznego z wapnia, podkreślając znaczenie odgałęzienia μ-OR1–cAMP–PKA. Odwrotnie, wysoce selektywny inhibitor PKA sam w sobie wystarczył, by wywołać uwolnienie wapnia, a dodanie legumainy później nie przynosiło dodatkowego efektu, co pokazuje, że gdy PKA zostaje wyłączona, szlak jest już w pełni zaangażowany. Analizy biochemiczne potwierdziły, że leczenie legumainą obniżało poziom grup fosforanowych na PLC i BAD w miejscach znanych jako kontrolowane przez PKA, zgodnie z przewidywaną zmianą ich aktywności. Wreszcie, gdy badacze zablokowali kanał wapniowy na retikulum endoplazmatycznym lub usunęli kluczowe białko rusztowania potrzebne do funkcjonowania tego kanału, legumaina przestała wywoływać śmierć komórki, co mocno powiązało efekt śmiertelny z zaburzeniem równowagi wapniowej.
Co to może znaczyć dla przyszłych terapii białaczki
Na końcu tego kaskadowego sygnalizowania komórki białaczkowe doświadczają utrzymującego się napływu wapnia z wewnętrznych magazynów oraz wyłączenia krytycznego obwodu przeżycia. Te zmiany razem przesuwają komórki na ścieżkę zaprogramowanej śmierci, czyli apoptozy. Dla czytelnika popularnonaukowego przekaz jest taki, że legumaina działa jak sabotażysta na dwa fronty: jednocześnie naciska oba „przyciski zapalające” uwalnianie wapnia i odcina przewody systemów bezpieczeństwa. Choć sama legumaina pochodzi od pasożytów i wymagałaby ostrożnej oceny przed zastosowaniem jako terapia, badanie wyróżnia μ-OR1, PAR2 i PKA jako obiecujące cele lekowe. Leki naśladujące selektywne zakłócenie równowagi wapniowej przez legumainę w komórkach białaczki — albo strategicznie hamujące PKA — mogłyby w przyszłości pomóc leczyć pacjentów, których nowotwory opierają się obecnym terapiom.
Cytowanie: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Słowa kluczowe: ostra białaczka limfoblastyczna, legumaina, sygnalizacja wapniowa, receptory sprzężone z białkiem G, apoptoza