Clear Sky Science · it
Lgmn bersaglia due GPCR distinti, PAR2 e µ-OR1, e induce la morte cellulare nella leucemia linfoblastica acuta tramite uno squilibrio intracellulare di Ca²⁺ innescato dal rilascio di Ca²⁺ dal RE
Come un enzima parassitario potrebbe aiutare a combattere la leucemia infantile
La leucemia linfoblastica acuta (LLA) è il tumore del sangue più comune nell’infanzia e, sebbene i trattamenti attuali possano guarire molti bambini, spesso comportano effetti collaterali gravosi e il rischio di recidiva. In una svolta inaspettata, ricercatori che studiavano una proteina usata da parassiti intestinali comuni per attaccare le cellule umane hanno scoperto che la stessa molecola può spingere selettivamente le cellule leucemiche verso l’autodistruzione. Seguendo come questa proteina altera l’equilibrio del calcio all’interno delle cellule tumorali, lo studio indica nuove modalità per uccidere le cellule leucemiche e suggerisce potenziali target farmacologici.
Un’arma nascosta di parassiti comuni
Il lavoro si concentra sulla legumain, un enzima secreto da protozoi intestinali e urogenitali come Blastocystis e Trichomonas. Questi parassiti utilizzano la legumain come parte del loro arsenale per invadere e danneggiare i tessuti ospiti. Ricerche precedenti avevano mostrato che la legumain può tagliare un recettore sulle cellule umane noto come PAR2 e, così facendo, innescare un aumento del calcio intracellulare. Ma anche quando PAR2 veniva rimosso o reso resistente al taglio, la legumain riusciva comunque ad aumentare i livelli di calcio, indicando che era in gioco un altro innesco. Poiché un farmaco ampiamente usato nella leucemia, L-asparaginasi, agisce anch’esso su PAR2 e su un secondo recettore chiamato μ-OR1, gli autori si sono chiesti se la legumain potesse ugualmente utilizzare più di una via per perturbare la vita interna delle cellule leucemiche.
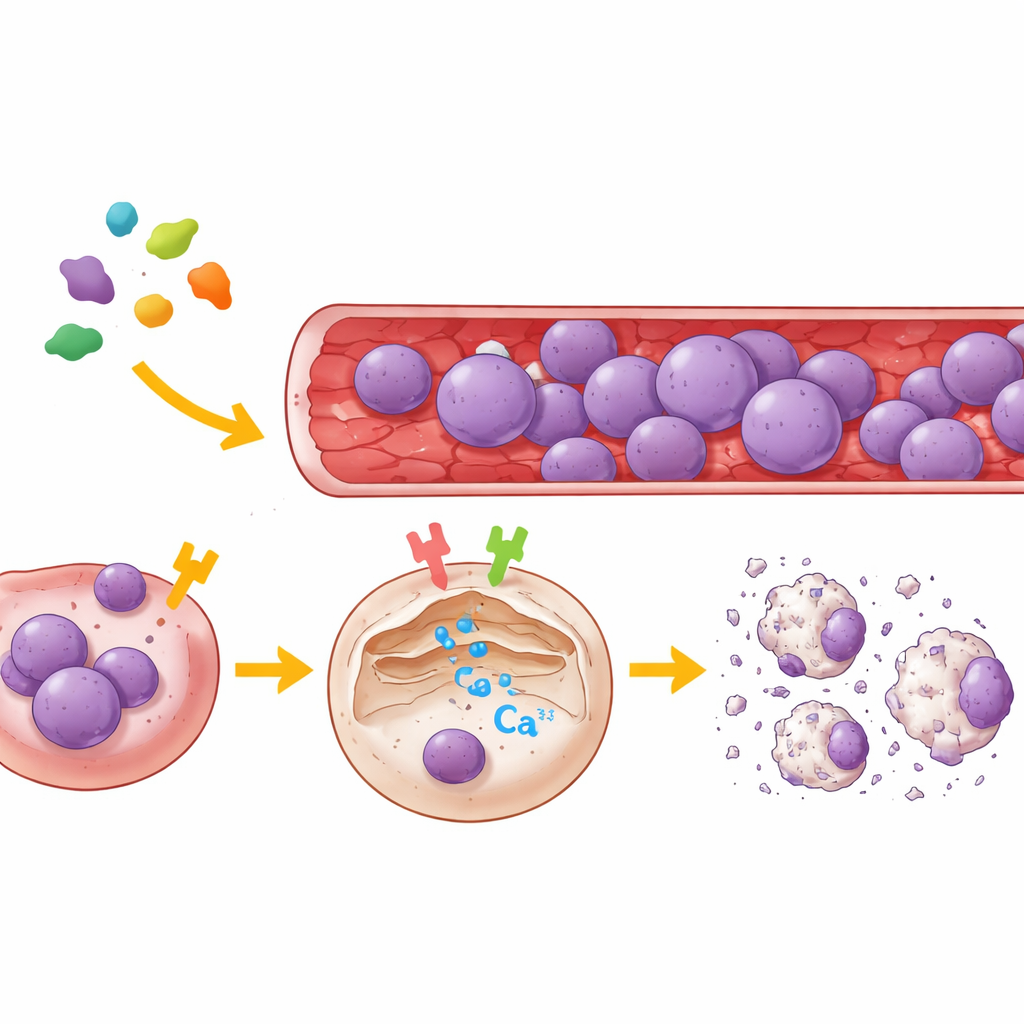
Due interruttori cellulari che controllano il calcio
Per mappare i bersagli della legumain, il team ha usato sia cellule renali umane sia diversi tipi di cellule di LLA provenienti da pazienti. Hanno ridotto selettivamente PAR2 o μ-OR1 in queste cellule, oppure li hanno bloccati con inibitori molecolari altamente specifici, quindi hanno osservato i movimenti del calcio in singole cellule usando una sonda fluorescente che segnala il rilascio di calcio dal reticolo endoplasmatico, il principale deposito intracellulare di calcio. I risultati sono stati chiari: la legumain ha provocato una forte scarica di calcio da questo deposito solo quando almeno uno dei due recettori era attivo. L’inibizione di μ-OR1 ha attenuato nettamente la sovraccarica di calcio, mentre il blocco di PAR2 ha prodotto una riduzione più piccola ma evidente. Quando entrambi i recettori sono stati disattivati, la legumain non ha più potuto provocare il rilascio di calcio. In diverse linee leucemiche di cellule B e T, μ-OR1 è emerso come l’interruttore dominante, con PAR2 in ruolo di supporto.
Segnali sbilanciati che spingono le cellule verso la morte
Dopo aver stabilito che la legumain colpisce entrambi i recettori, i ricercatori hanno poi seguito le catene di segnalazione che collegano questi interruttori di superficie a eventi profondi all’interno della cellula. PAR2 si accoppia a una proteina G che attiva direttamente un enzima chiamato PLC, che a sua volta apre le “valvole” del calcio sul reticolo endoplasmatico. μ-OR1, al contrario, segnala principalmente attraverso una diversa proteina G che riduce la produzione della molecola messaggera cAMP e di conseguenza attenua l’attività di un enzima noto come protein-chinasi A (PKA). Normalmente, la PKA esercita freni inibitori su PLC e mantiene l’attività di una proteina di sopravvivenza chiamata BAD in uno stato non letale. Quando la legumain stimola μ-OR1, i livelli di cAMP diminuiscono, l’attività della PKA cala, questi freni vengono rilasciati e il PLC è libero di spingere più calcio fuori dalle riserve. Allo stesso tempo, BAD si modifica in una forma che indebolisce le difese intrinseche della cellula contro la morte.
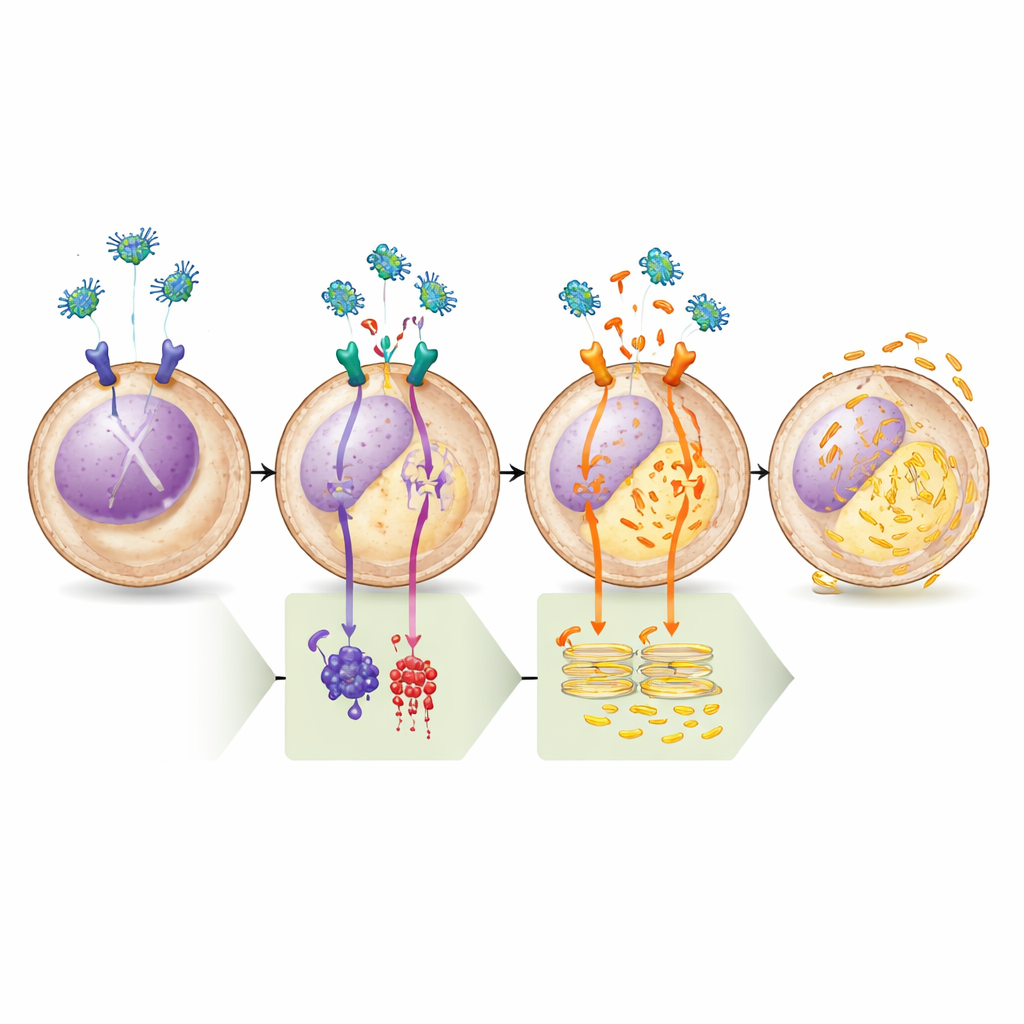
Dimostrare il percorso passo dopo passo
Il team ha verificato questo modello con una serie di test farmacologici. Farmaci che aumentavano il cAMP o attivavano direttamente l’enzima che lo produce (adenilato ciclasi) hanno bloccato completamente la capacità della legumain di svuotare il calcio dal reticolo endoplasmatico, sottolineando l’importanza del ramo μ-OR1–cAMP–PKA. Al contrario, un inibitore altamente selettivo della PKA da solo è stato sufficiente a indurre il rilascio di calcio, e l’aggiunta successiva di legumain non ha prodotto alcun effetto ulteriore, mostrando che una volta che la PKA è spenta il percorso è già completamente attivato. Analisi biochimiche hanno confermato che il trattamento con legumain riduceva i “tag” fosfato sia su PLC sia su BAD in siti noti per essere controllati dalla PKA, corrispondendo al cambiamento previsto nella loro attività. Infine, quando i ricercatori hanno bloccato il canale del calcio sul reticolo endoplasmatico o rimosso una proteina impalcatura chiave richiesta per questo canale, la legumain non ha più indotto la morte cellulare, collegando in modo saldo l’esito letale allo squilibrio di calcio.
Quello che potrebbe significare per i futuri trattamenti della leucemia
Alla fine di questa cascata di segnalazione, le cellule leucemiche sperimentano un flusso prolungato di calcio dalle loro riserve interne, abbinato allo spegnimento di un circuito critico di sopravvivenza. Questi cambiamenti insieme spingono le cellule verso la morte programmata, o apoptosi. Per il lettore non specialistico, il messaggio è che la legumain agisce come un sabotatore a due mani: preme entrambi i “pulsanti” della cellula per il rilascio di calcio mentre allo stesso tempo taglia i fili dei suoi sistemi di sicurezza. Sebbene la legumain stessa provenga da parassiti e richiederebbe una valutazione attenta prima di essere usata come terapia, lo studio mette in evidenza μ-OR1, PAR2 e PKA come promettenti target farmacologici. Medicinali che imitano la disruption selettiva dell’equilibrio del calcio nelle cellule leucemiche operata dalla legumain — o che inibiscono strategicamente la PKA — potrebbero un giorno aiutare a trattare pazienti i cui tumori resistono alle terapie correnti.
Citazione: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Parole chiave: leucemia linfoblastica acuta, legumain, segnalazione del calcio, recettori accoppiati a proteine G, apoptosi