Clear Sky Science · ru
Lgmn нацеливает два различных GPCR — PAR2 и µ-OR1 — и вызывает гибель клеток при острой лимфобластной лейкемии через внутриклеточный дисбаланс Ca²⁺, вызванный высвобождением Ca²⁺ из ЭР
Как фермент паразита может помочь в борьбе с детской лейкемией
Острая лимфобластная лейкемия (ОЛЛ) — наиболее частая форма рака крови у детей; хотя существующие методы лечения излечивают многих пациентов, они часто сопровождаются серьёзными побочными эффектами и риском рецидива. В неожиданном повороте события исследователи, изучавшие белок, которым обычные кишечные паразиты атакуют клетки человека, обнаружили, что та же молекула способна селективно направлять лейкемические клетки к самоуничтожению. Проследив, как этот белок нарушает баланс кальция внутри раковых клеток, исследование указывает на новые подходы к уничтожению лейкемических клеток и намекает на перспективные лекарственные мишени.
Скрытое оружие от обычных паразитов
Работа сосредоточена на легумазине — ферменте, секретируемом кишечными и урогенитальными простейшими, такими как Blastocystis и Trichomonas. Паразиты используют легумазин в своём арсенале для вторжения и повреждения тканей хозяина. Ранее было показано, что легумазин может расщеплять рецептор на клетках человека, известный как PAR2, и тем самым вызывать подъём уровня кальция внутри клетки. Но даже при удалении PAR2 или при его нечувствительности к расщеплению легумазин продолжал повышать уровень кальция, что указывало на наличие другого триггера. Поскольку широко применяемый препарат против лейкемии L‑аспарагиназа также действует на PAR2 и на второй рецептор, называемый μ‑OR1, авторы задались вопросом, не использует ли легумазин аналогично более одного пути для нарушения внутренней среды лейкемических клеток.
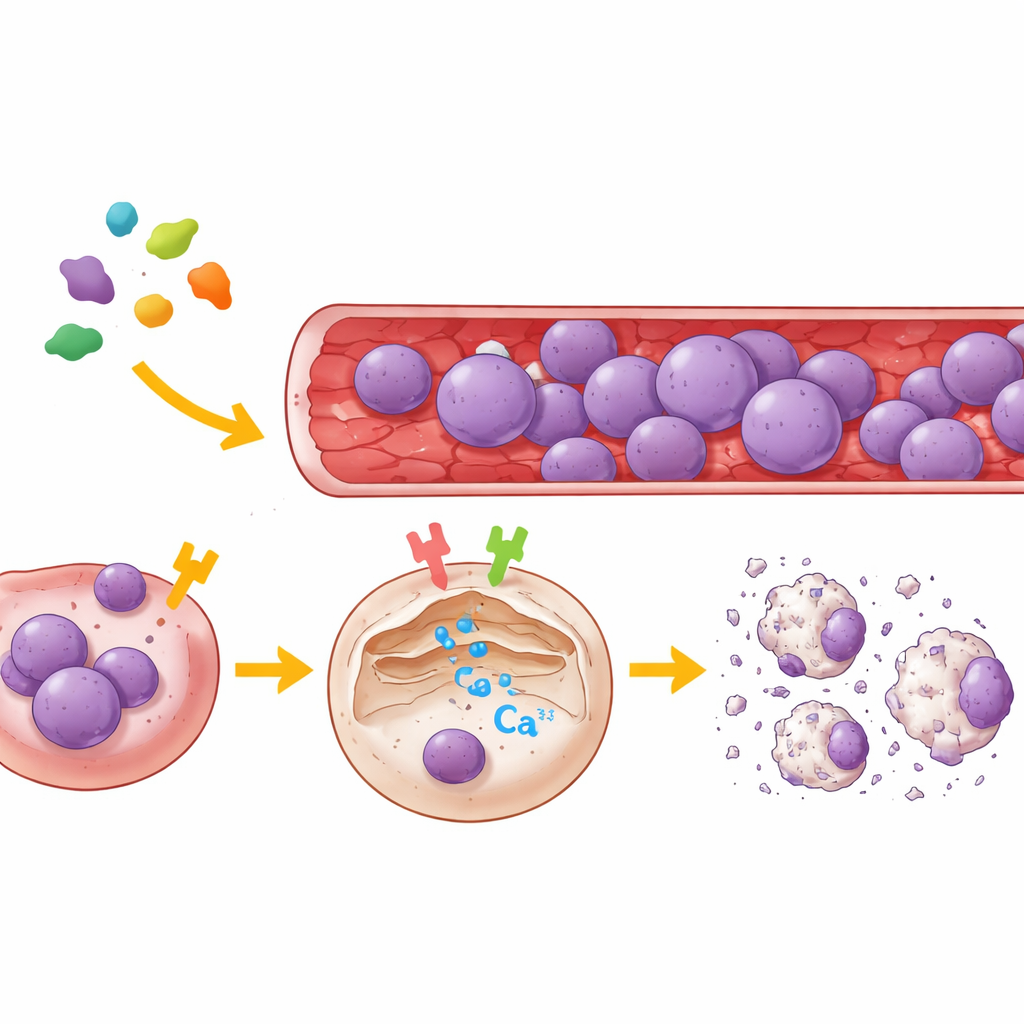
Два клеточных переключателя, контролирующие кальций
Чтобы отобразить мишени легумазина, команда использовала как клетки человеческой почки, так и несколько типов клеток ОЛЛ от пациентов. Они избирательно снижали уровень либо PAR2, либо μ‑OR1 в этих клетках, или блокировали их с помощью высоко специфичных малых молекул‑ингибиторов, а затем отслеживали движение кальция в отдельных клетках с помощью флуоресцентного зонда, сигнализирующего о высвобождении кальция из эндоплазматического ретикулума — основного внутриклеточного хранилища кальция. Результаты были ясны: легумазин вызывал сильный всплеск кальция из этого депо только при активности по крайней мере одного из двух рецепторов. Блокада μ‑OR1 резко ослабляла кальциевый всплеск, тогда как блокада PAR2 давала меньшую, но заметную редукцию. Когда оба рецептора были отключены, легумазин больше не мог вызывать высвобождение кальция. В нескольких линиях B‑ и T‑клеточной лейкемии μ‑OR1 проявился как доминирующий переключатель, в то время как PAR2 играл поддерживающую роль.
Дисбаланс сигналов подталкивает клетки к гибели
Установив, что легумазин действует на оба рецептора, исследователи проследили сигнальные цепочки, которые связывают эти поверхностные переключатели с событиями глубоко внутри клетки. PAR2 взаимодействует с G‑белком, который напрямую активирует фермент PLC, что в свою очередь открывает кальциевые «клапаны» эндоплазматического ретикулума. μ‑OR1, напротив, в основном сигнализирует через другой G‑белок, который подавляет выработку второго мессенджера цАМФ и тем самым угнетает активность киназы белка A (PKA). Обычно PKA накладывает тормозящие регуляции на PLC и поддерживает белок выживания BAD в нефатальном состоянии. Когда легумазин стимулирует μ‑OR1, уровень цАМФ падает, активность PKA снижается, эти тормоза снимаются, и PLC свободно выводит больше кальция из депо. Одновременно BAD переходит в форму, которая ослабляет встроенные клеточные механизмы защиты от гибели.
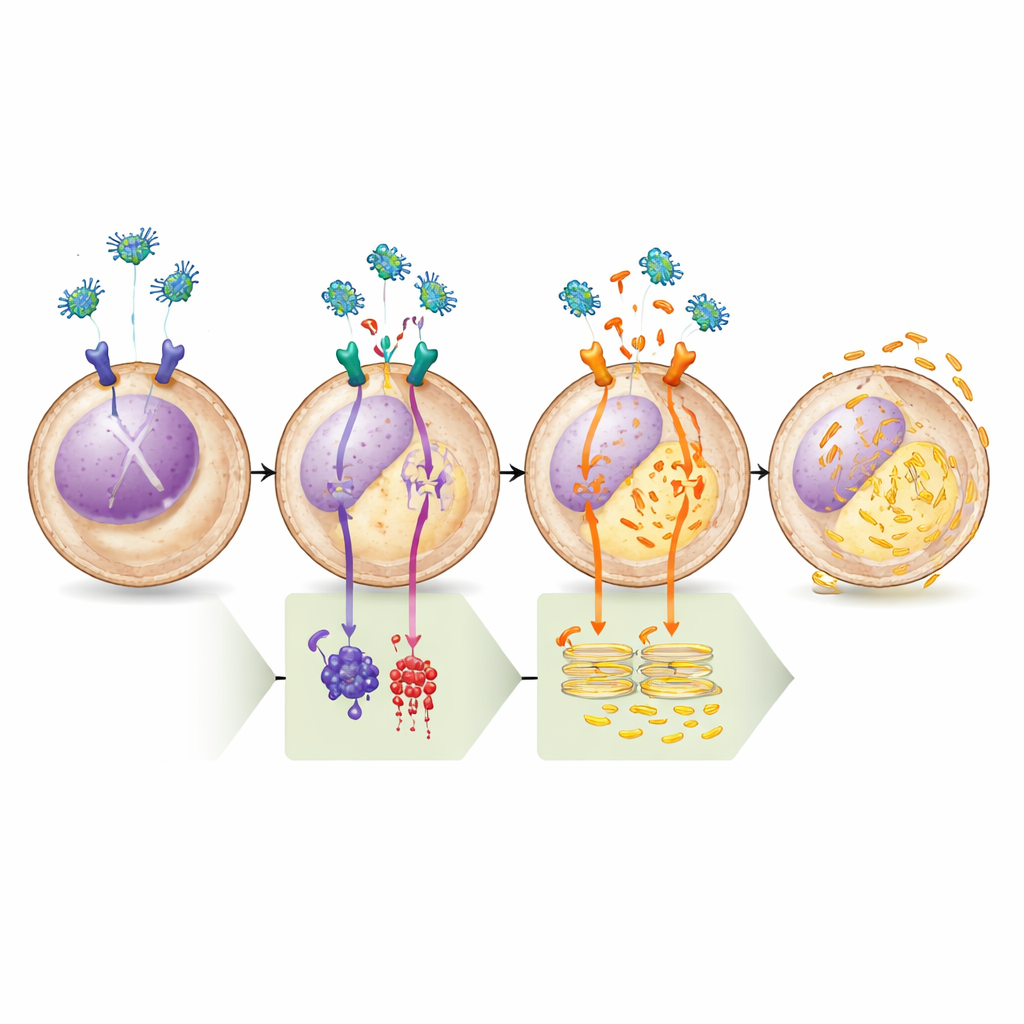
Пошаговое доказательство пути
Команда подтвердила эту модель серией фармакологических экспериментов. Препараты, повышающие цАМФ или напрямую активирующие фермент, его синтезирующий (аденилатциклазу), полностью блокировали способность легумазина опорожнять кальций из эндоплазматического ретикулума, подчёркивая важность ветви μ‑OR1–цАМФ–PKA. Наоборот, высокоселективный ингибитор PKA сам по себе был достаточен для вызова высвобождения кальция, а последующее добавление легумазина не давало дополнительного эффекта, показывая, что как только PKA выключается, путь уже полностью задействован. Биохимические анализы подтвердили, что лечение легумазином снижает фосфатные «маркеры» как на PLC, так и на BAD в местах, известных как контролируемые PKA, что согласуется с предсказанным изменением их активности. Наконец, когда исследователи блокировали кальциевый канал на эндоплазматическом ретикулуме или удаляли ключевой белок‑каркас, необходимый для этого канала, легумазин больше не вызывал гибели клеток, прочно связывая летальный исход с кальциевым дисбалансом.
Что это может означать для будущего лечения лейкемии
В конце этой сигнальной каскады лейкемические клетки испытывают продолжительный приток кальция из внутренних депо вместе с отключением критической цепи выживания. В сумме эти изменения подталкивают клетки к программируемой гибели, или апоптозу. Для неспециалиста суть в том, что легумазин действует как двуручный диверсант: он одновременно нажимает оба «триггера» клетки для высвобождения кальция и перерезает провода её предохранительных систем. Хотя сам легумазин происходит от паразитов и потребовал бы тщательной оценки перед применением в терапии, исследование выделяет μ‑OR1, PAR2 и PKA как перспективные лекарственные мишени. Препараты, имитирующие селективное нарушение кальциевого гомеостаза в лейкемических клетках, вызванное легумазином, — или целенаправленные ингибиторы PKA — могут однажды помочь лечить пациентов с опухолями, устойчивыми к существующим методам терапии.
Цитирование: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Ключевые слова: острая лимфобластная лейкемия, легумазин, кальциевый сигнальный путь, рецепторы, сопряжённые с G-белком, апоптоз