Clear Sky Science · ar
تستهدف Lgmn مستقبلَين مختلفين من عائلة مستقبلات G البروتينية، PAR2 وµ-OR1، وتُحدث موت الخلايا في اللوكيميا الليمفاوية الحادة عبر خلل داخلي في Ca²⁺ ناتج عن إفراز Ca²⁺ من الشبكة الإندوبلازمية
كيف قد يساعد إنزيم طفيلي في مكافحة سرطان الطفولة
اللوكيميا الليمفاوية الحادة (ALL) هي أكثر أنواع سرطانات الدم شيوعًا بين الأطفال، وعلى الرغم من أن العلاجات الحالية قد تَشفِي عددًا كبيرًا من الأطفال، إلا أنها غالبًا ما تصاحبها آثار جانبية قاسية وخطر الانتكاس. في منعطف غير متوقع، اكتشف باحثون يدرسون بروتينًا تستخدمه طفيليات الأمعاء الشائعة لمهاجمة الخلايا البشرية أن نفس الجزيء يمكنه دفع خلايا اللوكيميا بشكل انتقائي نحو تدمير ذاتي. من خلال تتبع كيفية اضطراب هذا البروتين لتوازن الكالسيوم داخل خلايا السرطان، تشير الدراسة إلى طرق جديدة لقتل خلايا اللوكيميا مع تقديم دلائل على أهداف دوائية محتملة.
سلاح خفي من طفيليات شائعة
تركز الدراسة على الليغومين، إنزيم تفرزه طفيليات أولية معوية ومجالها التناسلي مثل Blastocystis وTrichomonas. تستخدم هذه الطفيليات الليغومين كجزء من ترسانتها لاقتحام وإتلاف أنسجة العائل. أظهرت أبحاث سابقة أن الليغومين قادر على قطع مستقبل على الخلايا البشرية يعرف باسم PAR2 وبذلك يطلق ارتفاعًا في مستوى الكالسيوم داخل الخلية. لكن حتى عندما أزيل PAR2 أو جُعل مقاومًا للقطع، ظل الليغومين قادرًا على رفع مستويات الكالسيوم، ما يوحي بوجود محفز آخر. وبما أن دواءً واسع الاستخدام لعلاج اللوكيميا، L‑asparaginase، يعمل أيضًا على PAR2 وعلى مستقبل ثانٍ يسمى μ‑OR1، تساءل الباحثون عما إذا كان الليغومين قد يستخدم بدوره أكثر من مسار واحد لتعكير الحياة الداخلية لخلايا اللوكيميا.
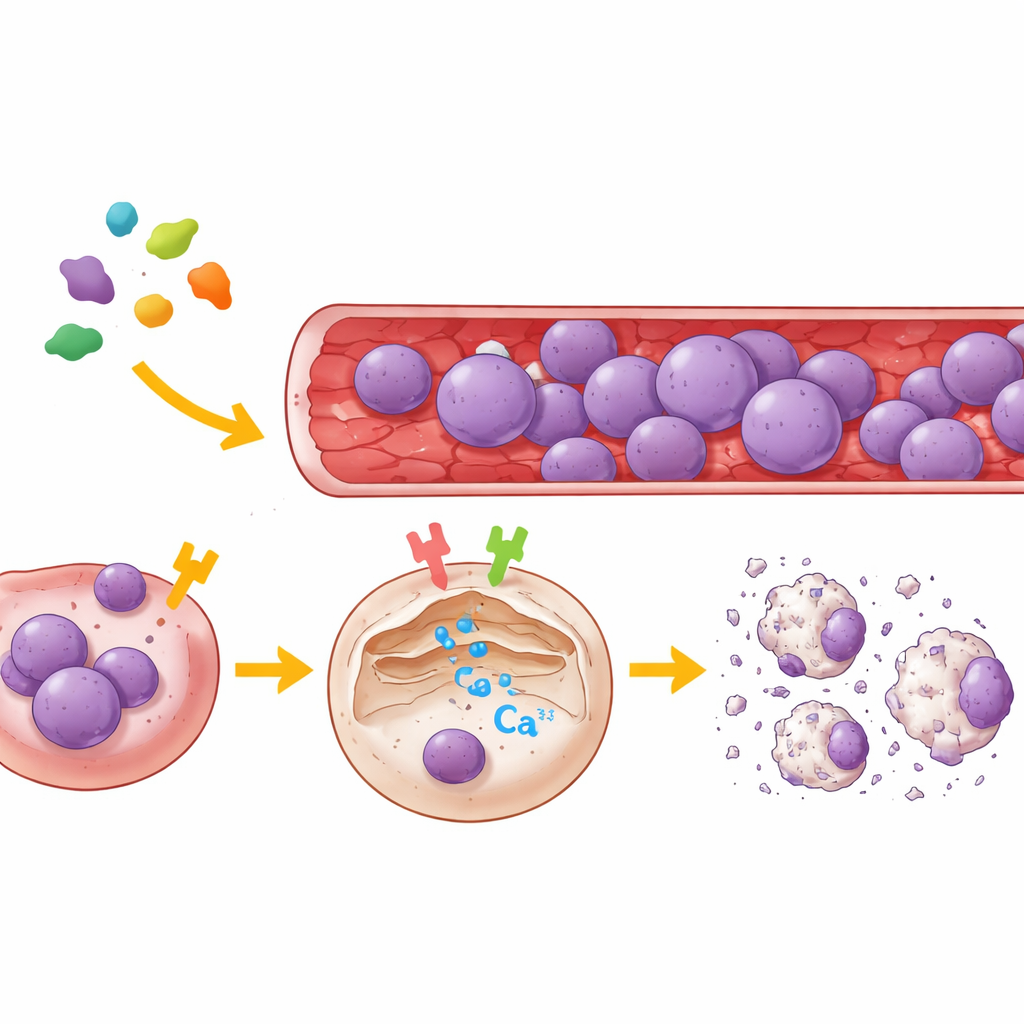
مفتاحان خلويان يتحكمان في الكالسيوم
لتحديد أهداف الليغومين، استخدم الفريق خلايا كلوية بشرية وأنواعًا متعددة من خلايا ALL مأخوذة من مرضى. خفّضوا انتقائيًا إما PAR2 أو μ‑OR1 في هذه الخلايا، أو حَجَبُوهما بمثبطات جزيئية صغيرة شديدة التخصيص، ثم راقبوا تحرّكات الكالسيوم في خلايا مفردة باستخدام مسبار فلوري يُبلغ عن إفراز الكالسيوم من الشبكة الإندوبلازمية، المخبأ الداخلي الرئيسي للكالسيوم في الخلية. النتائج كانت واضحة: دفع الليغومين موجة قوية من الكالسيوم خارج هذا المخزن فقط عندما كان واحد على الأقل من المستقبلين نشطًا. أدى تثبيط μ‑OR1 إلى تقليل حاد في الاندفاعة الكلسيّة، بينما أحدث حجب PAR2 انخفاضًا أصغر لكنه ملحوظ. عندما تعطل كلا المستقبلين، لم يعد الليغومين قادرًا على إحداث إفراز الكالسيوم. عبر عدة سلالات من خلايا اللمف البائية والتائية، برز μ‑OR1 كمفتاح مهيمن، مع دور مساعد لـ PAR2.
إشارات غير متوازنة تدفع الخلايا نحو الموت
بعد أن ثبت أن الليغومين يستهدف كلا المستقبلين، تتبع الباحثون سلاسل الإشارة التي تربط هذه المفاتيح السطحية بأحداثٍ داخل الخلية. يرتبط PAR2 ببروتين G ينشط مباشرة إنزيمًا يسمى PLC، والذي بدوره يفتح صمامات الكالسيوم على الشبكة الإندوبلازمية. بالمقابل، يرسِل μ‑OR1 في الأساس إشارة عبر بروتين G آخر يخفض إنتاج جزيء الرسول cAMP وبذلك يهدئ إنزيمًا يُعرف باسم بروتين كيناز A (PKA). عادةً ما يضع PKA «مكابح» تثبيطية على PLC ويحافظ على نشاط بروتين البقاء BAD في حالة غير مميتة. عندما ينبه الليغومين μ‑OR1، تنخفض مستويات cAMP، يتراجع نشاط PKA، وتُرفع هذه المكابح، ويصبح PLC حرًا لدفع المزيد من الكالسيوم من المخازن. في الوقت نفسه، ينتقل BAD إلى شكل يضعف دفاعات الخلية الذاتية ضد الموت.
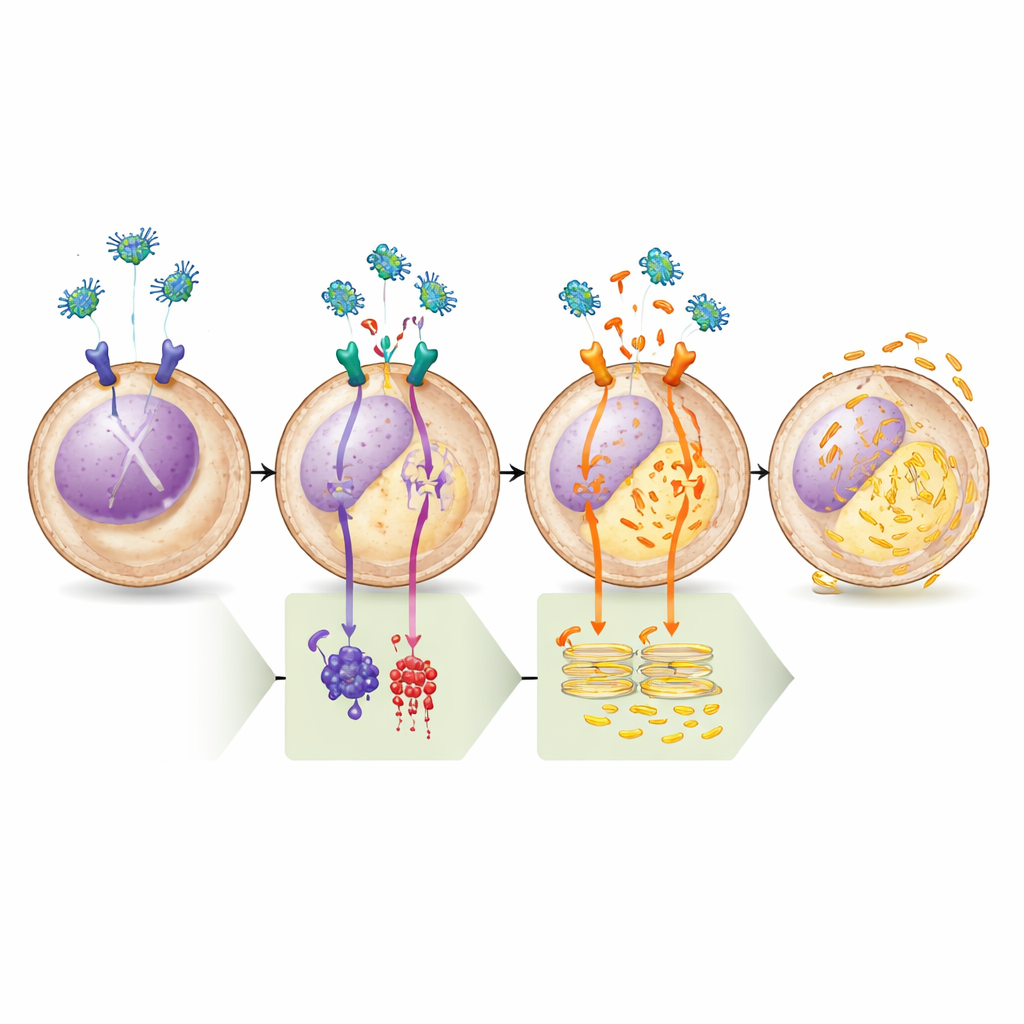
إثبات المسار خطوة بخطوة
تحقق الفريق من هذا النموذج عبر سلسلة من الاختبارات الدوائية. العقاقير التي رفعت مستوى cAMP أو نشطت مباشرةً الأنزيم الذي يصنعه (adenylate cyclase) منعت تمامًا قدرة الليغومين على تفريغ الكالسيوم من الشبكة الإندوبلازمية، ما يؤكد أهمية فرع μ‑OR1–cAMP–PKA. وعلى النقيض، كان مثبط PKA انتقائيًا عاليًا وحده كافيًا لإطلاق إفراز الكالسيوم، وإضافة الليغومين بعد ذلك لم تُحدث أي تأثير إضافي، مما يدل على أنه بمجرد إيقاف PKA يكون المسار قد تم تفعيله بالكامل. أكدت التحليلات البيوكيميائية أن علاج الليغومين خفض علامات الفسفرة على كل من PLC وBAD عند مواقع معروفة أنها تخضع للتحكم بواسطة PKA، متطابقة مع التغير المتوقع في نشاطهما. أخيرًا، عندما حجب الباحثون قناة الكالسيوم على الشبكة الإندوبلازمية أو أزالوا بروتين سقالات أساسيًا مطلوبًا لهذه القناة، لم يعد الليغومين يحفز موت الخلايا، رابطًا النتيجة المميتة ارتباطًا وثيقًا بخلل توازن الكالسيوم.
ماذا قد يعني هذا لعلاجات اللوكيميا المستقبلية
في ختام سلسلة الإشارات هذه، تتعرض خلايا اللوكيميا لفيض مستمر من الكالسيوم من مخازنها الداخلية، مصحوبًا بإيقاف دائرة بقاء حيوية. معًا، تدفع هذه التغييرات الخلايا نحو الموت المبرمج أو الاستماتة. للقراء العامين، الرسالة أن الليغومين يعمل كخائن ذا يدين: يضغط كليهما على أزرار «التفعيل» لإطلاق الكالسيوم بينما يقطع في الوقت نفسه أسلاك أنظمة الأمان. على الرغم من أن الليغومين نفسه مصدره طفيليات وسيتطلب تقييمًا دقيقًا قبل استخدامه كعلاج، تبرز الدراسة μ‑OR1 وPAR2 وPKA كأهداف دوائية واعدة. قد تساعد الأدوية التي تحاكي اضطراب الليغومين الانتقائي في توازن الكالسيوم داخل خلايا اللوكيميا — أو التي تعيق PKA بشكل استراتيجي — يومًا ما في علاج المرضى الذين تقاوم سرطاناتهم العلاجات الحالية.
الاستشهاد: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
الكلمات المفتاحية: اللوكيميا الليمفاوية الحادة, الليغومين, إشارة الكالسيوم, مستقبلات مرتبطة بالبروتين G, موت الخلايا المبرمج (الاستماتة)