Clear Sky Science · de
Lgmn zielt auf zwei verschiedene GPCRs, PAR2 und µ-OR1, und induziert Zelltod bei akuter lymphatischer Leukämie durch ein intrazelluläres Ca²⁺-Ungleichgewicht, ausgelöst durch ER-Ca²⁺-Freisetzung
Wie ein Parasiten-Enzym bei der Bekämpfung von Kinderleukämie helfen könnte
Die akute lymphatische Leukämie (ALL) ist der häufigste Blutkrebs im Kindesalter. Obwohl gegenwärtige Therapien viele Kinder heilen können, gehen sie oft mit starken Nebenwirkungen und dem Risiko eines Rückfalls einher. In einer unerwarteten Wendung entdeckten Forschende, die ein Protein untersuchten, das von verbreiteten Darmparasiten zur Attacke auf menschliche Zellen genutzt wird, dass dasselbe Molekül Leukämiezellen selektiv in Richtung Selbstzerstörung treiben kann. Indem sie nachverfolgten, wie dieses Protein das Calciumgleichgewicht in Krebszellen stört, weist die Studie auf neue Wege hin, Leukämiezellen zu töten, und deutet zugleich auf mögliche neue Angriffspunkte für Medikamente.
Eine verborgene Waffe aus gewöhnlichen Parasiten
Im Mittelpunkt der Arbeit steht Legumain, ein Enzym, das von intestinalen und urogenitalen Protozoen wie Blastocystis und Trichomonas ausgeschieden wird. Diese Parasiten verwenden Legumain als Teil ihres Arsenals, um Wirtsgewebe zu durchdringen und zu schädigen. Frühere Untersuchungen zeigten, dass Legumain einen Rezeptor auf menschlichen Zellen namens PAR2 schneiden kann und dadurch einen Anstieg des intrazellulären Calciums auslöst. Doch selbst wenn PAR2 entfernt oder gegen das Schneiden resistent gemacht wurde, gelang es Legumain weiterhin, die Calciumwerte zu erhöhen, was darauf hindeutet, dass ein weiterer Auslöser beteiligt ist. Da ein weitverbreitetes Leukämie-Medikament, L-Asparaginase, ebenfalls auf PAR2 und auf einen zweiten Rezeptor namens μ-OR1 wirkt, fragten die Autoren, ob Legumain möglicherweise ebenfalls mehr als einen Weg nutzt, um das Innenleben von Leukämiezellen zu stören.
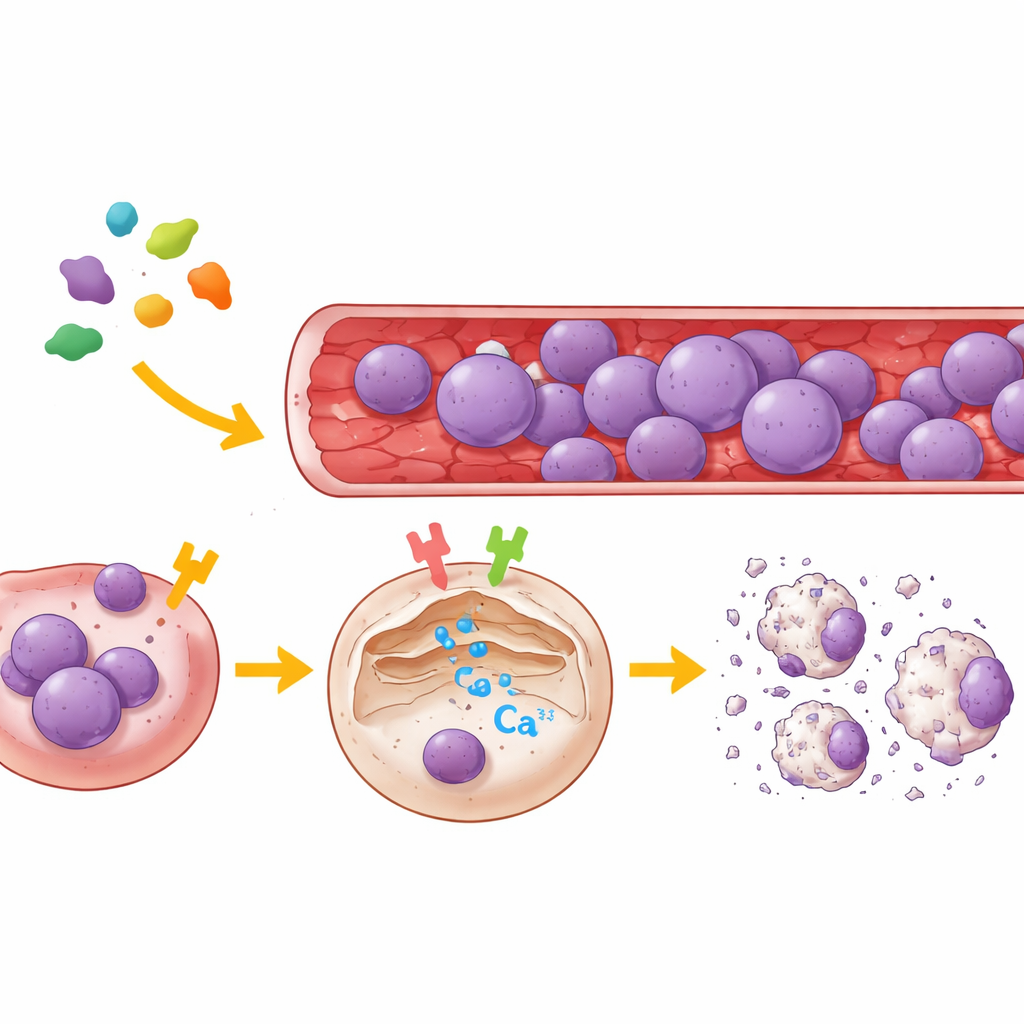
Zwei Zellschalter, die Calcium steuern
Um die Ziele von Legumain zu kartieren, nutzte das Team sowohl menschliche Nierenzellen als auch mehrere Typen von ALL-Zellen aus Patientenproben. Sie reduzierten gezielt entweder PAR2 oder μ-OR1 in diesen Zellen oder blockierten sie mit hochspezifischen niedermolekularen Inhibitoren und beobachteten dann Calciumbewegungen in Einzelzellen mit einer fluoreszenten Sonde, die die Calciumfreisetzung aus dem endoplasmatischen Retikulum – dem wichtigsten intrazellulären Calcium-Speicher – meldet. Die Ergebnisse waren eindeutig: Legumain löste einen starken Ausstoß von Calcium aus diesem Speicher nur dann aus, wenn mindestens einer der beiden Rezeptoren aktiv war. Die Hemmung von μ-OR1 schwächte den Calciumschub stark ab, während die Blockade von PAR2 eine kleinere, aber spürbare Reduktion bewirkte. Wenn beide Rezeptoren deaktiviert waren, konnte Legumain keine Calciumfreisetzung mehr hervorrufen. In mehreren B‑Zell- und T‑Zell-Leukämielinien erwies sich μ-OR1 als der dominierende Schalter, während PAR2 unterstützend wirkte.
Unbalancierte Signale kippen Zellen in Richtung Tod
Nachdem nachgewiesen war, dass Legumain beide Rezeptoren trifft, verfolgten die Forschenden die Signalketten, die diese Oberflächenschalter mit Ereignissen tief im Zellinneren verbinden. PAR2 koppelt an ein G-Protein, das direkt ein Enzym namens PLC aktiviert, das wiederum Calciumventile im endoplasmatischen Retikulum öffnet. μ-OR1 signalisiert dagegen hauptsächlich über ein anderes G-Protein, das die Produktion des Botenmoleküls cAMP dämpft und damit ein Enzym namens Proteinkinase A (PKA) beruhigt. Normalerweise setzt PKA hemmende „Bremsen“ auf PLC und hält die Aktivität eines Überlebensproteins namens BAD in einem nicht tödlichen Zustand. Wenn Legumain μ-OR1 stimuliert, sinken die cAMP-Spiegel, die PKA-Aktivität fällt, diese Bremsen werden gelöst, und PLC kann mehr Calcium aus den Speichern treiben. Gleichzeitig verändert sich BAD in eine Form, die die eingebauten Abwehrmechanismen der Zelle gegen den Tod schwächt.
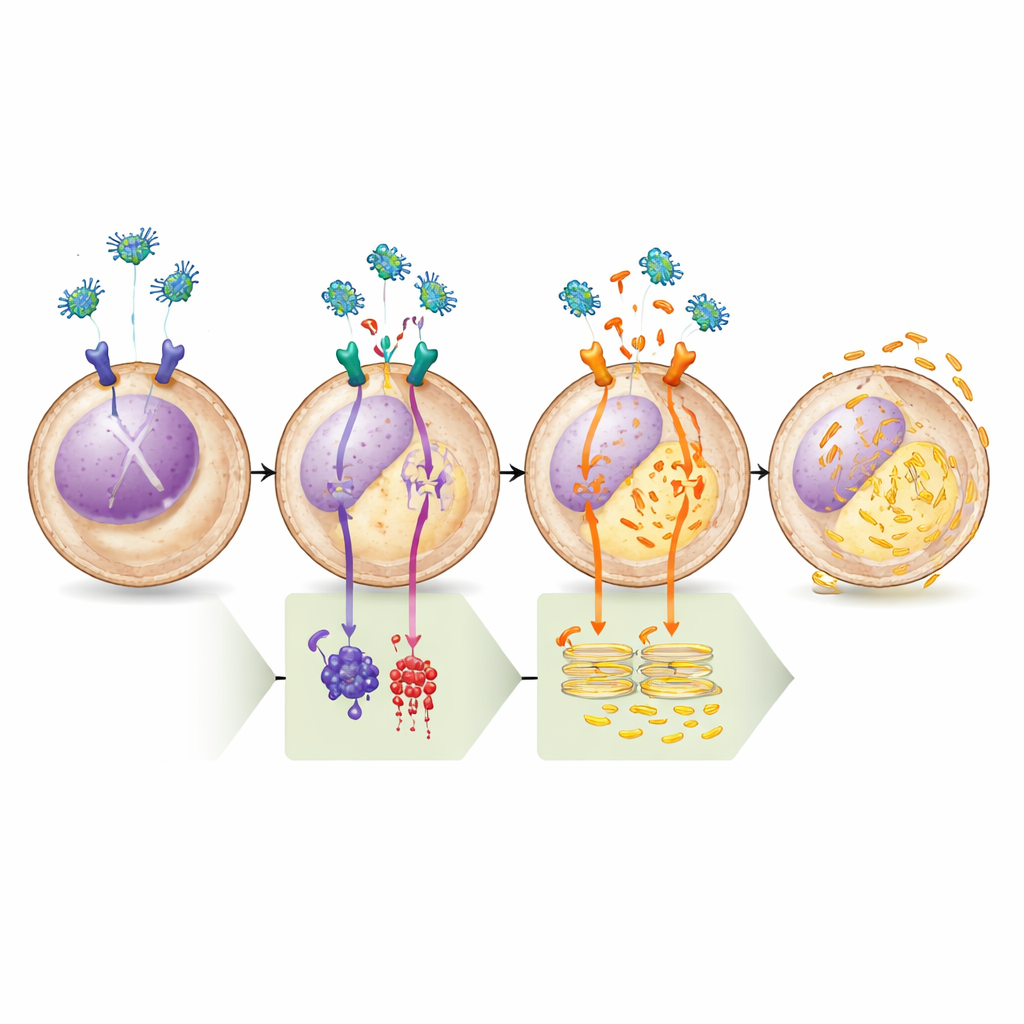
Den Weg Schritt für Schritt nachweisen
Das Team bestätigte dieses Modell mit einer Reihe pharmakologischer Tests. Wirkstoffe, die cAMP erhöhten oder das Enzym, das es herstellt (Adenylatcyclase), direkt aktivierten, blockierten die Fähigkeit von Legumain, Calcium aus dem endoplasmatischen Retikulum zu entleeren, und unterstrichen damit die Bedeutung des μ-OR1–cAMP–PKA-Zweigs. Umgekehrt reichte ein hochselektiver PKA-Inhibitor allein aus, um die Calciumfreisetzung auszulösen; die anschließende Zugabe von Legumain zeigte keinen weiteren Effekt, was beweist, dass der Weg nach Abschaltung von PKA bereits vollständig aktiviert ist. Biochemische Analysen bestätigten, dass die Legumain-Behandlung die Phosphat-„Marken“ sowohl auf PLC als auch auf BAD an Stellen verringerte, die bekanntermaßen von PKA kontrolliert werden, und damit die vorhergesagte Änderung ihrer Aktivität widerspiegelt. Schließlich, wenn die Forschenden den Calciumkanal im endoplasmatischen Retikulum blockierten oder ein entscheidendes Gerüstprotein entfernten, das für diesen Kanal erforderlich ist, induzierte Legumain keinen Zelltod mehr, was das tödliche Ergebnis eindeutig an das Calciumungleichgewicht koppelt.
Was das für künftige Leukämiebehandlungen bedeuten könnte
Am Ende dieser Signalkaskade erfahren Leukämiezellen eine anhaltende Flut von Calcium aus ihren internen Speichern, gekoppelt mit der Abschaltung einer kritischen Überlebensschaltung. Zusammen treiben diese Veränderungen die Zellen in den programmierten Zelltod, die Apoptose. Für den allgemeinen Leser lautet die Botschaft: Legumain agiert wie ein zweihändiger Saboteur – es betätigt beide „Startknöpfe“ der Zelle für die Calciumfreisetzung und durchtrennt gleichzeitig die Leitungen zu ihren Sicherheitssystemen. Obwohl Legumain selbst von Parasiten stammt und vor einem therapeutischen Einsatz sorgfältig geprüft werden müsste, hebt die Studie μ-OR1, PAR2 und PKA als vielversprechende medikamentöse Zielstrukturen hervor. Wirkstoffe, die Legumains selektive Störung des Calciumgleichgewichts in Leukämiezellen nachahmen – oder die strategisch PKA hemmen – könnten eines Tages dazu beitragen, Patienten zu behandeln, deren Tumoren gegen aktuelle Therapien resistent sind.
Zitation: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Schlüsselwörter: akute lymphatische Leukämie, Legumain, Calcium-Signalübertragung, G-Protein-gekoppelte Rezeptoren, Apoptose