Clear Sky Science · ja
Lgmnは2つの異なるGPCR、PAR2およびµ-OR1を標的とし、小胞体のCa²⁺放出によって引き起こされる細胞内Ca²⁺不均衡を介して急性リンパ性白血病の細胞死を誘導する
寄生虫由来酵素が小児白血病治療に役立つかもしれない理由
急性リンパ性白血病(ALL)は小児に最も多くみられる血液がんで、現在の治療で多くの子どもは治癒しますが、副作用が厳しく再発のリスクも残ります。思いがけない発見として、腸内や尿生殖管に寄生する一般的な原虫がヒト細胞へ攻撃する際に用いるタンパク質を研究していたところ、同じ分子が白血病細胞を選択的に自己破壊へと導くことが明らかになりました。本研究は、このタンパク質ががん細胞内のカルシウムバランスをどのように撹乱するかを追跡することで、白血病細胞を殺す新たな方法を示し、同時に新しい薬物標的の可能性を示唆しています。
一般的な寄生虫からの隠れた武器
本研究の焦点はレグマイン(legumain)という酵素で、BlastocystisやTrichomonasなどの腸管・泌尿生殖管原虫が分泌します。これらの寄生虫はレグマインを利用して宿主組織へ侵入し損傷を与えます。以前の研究では、レグマインがヒト細胞上の受容体PAR2を切断し、その結果として細胞内カルシウム濃度が上昇することが示されていました。しかしPAR2を除去するか切断に抵抗性にしても、レグマインは依然としてカルシウム濃度を上げることが分かり、別のトリガーが働いていることが示唆されました。広く用いられる白血病薬であるL-アスパラギナーゼがPAR2ともう一つの受容体であるμ-OR1にも作用することから、研究者らはレグマインが白血病細胞の内部で複数の経路を使っているかもしれないと考えました。
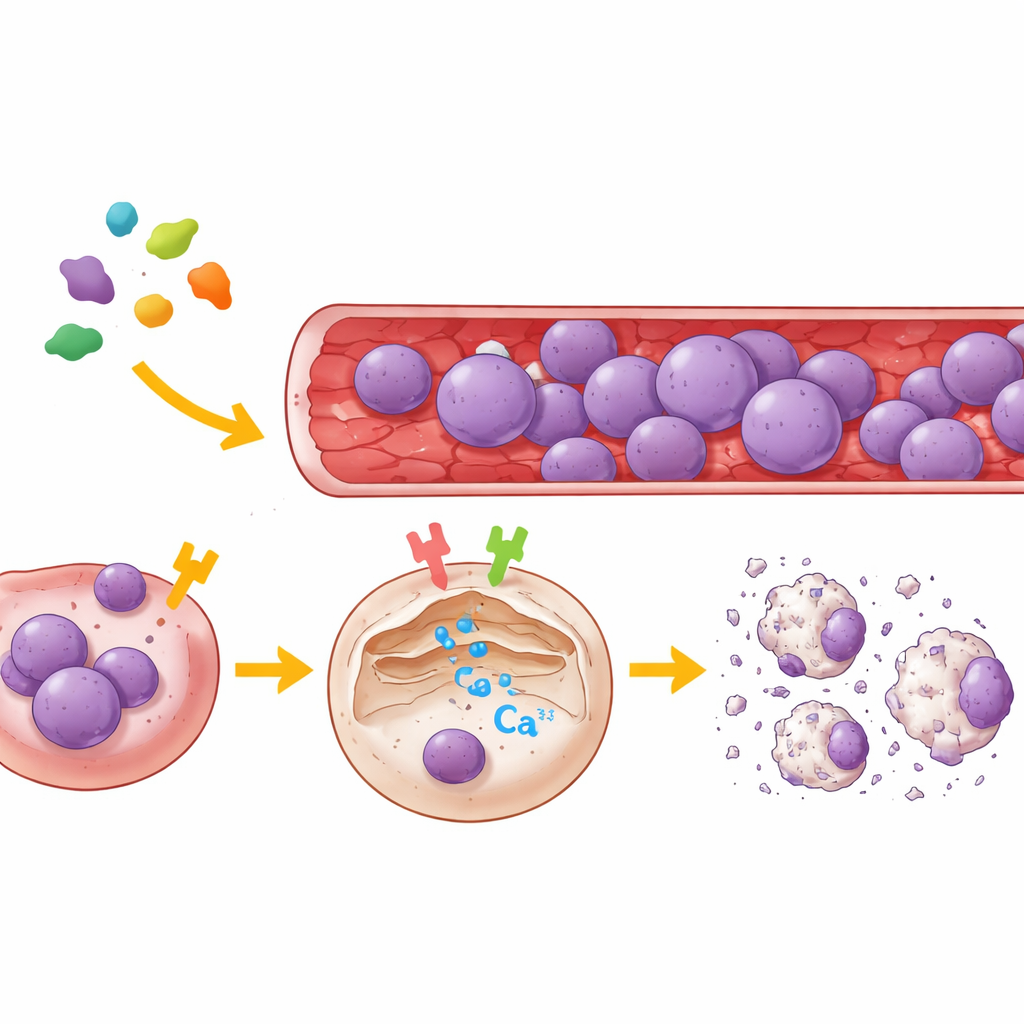
カルシウムを制御する二つのスイッチ
レグマインの標的を明らかにするため、研究チームはヒト腎臓細胞と患者由来の複数のALL細胞株を用いました。これらの細胞でPAR2またはμ-OR1のいずれかを選択的に減少させるか、極めて特異的な低分子阻害剤でブロックし、細胞内単一細胞レベルで蛍光プローブを用いて小胞体(細胞内の主要なカルシウム貯蔵庫)からのカルシウム放出を観察しました。結果は明瞭でした:少なくとも一方の受容体が活性化されている場合にのみ、レグマインはこの貯蔵庫からの強いカルシウム放出を引き起こしました。μ-OR1を阻害するとカルシウムの急増は大幅に鈍り、PAR2を遮断するとより小さいものの明確な減少が見られました。両方の受容体が無効化されると、レグマインはもはやカルシウム放出を誘発しませんでした。複数のB細胞系およびT細胞系白血病株においては、μ-OR1が優勢なスイッチとして機能し、PAR2は補助的な役割を果たしていることが示されました。
不均衡なシグナルが細胞を死へと傾ける
レグマインが両方の受容体に作用することを確立した後、研究者らはこれらの表面スイッチが細胞内部の出来事につながるシグナル伝達経路を追跡しました。PAR2はGタンパク質と結合してPLCという酵素を直接活性化し、これが小胞体上のカルシウム弁を開きます。これに対しμ-OR1は主に別のGタンパク質を介してシグナルを送り、セカンドメッセンジャーであるcAMPの生成を抑えてプロテインキナーゼA(PKA)の活動を低下させます。通常、PKAはPLCに対して抑制的な“ブレーキ”をかけ、さらに生存を助けるタンパク質BADの活性を非致死的な状態に保ちます。レグマインがμ-OR1を刺激するとcAMPレベルは低下し、PKA活性が落ち、これらのブレーキは解除されてPLCが貯蔵からより多くのカルシウムを排出できるようになります。同時にBADは細胞の死に対する防御を弱める形態に変化します。
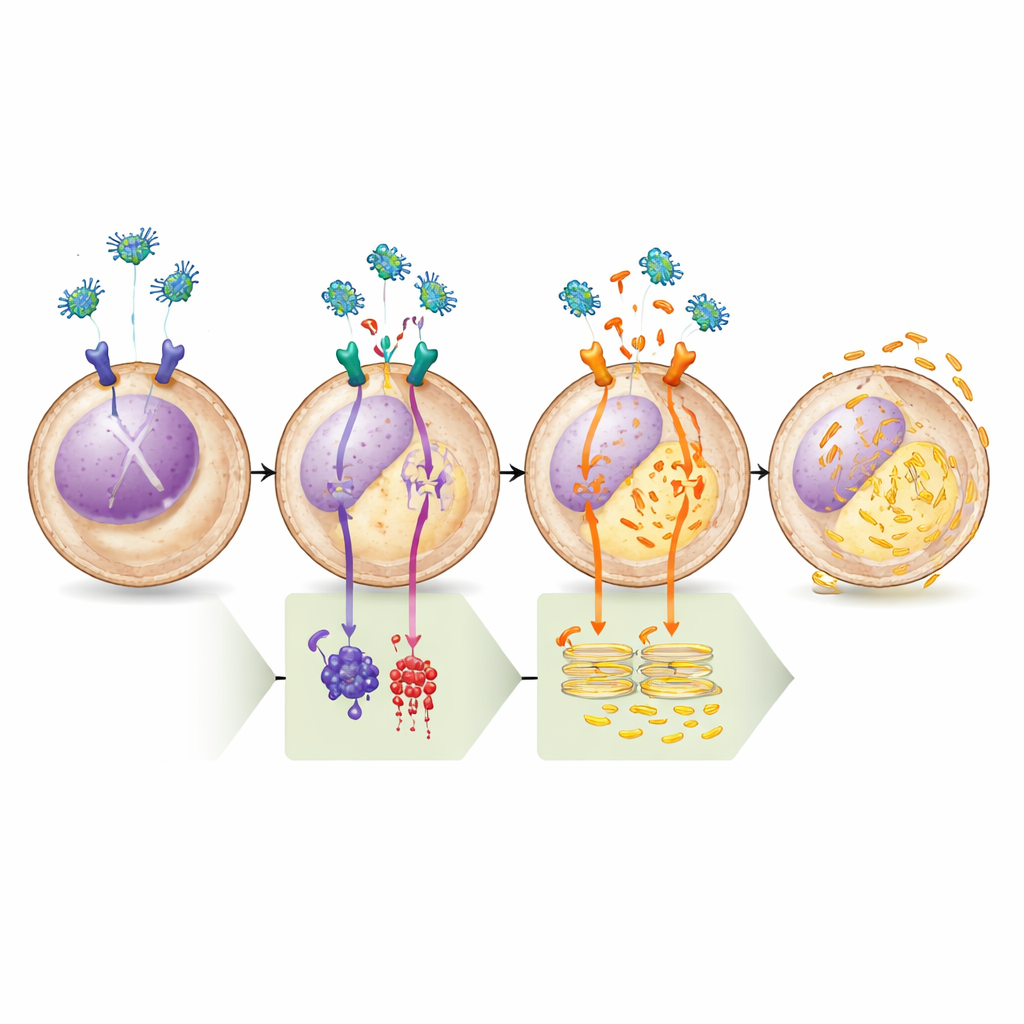
段階を追った経路の実証
チームは一連の薬理学的試験でこのモデルを検証しました。cAMPを増強する薬剤やcAMPを合成する酵素(アデニル酸シクラーゼ)を直接活性化する薬剤は、レグマインが小胞体からカルシウムを放出する能力を完全に阻害し、μ-OR1–cAMP–PKA経路の重要性を裏付けました。逆に、極めて選択的なPKA阻害剤単独でカルシウム放出を誘発し、その後にレグマインを添加してもさらなる効果は見られず、PKAが一度オフになると経路は完全に作動することが示されました。生化学的解析では、レグマイン処理によりPLCとBADの両方におけるPKAによって制御される既知の部位のリン酸化“タグ”が低下し、これらの活性変化の予測と一致しました。最後に、小胞体上のカルシウムチャネルをブロックするか、このチャネルに必要な重要な足場タンパク質を除去すると、レグマインはもはや細胞死を誘導せず、致死結果がカルシウム不均衡にしっかり結び付いていることが確かめられました。
将来の白血病治療への含意
このシグナルカスケードの終点では、白血病細胞は内部貯蔵から持続的なカルシウムのあふれを経験し、同時に重要な生存回路が遮断されます。これらの変化が合わさって細胞をプログラムされた死(アポトーシス)へと押し出します。一般向けに言えば、レグマインは二刀流のサボタージュを行うようなもので、カルシウム放出の“進行”ボタンを同時に押しつつ安全装置の配線を切断します。レグマイン自体は寄生虫由来であり治療として用いるには慎重な評価が必要ですが、本研究はμ-OR1、PAR2、PKAを有望な薬物標的として浮かび上がらせます。レグマインが白血病細胞のカルシウムバランスを選択的に撹乱する作用を模倣する薬剤や、戦略的にPKAを抑制する薬は、将来的に既存治療に抵抗する患者の治療に役立つ可能性があります。
引用: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
キーワード: 急性リンパ性白血病, レグマイン, カルシウムシグナル伝達, Gタンパク質共役受容体, アポトーシス