Clear Sky Science · es
Lgmn apunta a dos GPCR distintos, PAR2 y µ-OR1, e induce la muerte celular en leucemia linfoblástica aguda mediante un desequilibrio intracelular de Ca²⁺ desencadenado por la liberación de Ca²⁺ del RE
Cómo una enzima parasitaria puede ayudar a combatir la leucemia infantil
La leucemia linfoblástica aguda (LLA) es el cáncer de sangre infantil más común y, aunque los tratamientos actuales pueden curar a muchos niños, a menudo conllevan efectos secundarios severos y riesgo de recaída. En un giro inesperado, investigadores que estudiaban una proteína usada por parásitos intestinales comunes para atacar células humanas han descubierto que esa misma molécula puede inducir selectivamente la autodestrucción de células leucémicas. Al rastrear cómo esta proteína altera el equilibrio del calcio dentro de las células cancerosas, el estudio apunta a nuevas formas de eliminar células leucémicas y sugiere posibles blancos farmacológicos.
Un arma oculta de parásitos comunes
El trabajo se centra en la legumasa, una enzima secretada por protozoos intestinales y urogenitales como Blastocystis y Trichomonas. Estos parásitos usan la legumasa como parte de su arsenal para invadir y dañar tejidos del huésped. Investigaciones previas mostraron que la legumasa puede cortar un receptor en células humanas conocido como PAR2 y, al hacerlo, provocar un aumento de calcio dentro de la célula. Pero incluso cuando PAR2 se eliminó o se hizo resistente al corte, la legumasa seguía elevando los niveles de calcio, lo que implica que había otro desencadenante en juego. Dado que un fármaco ampliamente utilizado contra la leucemia, la L-asparaginasa, actúa también sobre PAR2 y sobre un segundo receptor llamado μ-OR1, los autores se preguntaron si la legumasa podría usar igualmente más de una vía para perturbar la vida interna de las células leucémicas.
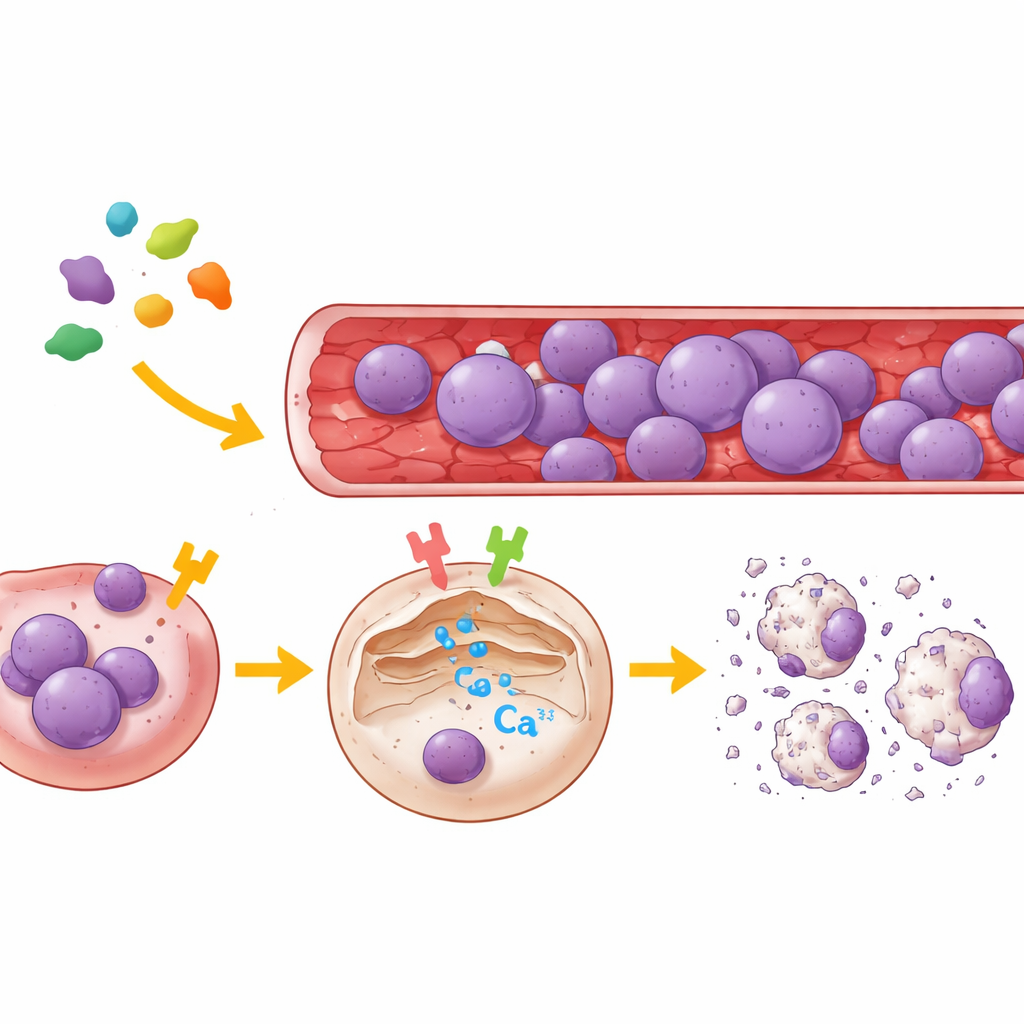
Dos interruptores celulares que controlan el calcio
Para mapear los blancos de la legumasa, el equipo usó tanto células renales humanas como varios tipos de células de LLA procedentes de pacientes. Redujeron selectivamente PAR2 o μ-OR1 en estas células, o los bloquearon con inhibidores moleculares pequeños altamente específicos, y luego observaron los movimientos de calcio en células individuales usando una sonda fluorescente que informa sobre la liberación de calcio del retículo endoplásmico, el principal almacén interno de calcio de la célula. Los resultados fueron claros: la legumasa provocó una fuerte oleada de calcio fuera de este depósito solo cuando al menos uno de los dos receptores estaba activo. Inhibir μ-OR1 redujo bruscamente el aumento de calcio, mientras que bloquear PAR2 produjo una disminución menor pero perceptible. Cuando ambos receptores fueron desactivados, la legumasa ya no pudo provocar la liberación de calcio. En varias líneas leucémicas de células B y T, μ-OR1 emergió como el interruptor dominante, con PAR2 desempeñando un papel de apoyo.
Señales desequilibradas que inclinan a las células hacia la muerte
Habiendo establecido que la legumasa afecta a ambos receptores, los investigadores siguieron las cadenas de señalización que conectan estos interruptores de la superficie con eventos en el interior de la célula. PAR2 se acopla a una proteína G que activa directamente una enzima llamada PLC, que a su vez abre las válvulas de calcio en el retículo endoplásmico. μ-OR1, por el contrario, señala principalmente a través de una proteína G diferente que reduce la producción del mensajero cAMP y, de ese modo, apaga una enzima conocida como proteína quinasa A (PKA). Normalmente, la PKA ejerce frenos inhibitorios sobre PLC y mantiene la actividad de una proteína de supervivencia llamada BAD en un estado no letal. Cuando la legumasa estimula μ-OR1, los niveles de cAMP caen, la actividad de la PKA disminuye, estos frenos se liberan y PLC queda libre para impulsar más liberación de calcio desde los depósitos. Al mismo tiempo, BAD cambia a una forma que debilita las defensas internas de la célula contra la muerte.
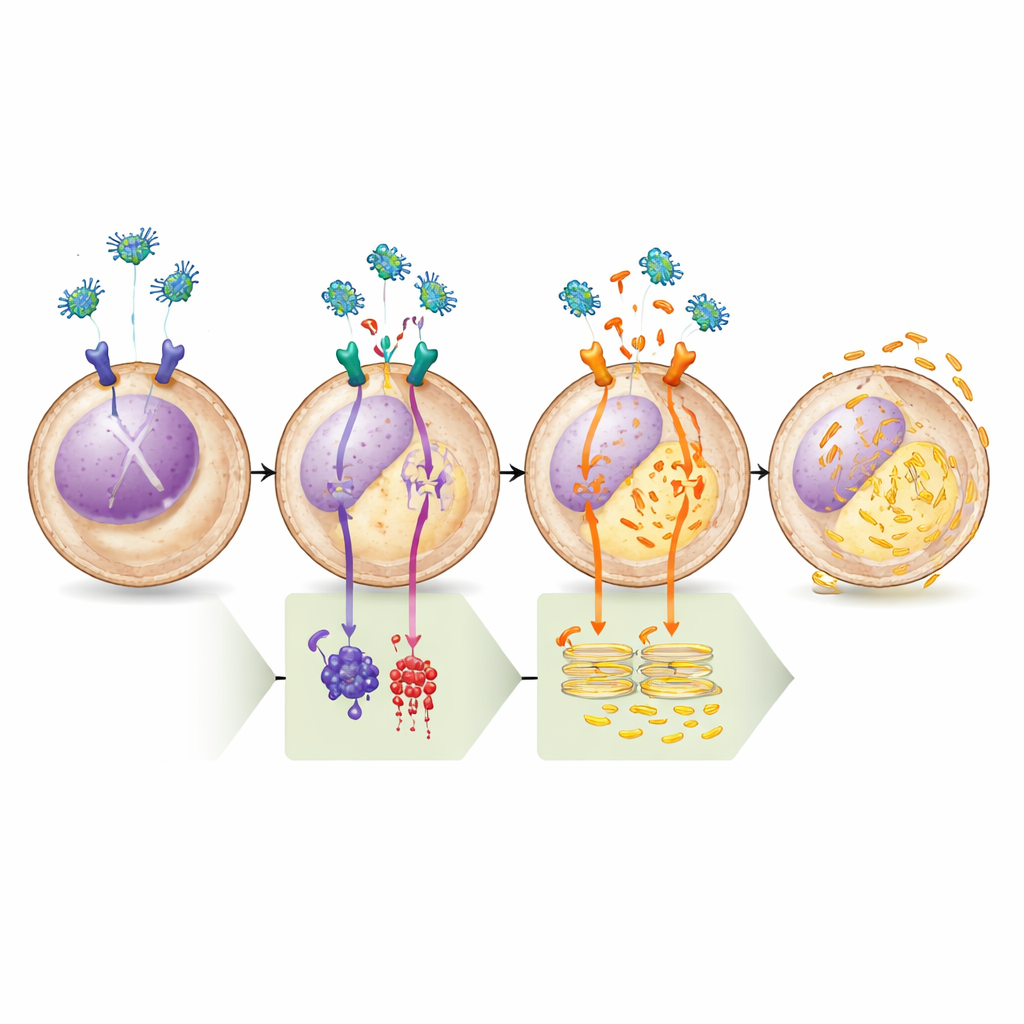
Demostrando la vía paso a paso
El equipo verificó este modelo con una serie de ensayos farmacológicos. Fármacos que aumentaron el cAMP o activaron directamente la enzima que lo sintetiza (adenilato ciclasa) bloquearon por completo la capacidad de la legumasa para vaciar el calcio del retículo endoplásmico, subrayando la importancia de la rama μ-OR1–cAMP–PKA. Por el contrario, un inhibidor de PKA altamente selectivo por sí solo fue suficiente para desencadenar la liberación de calcio, y añadir legumasa posteriormente no produjo efecto adicional, mostrando que una vez que la PKA se apaga, la vía ya está completamente activada. Los análisis bioquímicos confirmaron que el tratamiento con legumasa redujo las “etiquetas” de fosfato tanto en PLC como en BAD en sitios conocidos por ser controlados por la PKA, coincidiendo con el cambio previsto en su actividad. Finalmente, cuando los investigadores bloquearon el canal de calcio del retículo endoplásmico o eliminaron una proteína andamio clave necesaria para ese canal, la legumasa dejó de inducir la muerte celular, vinculando firmemente el desenlace letal al desequilibrio de calcio.
Qué podría significar esto para futuros tratamientos de la leucemia
Al final de esta cascada de señalización, las células leucémicas experimentan un flujo sostenido de calcio desde sus depósitos internos, junto con el cierre de un circuito crítico de supervivencia. En conjunto, estos cambios empujan a las células hacia la muerte programada, o apoptosis. Para el lector no especializado, el mensaje es que la legumasa actúa como un saboteador de dos manos: presiona ambos “botones de salida” de la célula para la liberación de calcio mientras, al mismo tiempo, corta los cables de sus sistemas de seguridad. Aunque la legumasa proviene de parásitos y requeriría una evaluación cuidadosa antes de considerarse como terapia, el estudio destaca a μ-OR1, PAR2 y la PKA como objetivos farmacológicos prometedores. Medicamentos que imiten la perturbación selectiva del equilibrio del calcio en células leucémicas provocada por la legumasa —o que inhiban estratégicamente la PKA— podrían algún día ayudar a tratar a pacientes cuyos cánceres resisten las terapias actuales.
Cita: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Palabras clave: leucemia linfoblástica aguda, legumasa, señalización por calcio, receptores acoplados a proteína G, apoptosis