Clear Sky Science · he
Lgmn מכוון שני GPCRים נפרדים, PAR2 ו-µ-OR1, ומעורר מוות תאי בלוקמיה לימפובלסטית חריפה באמצעות חוסר איזון תאי של Ca²⁺ המופעל על ידי שחרור Ca²⁺ מ-ER
כיצד אנזים של טפיל עלול לסייע להילחם בלוקמיה בילדים
לוקמיה לימפובלסטית חריפה (ALL) היא הסרטן הדם הנפוץ ביותר בילדות, ולמרות שטיפולים עכשוויים יכולים לרפא ילדים רבים, הם לעיתים קרובות מלוּים בתופעות לוואי קשות ובסיכון לחזרת המחלה. במפנה בלתי צפוי, חוקרים שחקרו חלבון שמשמש טפילים מעיים שכיחים לתקוף תאים אנושיים גילו שאותו מולקולה יכולה לדחוף באופן בררני תאי לוקמיה לעבר השמדה עצמית. באמצעות מעקב אחר האופן שבו החלבון הזה מפר את מאזן הסידן בתוך תאי הסרטן, המחקר מצביע על דרכים חדשות להרוג תאי לוקמיה ובו בזמן מציע מטרות תרופתיות חדשות.
נשק חבוי מטפילים שכיחים
העבודה מתמקדת בלגומאין, אנזים המופרש על ידי פרוטוזואה של מערכת העיכול והמערכת הנשית-שירותית כגון Blastocystis ו-Trichomonas. טפילים אלה משתמשים בלגומאין כחלק מארסנל הפעולה שלהם על מנת לחדור ולפגוע ברקמות המארחות. מחקרים קודמים הראו שלגומאין יכול לחתוך רצפטור על תאים אנושיים הידוע בשם PAR2 ובכך להפעיל עלייה ברמות הסידן בתוך התא. אך גם כאשר הסירו או הפכו את PAR2 לעמיד לחריכה, לגומאין עדיין הצליח להגביר את רמות הסידן, מה שאילץ את החוקרים להסיק שקיים מפעיל נוסף. מאחר שתרופה נפוצה ללוקמיה, L-אספרגינאז, פועלת גם על PAR2 וגם על רצפטור שני שנקרא μ-OR1, העלו החוקרים את השאלה האם לגומאין עשוי גם הוא לנקוט ביותר מדרך אחת כדי להפר את החיים הפנימיים של תאי הלוקמיה.
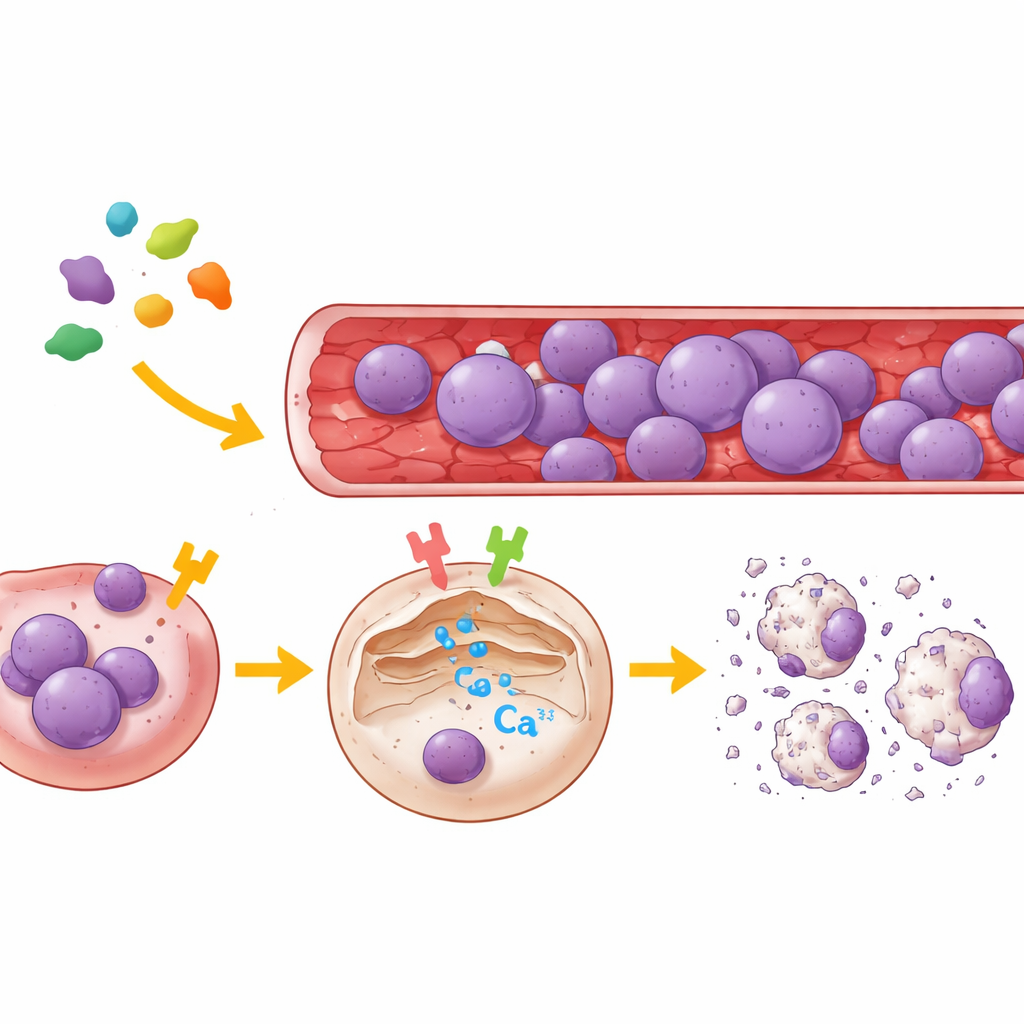
שני מתגים תאיים ששולטים בסידן
כדי למפות את היעדים של לגומאין, הצוות השתמש גם בתאי כליה אנושיים וגם במספר סוגי תאי ALL של מטופלים. הם צמצמו באופן סלקטיבי את PAR2 או את μ-OR1 בתאים אלה, או חסמו אותם בעזרת מעכבים קטנים וספציפיים מאוד, ואז צפו בתנועות הסידן בתא בודד באמצעות גלאי פלואוריסצנטי המדווח על שחרור סידן מהרשתית האנדופלזמטית, מאגר הסידן העיקרי הפנימי של התא. התוצאות היו ברורות: לגומאין גרם לשחרור חזק של סידן מאגר זה רק כאשר לפחות אחד משני הרצפטורים היה פעיל. עיכוב μ-OR1 הטה את ההדף של הסידן באופן ניכר, בעוד שחסימת PAR2 צמצמה את ההגברה במידה קטנה אך מורגשת. כאשר שני הרצפטורים הושתקו, לגומאין לא יכול היה לעורר עוד שחרור סידן. בקווי לוקמיה מסוג B ו-T שונים, μ-OR1 התגלה כמתג השולט ברוב המקרים, כאשר PAR2 ממלא תפקיד תומך.
איתותים לא מאוזנים משפיעים על גורל התא
לאחר שקבעו שלגומאין מתקף על שני הרצפטורים, החוקרים עקבו אחר שרשראות האיתות המקשרות בין מתגי המשטח לאירועים עמוק בתוך התא. PAR2 מזווגת לחלבון G שמפעיל ישירות אנזים שנקרא PLC, שאחר כך פותח שסתומי סידן ברשתית האנדופלזמטית. μ-OR1, לעומת זאת, משדר בעיקר דרך חלבון G שונה המפחית את ייצור המוליך cAMP ובכך מהיר פעילות אנזים הנקרא חלבון קינאז A (PKA). באופן רגיל, PKA מפעילה "בלמים" מדכאים על PLC ומשמרת את פעילותו של חלבון הישרדות בשם BAD במצב שאינו קטלני. כאשר לגומאין מגרה את μ-OR1, רמות ה-cAMP יורדות, פעילות ה-PKA נפחתת, הבלמים משתחררים ו-PLC משתחרר לגרום ליותר סידן להיצא מהמאגרים. במקביל, BAD עובר שינוי למצב שמחליש את מניעת המוות הטבעית של התא.
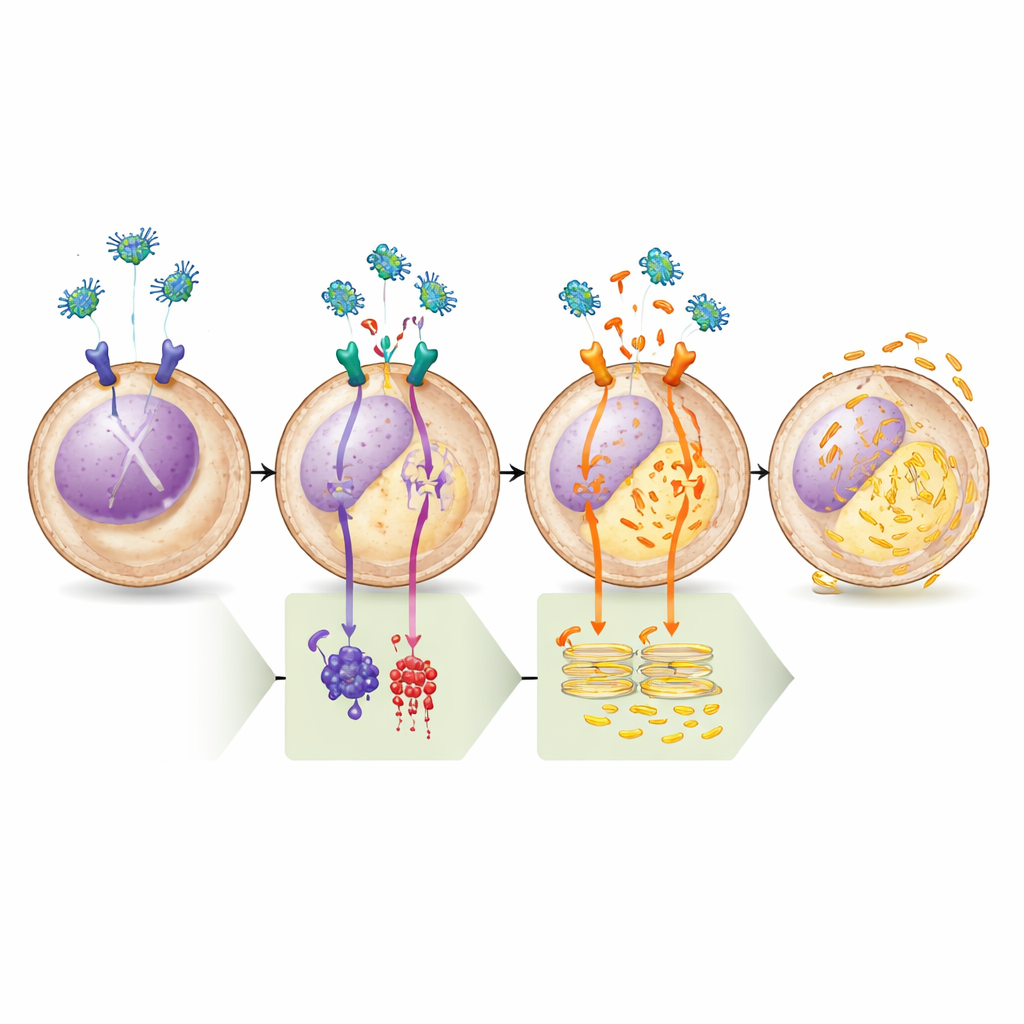
הוכחת המסלול שלב אחרי שלב
הצוות אימת את המודל בעזרת סדרת ניסויים פרמקולוגיים. תרופות שהגבירו cAMP או שהפעילו ישירות את האנזים שיוצר אותו (אדנילאט ציקלאז) חסמו לחלוטין את יכולתו של לגומאין לרוקן סידן מהרשתית האנדופלזמטית, מה שמדגיש את חשיבות הסניף μ-OR1–cAMP–PKA. מנגד, מעכב PKA סלקטיבי מאוד לבדו הספיק לעורר שחרור סידן, והוספת לגומאין לאחר מכן לא הוסיפה אפקט נוסף, מה שמראה כי ברגע ש-PKA כבוי, המסלול כבר מופעל באופן מלא. ניתוחים ביוכימיים אישרו שטיפול בלגומאין הוריד את תגי הפוסט-תרכובת הפוספט על שני PLC ו-BAD באתרים הידועים שנשלטים על ידי PKA, תאימות לשינוי הצפוי בפעילותם. לבסוף, כאשר החוקרים חסמו את תעלת הסידן ברשתית האנדופלזמטית או הסירו חלבון שלד מרכזי הדרוש לתעלת זו, לגומאין כבר לא השפיל תאי מוות, וקישר באופן חזק את תוצאת המוות לחוסר האיזון בסידן.
מה המשמעות של זה לטיפולי לוקמיה בעתיד
בסוף קסקדת האיתות הזו, תאי הלוקמיה חווים שטף ממושך של סידן ממאגריהם הפנימיים, בצירוף לכיבוי מעגל הישרדות קריטי. יחד, השינויים האלה דוחפים את התאים לתכנות מוות, או אפופטוזה. עבור הקורא הרחב, המסר הוא שלגומאין פועל כמו מפר בעזרת שתי ידיים: הוא לוחץ על שתי "כפתורי ההפעלה" של התא לשחרור סידן ובמקביל חותך את החוטים של מערכות הבטיחות שלו. למרות שלגומאין עצמו מקורו בטפילים וידרוש הערכה זהירה לפני שימוש טיפולי, המחקר מדגיש את μ-OR1, PAR2 ו-PKA כמטרות תרופתיות מבטיחות. תרופות המדמות את השיבוש הבררני של מאזן הסידן על ידי לגומאין בתאי לוקמיה — או שמעכבות אסטרטגית של PKA — עשויות יום אחד לסייע בטיפול בחולים שסרטניהם עמידים בפני הטיפולים הקיימים.
ציטוט: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
מילות מפתח: לוקמיה לימפובלסטית חריפה, לגומאין, אותות סידן, קולטני חלבון G (GPCR), אפופטוזה